
1.当氨完全分解成氮气和氢气时, 混合气体对空气的相对密度为
A.1.17 B.0.74
C.0.293 D.1.03
3.有一种复盐A,其分子式为FeSO4·m(NH4)2SO4·nH2O,将9.60克A同足量浓NaOH溶液共热,产生的氨气用100毫升0.50摩/升硫酸吸收,剩余的硫酸再用2.00摩/升NaOH溶液中和,需NaOH溶液25.50毫升,如已知复盐A中硫酸根离子的质量百分组成为49%,试问:
(1)H2SO4吸收了多少摩氨气?
(2)复盐A中NH4+的质量百分组成是多少?
(3)m和n各为多少?
检测提高
2.现有100 ml无色气体, 其中可能有NH3、HCl、CO2、NO中的一种或几种, 把气体通过浓H2SO4, 气体体积减少了30ml, 再把所剩气体通过Na2O2固体, 气体体积又减少了30ml, 气体变为红棕色, 最后剩余气体通入水中, 收集到20ml无色气体(相同条件下), 试计算原混合气体中各组分的体积。
1.某课外活动小组在实验室用下图所示的装置进行实验,验证氨的某些性质并收集少量纯净氮气。试回答:
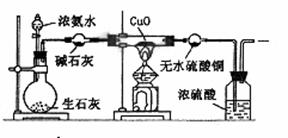
(1)实验前先将仪器按图连接好,然后 再开始实验。
(2)实验进行一段时间后,可以观察到硬质试管内黑色的CuO粉末变成 色,盛无水CuSO4的干燥管内出现 色,并在最后的出气导管处收集到纯净、干燥的N2。根据这些现象,硬质试管中的反应方程式为 ,这个反应说明氨气其有 性。
(3)烧瓶内盛有生石灰,随着浓氨水的滴入,产生氨气,氨气产生的原因是 。
(4)洗气瓶中浓硫酸的主要作用是 。
(5)在最后出气管口收集干燥、纯净的氮气,收集方法是 (填编号)
A.排气法
B.排水法
C.用塑料袋或球胆收集
4.有关氨的实验分析能力不够,不能综合运用有关知识进行实验分析。
纠错训练
3.计算技能不到位,守恒法应用不熟练。
2.NO2溶于水的物质的量浓度的计算弄不清楚,注意不
到溶液体积的问题。
1.对氨分子的结构弄不清楚,和铵盐的性质相混淆。
11.取硫酸铵化肥样品1.48g, 加入足量的NaOH并加热, 充分反应生成的气体, 全部被250mL 0.05mol / L的H2SO4溶液吸收, 多余的H2SO4恰好为15mL 0.2mol / L的NaOH溶液中和, 已知样品中杂质不含氮元素, 计算该化肥中氮元素的量质百分数。
(此题考查根据铵盐的知识进行计算的综合能力。)
第27课时 氨 铵盐(B)
易错现象
10.已知室温下几种盐的溶解度由大到小的顺序是:
NH4Cl > NaCl > NH4HCO3 > NaHCO3, 实验室利用它们在溶解度上的差异制取化工原料B, 其步骤如下:

回答下列问题:
(1)晶体A的名称是 , 生成该晶体的化学方程式是 ;
(2)操作(Ⅰ)和(Ⅱ)的顺序不能颠倒的原因是 ;
(3)操作(Ⅲ)中使用玻璃棒的作用是 ;
(4)第Ⅳ的化学反应方程式是 ;
(5)整个过程中没有涉及到的反应类型是
A.化合反应 B.复分解反应
C.分解反应 D.置换反应
(此题考查实验的设计能力,实验知识的应用能力。)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com