
8.已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8mol电子转移,此时硝酸的还原产物可能是
A.NO2 B.N2O C.NH4NO3 D.NO
(此题考查质量守恒原理、电子守恒原理的运用。)
7.往浅绿色的Fe(NO3)2溶液中,逐滴加入稀盐酸时,溶液的颜色变化应该是
A.颜色变浅 B.逐渐加深
C.没有改变 D.变棕黄色
(次题考查硝酸性质的灵活应用能力。)
6.Cu粉放入稀H2SO4中,加热后无现象,当加入一种盐后,Cu粉质量减少,而溶液变蓝,同时有气体生成,此盐是
A.氯化物 B.硫酸盐
C.硝酸盐 D.碳酸盐
(次题考查硝酸性质的灵活应用能力。)
5.有关硝酸化学性质的叙述中,正确的是
A.稀硝酸使蓝色石蕊试纸变红
B.硝酸能与Na2CO3反应,但不生成CO2
C.硝酸可与Na2S反应制得H2S气体
D.浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色
(此题考查硝酸性质知识的应用能力。)
4.不能大量共存的离子组是
A. H+、Fe2+、Cl-、NO3-
B.NH4+、SO42-、Na+、NO3-
C,Cu2+、Fe3+、NO3-、Cl-
D. H+、Na+、HCO3-、SO42-
(此题考查常见离子的性质的知识。)
3. 0.1mol固体M(NO3)2加热分解,
0.1mol固体M(NO3)2加热分解,
2M(NO3)2 2MO + 4NO2 ↑ + O2↑
将产生的气体用排水法收集,在标准状况下收集到的气体的体积接近
A.5.6L B.4.48L
C.0L D.1.12L
(此题考查信息的接受能力及分析问题的能力。)
2.下列反应中HNO3即表现出酸性,又表现出强氧化性的是
A.Fe2O3+HNO3 B.Ca(OH)2+HNO3
C.P+HNO3 D.FeO+HNO3
(此题考查硝酸的化学性质及应用。)
1. 某单质能与浓硝酸反应,若参加反应的单质与硝酸的物质的量之比为1:4,则该元素在反应中所显示的化合价可能是
A +1 B +2
C +3 D +4
(此题考查硝酸化学性质的运用能力。)
4.(96年上海高考题)某试剂厂用银(含杂质铜)和硝酸(含杂质Fe3+)反应制取硝酸银.步骤如下:
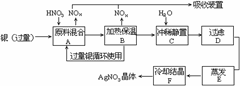 依据上述步骤,完成下列填空:
依据上述步骤,完成下列填空:
(1)溶解银的硝酸应该用 硝酸(填浓或稀).原因是 .
(a)减少过程中产生NOx的量 (b)减少原料银的消耗量 (c)节省硝酸物质的量
(2)步骤B加热保温的作用是 .
(a) 有利于加快反应速度
(b)有利于未反应的硝酸挥发
(c)有利于硝酸充分反应,降低溶液中[H+]
(3)步骤C是为了除去Fe3+、Cu2+等杂质.冲稀静置时发生的化学反应是 。
(a)置换反应 (b)水解反应 (c)氧化-还原反应
产生的沉淀物化学式: .
(此题考查实验设计原理的运用,实验分析能力。)
新活题网站
3. 38.4mg铜跟适量的浓硝酸反应,铜全部作用后,共收集到气体22.4ml(标准状况),反应消耗的HNO3的物质的量可能是
A.1.0×10-3mol B.1.6×10-3mol
C.2.2×10-3mol D.2.4×10-3mol
(此题考查质量守恒原理、电子守恒原理的运用能力。)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com