
1.(1)2Na2O2 + 2H2O = 4NaOH + O2↑
Na2O + H2O = 2NaOH
(2)5,1,4.
(3)G,A,B,F.
讲析:问题(1)对该题有提示作用,联想Na2O2、Na2O与水反应,只有Na2O2与水反应生成氧气,通过测量O2气体的体积,可以计算出Na2O2的量,从而测定Na2O2的纯度。由于是用排水法测量气体的体积,所以气体不需干燥。
15. m(Na2CO3)=7.42g
m(NaHCO3)=1.68g
m(Na2SO4)=1.42g
第29课时 (B卷)
纠错训练
14. NaHCO3%=28.4%
13.(1)1。增大固体质量,继续产生气体。
(2)不足量
(3)55.8% 44.2%
12. (1)TiCl4+4NaH 4NaCl + Ti +2H2
(1)TiCl4+4NaH 4NaCl + Ti +2H2
(2)NaH + H2O = NaOH + H2↑ 1:1。
11.(1)加热。
2NaHCO3
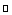 Na2CO3 + CO2 ↑+ H2O
Na2CO3 + CO2 ↑+ H2O
(2)通入CO2。Na2CO3 + CO2 + H2O = 2NaHCO3
(3)加适量的Ca(OH)2溶液过滤。
Ca(OH)2 + Na2CO3 = CaCO3 ↓+ 2NaOH
10. 钠在氧气中燃烧生成过氧化钠,得不到氧化钠。该方法生成的氮气可保护氧化钠不被空气中的氧气氧化。
8.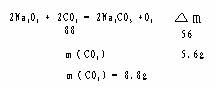
6. 4.6gNa与HCl反应生成0.2gH2。4.6g Mg、Li生成的H2大于0.2g。由平均值原理可知杂质不可能是Mg、Li。
3.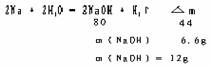
12:19.2 = S:100 S= 62.5g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com