
4.(1)①;③;③;④
 Cu2(OH)2CO3 2CuO+H2O+CO2↑
Cu2(OH)2CO3 2CuO+H2O+CO2↑
 C+2CuO 2Cu+CO2↑
C+2CuO 2Cu+CO2↑
 (2)②Fe2O3+3CO 2Fe+3CO2↑,
(2)②Fe2O3+3CO 2Fe+3CO2↑,
 WO3+3H2
W+3H2O;
WO3+3H2
W+3H2O;
 ③3MnO2+4Al 3Mn+2 Al2O3
③3MnO2+4Al 3Mn+2 Al2O3
④2NaCl 2Na + C12↑
讲析: 4种方法有一个共同点,都是从金属化合物
 里把金属还原出来。焦炭、氢气、一氧化碳是常使用的还原剂,方法①、②一般冶炼不活泼或较活泼的金属,如铜、铁等。活泼金属置换法,一般在水溶液中进行,也可以是粉末状。在工业上利用铝热反应,用铝作还原剂冶炼难溶的金属,如钒、铬、锰等。活泼的金属一般采用电解的方法,电解熔融的氯化钠、氯化镁、氧化铝制取钠、镁、铝。
里把金属还原出来。焦炭、氢气、一氧化碳是常使用的还原剂,方法①、②一般冶炼不活泼或较活泼的金属,如铜、铁等。活泼金属置换法,一般在水溶液中进行,也可以是粉末状。在工业上利用铝热反应,用铝作还原剂冶炼难溶的金属,如钒、铬、锰等。活泼的金属一般采用电解的方法,电解熔融的氯化钠、氯化镁、氧化铝制取钠、镁、铝。
(Ⅰ)孔雀石的主要成分是Cu2(OH)2CO3,加热分解:
Cu2(OH)2CO3 2CuO+H2O+CO2↑
 火烧时,使用的树木变为木炭,CuO再与木炭反应,产生铜,属于焦炭法。
火烧时,使用的树木变为木炭,CuO再与木炭反应,产生铜,属于焦炭法。
C+2CuO 2Cu+CO2↑ 符合①
(Ⅱ)湿法炼铜是我国西汉时期用铁从某些含铜化合物的溶液中置换出铜,属活泼金属置换法。
Fe+CuSO4=Fe SO4+Cu 适合于③
(Ⅲ)是使铝粉和Cr2O3的混合物在高温下反应,置换出铬,反应产生的热量使铬熔化而分离。
 2Al+ Cr2O3 Al2O3
+2Cr 适合于③
2Al+ Cr2O3 Al2O3
+2Cr 适合于③
 (Ⅳ)从光卤石(KCl·MgCl2·6H2O)中可得到六水合氯化镁晶体,再采用通电分解熔融的氯化镁的方法制取镁。
(Ⅳ)从光卤石(KCl·MgCl2·6H2O)中可得到六水合氯化镁晶体,再采用通电分解熔融的氯化镁的方法制取镁。
MgCl2 Mg + C12↑ 符合④
新活题网站
1.C 2.C 3.D
讲析:1.在元素周期表中,金属与非金属元素分界线附近的金属元素往往表现一定的非金属性,②错;价电子数多少与失电子难易不一致,故③错;铵盐中不含金属元素,故④错。金属晶体中只含阳离子,而不含阴离子。
 讲析:3.硬铝是Al、Cu、Mg、Mn、Si的合金,黄铜是Cu、Zn的合金,钢铁主要是Fe、C合金。水银是金属单质。
讲析:3.硬铝是Al、Cu、Mg、Mn、Si的合金,黄铜是Cu、Zn的合金,钢铁主要是Fe、C合金。水银是金属单质。
13.超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为:Al2O3+N2+3C 2AlN+3CO由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。为测定该产品中有关成分的含量,进行了以下两个实验:
2AlN+3CO由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。为测定该产品中有关成分的含量,进行了以下两个实验:
(1)称取10.00g样品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,并放出氨气3.36L(标准状况)。
①上述反应的化学方程式为 ;
②该样品中的A1N的质量分数为 ;
(2)另取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AlN不跟O2反应)。该样品中含杂质炭 g。
第33课时 (A卷)答案与讲析
典型题点击
12.纳米材料是指由极细晶粒组成,纳米粒子是指直径为1-100nm的超细粒子。纳米材料在催化、光学、磁性力学等方面具有许多奇异的性能。有一种第ⅢA-VA族元素的二元化合物纳米粒子,由元素M和元素A组成。制备这种纳米粒子的方法是:在真空的容器中用电阻丝加热,首先发生M的单质与Fe3O4粉末的置换反应,利用该反应放出的热引发化合物X与化合物Y的反应,从而制得纳米粒子。巳知:X由元素M和元素B组成,Y由元素N和元素A组成。M、N、A、B均为同一短周期元素,且原于序数均为奇数。试回答:
(1)M和Fe3O4发生反应的化学方程式为:
(2)制取这种纳米粒子的化学反应方程式为:
(3)用这种方法制取纳米粒子都必须在真空的容器中或惰性气氛中进行,其原因是:
。
11.随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”。已知钒的原子序数是23,回答下列问题:
(1)钒被认为是一种稀土元素,广泛分散于各种矿物中。钾钒铀矿中的钒原于是最外层已达8电子稳定结构,其化学式为K2H6U2V2O15,若用氧化物的形式表示,该化合物的化学式为 ;
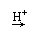 (2)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO2+,再用盐酸、硫酸亚铁、草酸等测定钒。总反应可表示为:
(2)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO2+,再用盐酸、硫酸亚铁、草酸等测定钒。总反应可表示为:
VO2++H2C2O4 VO++CO2+H2O(未配平)
其中的还原剂是 。若消耗0.9mol草酸,所对应钒元素的质量是 g。
10.工业上常用Na制备钛、锆、铌、钽等。如制钛,常用如下反应步骤;
(1)用90%浓H2SO4溶解钛铁矿(FeTiO3),反应式为:FeTiO3+3 H2SO4=FeSO4+Ti(SO4)2 +3H2O。
在除去不溶性杂质后,结晶析出FeSO4·7H2O时,为保持较高的酸度不能加水,其原因可能是
A.防止Fe2+被氧化
B.防止Ti(SO4)2水解
C.减少FeSO4·7H2O的溶解量
D.减少Ti(SO4)2的溶解量
(2)在除去杂质后,又需加大量水稀释以降低酸度,同时加热以生成TiO(OH)2沉淀,过滤,将TiO(OH)2加热分解即得钛白粉(TiO2)。除杂后加水稀释和加热的目的是
。
(3)在高温HCl气流中,TiO2可转化为TiCl4,反应方程式为: 。
(4)将TiCl4与Na共熔即可得Ti,反应式为
,若用TiCl4溶液与Na反应制Ti,不能达到预期目的,原因是
。
9.已知有关物质的熔沸点数据如下表:
|
|
MgO |
Al2O3 |
MgCl2 |
AlCl3 |
|
熔点/℃ |
2852 |
2072 |
714 |
190(2.5×105Pa) |
|
沸点/℃ |
3600 |
2982 |
1412 |
182.7 |
请参考上述数据回答下列问题:
工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁?理由是
。
为什么不用电解AlCl3的方法生产铝?理由是
。
8.现用一包可能由镁、铝、铁、铜、银几种金属组成的混合物进行如下实验:
(1)该混合物和过量的金属钾一起投入足量的水里立即有气体产生,反应停止后发现有少量残留固体。
(2)向上述固、液混合物逐滴加入盐酸,发现有白色沉淀产生,当盐酸滴加至过量时,沉淀部分消失伴有气体逸出,这时溶液显浅绿色。
(3)向(2)所得固、液混合物中加入足量稀硝酸,加热,发现残留固体溶解,最终得到澄清的溶液。
问:(1)上述混合物中一定存在的金属是 ,一定不存在的金属是 ,可能存在的金属是 。
(2)写出上述实验过程中所有肯定发生的化学方程式。
7.将5 g某金属加入100mL4mol·L-1的硫酸溶液中,当硫酸浓度降到原浓度的一半时(设溶液体积不变),金属还没有全部溶解,该金属可能是( )
A.铝 B.锌 C.铁 D.镁
6.将ag锌粉、A1粉、Mg粉的混合物与一定量的溶质质量分数为25%的稀硫酸恰好完全反应,加热蒸发水分后得固体bg(不含结晶水),则反应生成的H2质量是( )
A.(b-a)g B.(a-b)g
C.(b-a)/48g D.无法计算
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com