
1.B
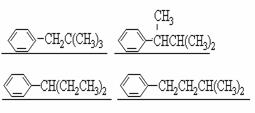 讲析:此题是考查同分异构体的书写和物理性质的特点,只要把题中所说的二甲苯一溴代物的6种同分异构体写出来,便可以得到题解。已知邻-二甲苯的一溴代物有两种,应该是题目中所示的214、215℃;间-二甲苯的一溴代物有三种,应该是题目中所示的204、205、206℃;对-二甲苯的一溴代物有一种,其沸点为234℃。
讲析:此题是考查同分异构体的书写和物理性质的特点,只要把题中所说的二甲苯一溴代物的6种同分异构体写出来,便可以得到题解。已知邻-二甲苯的一溴代物有两种,应该是题目中所示的214、215℃;间-二甲苯的一溴代物有三种,应该是题目中所示的204、205、206℃;对-二甲苯的一溴代物有一种,其沸点为234℃。
16.使浓硫酸增重10.8g,即生成的水为10.8g,通过NaOH溶液,气体质量减少39.6g,即生成CO2为39.6g,则每mol这种苯的同系物中含C、H原子的物质的量为:

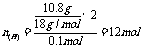

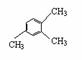 所以这种苯的同系物的分子式为C9H12,而这种烃没有四氯代物,则应是苯环上有三个甲基,按一氯、二氯各
所以这种苯的同系物的分子式为C9H12,而这种烃没有四氯代物,则应是苯环上有三个甲基,按一氯、二氯各
为3种,则其结构简式应为:
第37课时 (B卷)
纠错训练
15.(1) n-1(2)n+3(3)C80 、C160H320
1. C 2.B 3.C 4.B 5.A 6.B 7.A 8.D 9.D 10.BC 11.A 12.B 13.AD 14.B
讲析:1.甲苯中有四种等效氢,而甲基环己烷有五中等效氢,故其同分异构体有五种。 2.聚苯乙烯树脂、苯、乙炔的碳氢比都是1∶1,故无论它们如何混合其质量比都是一定的。3.既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的有机物必须具有不饱和结构,如烯烃、炔烃等。4.可以把四氯苯中的四个氯原子、二个氢原子换成二个氯原子、四个氢原子,因此它们的同分异构体的数目相同。6.可把本题中有机物的结构看成是甲烷中的四个氢被苯所取代,从而得到正确答案。7.这道题要求学生掌握常见的混合物的分离方法,如分馏、蒸馏、洗气、分液、萃取、过滤等。 9.石油催化裂化的目的是提高汽油的产量和质量。 10.辛烷有不同种裂化方式:
(1)C8H18 C4H10+C4H8,C4H10
C4H10+C4H8,C4H10 CH4+C3H6或C4H10
CH4+C3H6或C4H10 C2H4+C2H6
C2H4+C2H6
(2)C8H18 C2H4+C6H14,C6H14
C2H4+C6H14,C6H14 C3H6+C3H8,C3H8
C3H6+C3H8,C3H8 CH4+C2H4(3)C8H18
CH4+C2H4(3)C8H18 C3H6+C5H12,C5H12
C3H6+C5H12,C5H12 CH4+C4H8或C5H12
CH4+C4H8或C5H12 C2H4+C3H8或C5H12
C2H4+C3H8或C5H12 C2H6+C3H6。若按照第(1)种情况裂化则混合气体的平均相对分子质量为114/3=38;若按照第(2)或(3)种情况裂化则混合气体的平均相对分子质量为114/4=28.5。所以只要在混合气体的平均相对分子质量在28.5-38之间都符合题意。 11.根据题意5个氯原子在环戊烷平面上可分为五上(或五下),四上一下(或四下一上),三上二下(或三下二上)三种情况。其中前两种情况分别只有一种结构,而三上二下有两中同分异构体。所以共有四种同分异构体。 12.首先要了解溴苯的制取,在生成溴苯的同时,有溴化氢生成,得到的粗苯中会含有杂质。而后就应考虑操作的顺序问题。先用水洗可以除去水溶性杂质,如溴化氢、少量的溴;然后用10%的NaOH溶液洗,可把溴转变为水溶性的次溴酸钠除去;然后再用水洗一次,把残存的NaOH除去;接着用干燥剂除水;最后蒸馏得到纯溴苯。 13. 苯并[a]芘的正确写法是三环成一直线,另两个环的中心连线与之平行,另两个环的起点在三个环的两个环的中间,换而言之,在三个环的两个环之间嵌入一个环。可以看出(Ⅰ)(Ⅱ)A、D都符合要求,所以是等同的。
14.C式的两个苯环的连线起点和终点都在三个苯环的连线中间,所以少了一个碳原子,少了一个烯键,不是同分异构体。
C2H6+C3H6。若按照第(1)种情况裂化则混合气体的平均相对分子质量为114/3=38;若按照第(2)或(3)种情况裂化则混合气体的平均相对分子质量为114/4=28.5。所以只要在混合气体的平均相对分子质量在28.5-38之间都符合题意。 11.根据题意5个氯原子在环戊烷平面上可分为五上(或五下),四上一下(或四下一上),三上二下(或三下二上)三种情况。其中前两种情况分别只有一种结构,而三上二下有两中同分异构体。所以共有四种同分异构体。 12.首先要了解溴苯的制取,在生成溴苯的同时,有溴化氢生成,得到的粗苯中会含有杂质。而后就应考虑操作的顺序问题。先用水洗可以除去水溶性杂质,如溴化氢、少量的溴;然后用10%的NaOH溶液洗,可把溴转变为水溶性的次溴酸钠除去;然后再用水洗一次,把残存的NaOH除去;接着用干燥剂除水;最后蒸馏得到纯溴苯。 13. 苯并[a]芘的正确写法是三环成一直线,另两个环的中心连线与之平行,另两个环的起点在三个环的两个环的中间,换而言之,在三个环的两个环之间嵌入一个环。可以看出(Ⅰ)(Ⅱ)A、D都符合要求,所以是等同的。
14.C式的两个苯环的连线起点和终点都在三个苯环的连线中间,所以少了一个碳原子,少了一个烯键,不是同分异构体。
3.(1)C、A、B
(2)硝基化合物的同分异构体是氨基酸,一硝基分别用一个氨基和一个羧基取代,就得到了所要写的的结构简式。例如: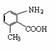 或其位置异构。
或其位置异构。
新活题网站
2. 硼氮苯和苯具有相似的分子结构、且氮、硼两种原子互相交替,解题可以这样考虑,若一种氯原子首先取代硼原子上的氢原子,根据分子的对称性另一种氯原子有3种可能的取代位置;接下考虑,若一种氯原子取代氮原子则有1种取代位置。
1.D 2.C
讲析:1.虽然此化合物较复杂,但道理是一样的。首先保证萘的序号编排原则的正确,再考虑各取代基序号之和最小。
17. (1)据平均组成中含碳2.5,则A、B的可能组合和体积比为:
|
A |
B |
体积比 |
|
CH4 |
C4H8 |
1 :1 |
|
CH4 |
C3H6 |
1:3 |
|
C2H6 |
C3H6 |
1:1 |
|
C2H6 |
C4H8 |
3:1 |
(2)CxHy+(x+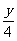 )O2→xCO2+
)O2→xCO2+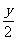 H2O
△v
H2O
△v
1 x+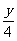 x
x
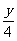 -1
-1
1 (1+9)×6.25%
即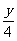 -1=10×6.25% y=6.5
-1=10×6.25% y=6.5
则A、B混合物平均组成为 C2.5H6.5
通过讨论:A为C2H6,B为C4H8.
16.(1)CaC2+2H2O
 Ca(OH)2+C2H2↑; 测定气体体积;避免空气中水蒸气与CaC2作用而产生误差。
Ca(OH)2+C2H2↑; 测定气体体积;避免空气中水蒸气与CaC2作用而产生误差。
(2)B中水排完后导致空排,以至产生误差;0.7g
(3)有利于漏斗中水滴下,同时可避免气体从漏斗中逸出。
(4)
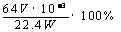 或
或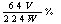
讲析:本题是一个综合实验题,首先应弄清实验原理和实验目的,然后根据原理和题目的要求回答问题。该实验测定CaC2的纯度是通过测定C2H2的体积来实现的,测定C2H2的体积所用的装置就是B、C。体系的压强比空气略大,才能把B中的水压出。为了防止气体从分液漏斗逸出以及有利于水从漏斗中滴下,在漏斗与烧瓶之间加一个导管。在计算中应先根据体积计算CaC2的量(由化学方程式计算)
15.(1)NH4HCO3;CaC2(2)CaC2+2H2O Ca(OH)2+C2H2↑;
Ca(OH)2+C2H2↑;
NH4HCO3+Ca(OH)2=CaCO3↓ +NH3↑ + 2H2O
(3)2NH3+CO2+H2O+Ca2+=CaCO3+2NH4+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com