
4.98≤W≤12.45 V(CO2)=1680-134.9W(mL)
注:V(CO2)=[0.075-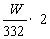 ]×22400(mL)也对
]×22400(mL)也对
2.(1) 504
(2)由题意可知,天然碱含NaHCO3、Na2CO3
n(NaHCO3)=2n(CO2)=2×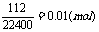
n(Na2CO3)=
n(H2O)=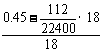 =0.02(mol)
=0.02(mol)
∴天然碱组成:2Na2CO3·NaHCO3·2H2O
(3)2.5
(4)0<W≤4.98 V(CO2)=202.4W(mL)
V(CO2)=  也对
也对
1.(1)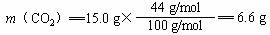
m(CO2+H2O)= 9.3 g m(H2O)=9.3 g-6.6 g =2.7 g
(2)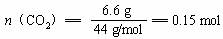
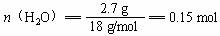
分子中C︰H = 1︰2
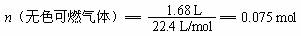
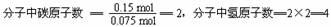
所以该气体的分子式是C2H4
(3)C4H6和H2(或C3H8和CO,C3H6和CH2O等)
讲析:因为单一气体为C2H4,现为等物质的量的两种气体之混合物,所以在2 mol混合气体中,应含有4 mol C原子,8 mol H原子,这两种气体可能是C4H6和H2。
22.(99上海)某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO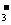 六种离子。
六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是 、 、 。
乙厂的废水中含有另外三种离子。如果加一定量 (选填:活性炭、硫酸亚铁、铁粉)。可以回收其中的金属 (填写金属元素符号)。
另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的 (填写离子符号)转化为沉淀。经过滤后的废水主要含 ,可用来浇灌农田。
21.有一种白色粉末,含有下列阴离子和阳离子中的几种:阴离子:S2-、Cl-、NO3-、SO42-、CO32-、HCO3- 、MnO4-,阳离子:Na+、Mg2+、Al3+、Ba2+、Fe2+、Fe3+、Cu2+、NH4+,将该白色粉末进行下列实验,观察到的现象如下:
|
实验操作 |
现象 |
|
a.取少量粉末,加水、振荡 |
全部溶解、溶液无色透明 |
|
b.向所得溶液中慢慢滴入苛性钠并加热 |
无明显现象 |
|
c.取少量粉末,加盐酸 |
无明显现象 |
|
d.取少量粉末,加稀H2SO4和稀混合液 |
有白色沉淀生成 |
根据实验推断(沉淀A不溶于稀HNO3)
(1)a实验中,可推断粉末中,不可能有 离子;
(2)从b实验中,可推断粉末中,不可能有
离子;
(3)从c实验中,可推断粉末中,不可能有
离子;
(4)从d实验中,可推断粉末中,不可能有
离子,必定含 离子;
(5)综上所述,粉末中还可能含有 离子。
20.过氧化氢是一种常见的氧化剂,医疗上可作外科消毒剂,且在一定条件下能发生分解反应。①现将过氧化氢溶液加入碘化钾和硫酸的混合溶液中,溶液变为棕色,写出表示此变化的离子方程式是 。
②如果将9.60×10-4molAO4-离子在溶液中还原成较低价态,需用0.100 mol•L-1H2O2溶液24.0mL,试通过计算确定A元素的最终价态为 。
19.某待测液中可能含有Fe2+、Fe3+、Ag +、Al 3+、Ba 2+、Ca 2+、NH 4 +等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的)。根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由。
答: 。
(2)写出沉淀D的分子式: ;
(3)写出从溶液D生成沉淀E的反应的离子方程式:
。
18.(2002年上海高考题)在pH=1的无色溶液中能大量共存的离子组是( )
A.NH4+ Mg2+ SO42- Cl- B.Ba2+ K+ OH- NO3-
C.Al3+ Cu2+ SO42- Cl- D.Na+ Ca2+ Cl- AlO2-
17.(2000年上海高考题)下列各组离子在溶液中能大量共存的是( )
A.Ca2+ HCO3- Cl- K+ B.Al3+ AlO2- HCO3- Na+
C.Fe2+ NH4+ SO42- S2- D.Fe3+ SCN- Na+ CO32-
16.(98年上海高考题)下列各组离子在水溶液中能大量共存的是 ( )
A.Na+ HS- Cu2+ Cl- B.HS- Na+ OH- K+
C.K+ CO32- Br- AlO2- D.H+ Cl- Na+ SO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com