
9.(1)2KCl O3+6NaHSO3==3Na2SO4+2KCl+3H2SO4,溶液中c(H+)增大,化学反应速率加快。
(2)随着反应的进行,H2SO4和NaHSO3之间反应使H+及HSO3-浓度减小,后期化学反应速率减慢。
8.(1)0.25 mol·(L·min)-1 (2)0.25 mol·(L·min)-1
(3)因在同一反应里,v(HCl)=2 v(FeCl2),对比前2min和后4min的反应速率知前2min时HCl的浓度较大,所以前2min反应速率较快(实际上随着反应的进行,反应物浓度不断减小,反应速率肯定要减慢。)
7.升高温度和使用催化剂。升高温度,反应物分子的能量增加,使一部分原来能量较低的分子变成活化分子;使用催化剂能够降低反应所需要的能量,从而使更多的反应物分子成为活化分子;因此,升高温度和使用催化剂都可以增大反应物分子中活化分子的百分数。
2.0m= 则n=1/2
则n=1/2
1.0n=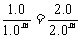 则m=1
则m=1
选择c(H2)=2.0 mol/L的两种情况:
1.C 2.CD 3.A 4.BD 5.D 6.B
讲析:2.若反应物为固体或纯液体,增大其量对反应速率无影响。压强只是对有气体参加或生成的反应而言,改变压强会改变速率。3.温度升高,反应速率都增大。对于一个可逆反应来说,吸热反应速率增大的倍数比放热反应增大的倍数要大。5. 选择c(Cl2)=1.0 mol/L的两种情况:
4.(1)反应速率可用反应物的消耗速率,也可用产物的生成速率来表示。(2)直线、抛物线。(3)Ni,它的腐蚀速率随时间的增长比镁的要慢。
讲析:4.(1)金属因高温氧化反应,遭到破坏是常见的一种腐蚀现象。然而,不同的金属因其所形成的氧化膜致密程度不同,它们的耐腐蚀性亦不同。化学反应的快慢既可由反应物消耗速率表示,也可由生成物的生成速率来表示,显然,金属的腐蚀速率可用其氧化膜的生长速率表示。(2)根据题给数据不难导出以下数学关系式:MgO膜厚Y与时间t的关系为:Y=0.05at;NiO膜厚Y’与时间t的关系为Y’=bt1/2。由数学知识知,前者为直线型,后者为抛物线型。(3)据此可知Y’随时间t增长要比Y随时间t增长得慢,故而镍的耐高温氧化腐蚀性要比镁的好。
新活题网站
2.影响化学反应速率的因素有温度、浓度、压强、催化剂,还有增大固体反应物的有效表面积等。从稀硫酸改用98%浓硫酸,虽然浓度增大了,但浓硫酸使铁钝化而不能产生氢气。滴加少量硫酸铜溶液,铁与其发生置换反应,形成Cu-Fe原电池,使反应速率加快。 3.从曲线变化的趋势看,在反应过程中物质N逐渐减少,物质M逐渐增多。当时间为0时, 容器中M和N两物质的物质的量均不为0,且分别为2mol和8mol;t1时,N物质由8mol减至6mol,减少量为2mol,M物质由2mol增至3mol,增加量为1mol,说明M,N之间的量变关系为:M 2N或2N
2N或2N M。t1时容器中有M物质3mol,N物质6mol,即N的浓度是M浓度的2倍:t2时,M、 N两物质的物质的量相等,且为4mol,但不是正、逆反应速率相等;t3时,M、N的物质的量不随时间的变化而改变,是化学平衡状态的特征,说明正、逆反应速率相等。综上分析,答案为D。
M。t1时容器中有M物质3mol,N物质6mol,即N的浓度是M浓度的2倍:t2时,M、 N两物质的物质的量相等,且为4mol,但不是正、逆反应速率相等;t3时,M、N的物质的量不随时间的变化而改变,是化学平衡状态的特征,说明正、逆反应速率相等。综上分析,答案为D。
1.BD 2.B 3.D
 讲析:1.因A是固态物质,一般不用浓度变化表示反应速率,A不正确。v= 求的是平均反应速率。C不正确。
讲析:1.因A是固态物质,一般不用浓度变化表示反应速率,A不正确。v= 求的是平均反应速率。C不正确。
16.Ⅰ.某天然油脂A的分子式为C57H106O6。1mol该油脂水解可得到1 mol甘油、1 mol不饱和脂肪酸B和2 mol直链饱和脂肪酸C。经测定B的相对分子质量为280,原子个数比为C∶H∶O=9∶16∶1。
(1)写出B的分子式:_____________________。
(2)写出C的结构简式:________;C的名称是_________。
(3)写出含5个碳原子的C同系物的同分异构体的结构简式:___________________________________________。
|
|
 RCH=CHR’
RCOOH++RCOOH,常利用该反应的产物反推含碳碳双键化合物的结构。在催化剂存在下,1 mol不饱和脂肪酸B和1 mol氢气反应后经处理得到D和E的混合物,D和E互为同分异构体。当D和E的混合物与碱性KMnO4溶液共热后酸化,得到如下四种产物: HOOC-(CH2)10―COOH
、CH3―(CH2)7-COOH、HOOC-(CH2)7―COOH 、CH3―(CH2)4-COOH
RCH=CHR’
RCOOH++RCOOH,常利用该反应的产物反推含碳碳双键化合物的结构。在催化剂存在下,1 mol不饱和脂肪酸B和1 mol氢气反应后经处理得到D和E的混合物,D和E互为同分异构体。当D和E的混合物与碱性KMnO4溶液共热后酸化,得到如下四种产物: HOOC-(CH2)10―COOH
、CH3―(CH2)7-COOH、HOOC-(CH2)7―COOH 、CH3―(CH2)4-COOH
(4)写出D和E的结构简式:____________,__________。
(5)写出B的结构简式:__________________________。
(6)写出天然油脂A的一种可能结构简式:____________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com