
3.[江苏省泗阳中学2009届高三第一次摸底考试](10分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)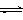 CH3OH(g)+H2O(g) △H=-49.0kJ/mol
CH3OH(g)+H2O(g) △H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)=___________mol/(L·min)。
②该反应的平衡常数表达式为__________________。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2 CO2=2 CO+O2,CO可用作燃料。
已知该反应的阳极反应为:4OH――4e―=O2↑+2H2O
则阴极反应式为:________________________________。
有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断是否可行并说出理由:__________________________________________。
答案. ⑴①0.225 ② ③C、D
⑵ 2CO2+4e―+2H2O=2 CO+4OH―
不可行,该反应是一个焓增、熵减的反应,任何情况下不能自发进行 (每空2分,共10分)
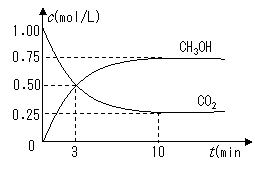
2. [江苏省泗阳中学2009届高三第一次摸底考试]将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
[江苏省泗阳中学2009届高三第一次摸底考试]将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是
A.镁比铝活泼,镁失去电子被氧化成Mg2+
B.铝是电池负极,开始工作时溶液中会立即
有白色沉淀生成
C.该装置的内、外电路中,均是电子的定向
移动形成电流
D.该装置开始工作时,铝片表面的氧化膜可不必处理
1.[江苏省泗阳中学2009届高三第一次摸底考试]下列反应的离子方程式中正确的是
A.碳酸氢钠的水解反应:HCO3-+H2O=CO32-+ H3O+
B.在NaHSO4溶液中加Ba(OH)2至中性:H++SO42-+Ba2++OH-= BaSO4↓+H2O
C.以铜作电极电解硫酸铜溶液:2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.用侯氏制碱法制得NaHCO3 :Na++NH3+CO2+H2O = NaHCO3↓+NH4+
⑴制皂过程:
将油脂与 混合煮沸,得到皂化混合液,再向混合液中加入 ,再过滤即可得到高级脂肪酸盐。
[思考] ①所加入的物质的作用是什么?
②由高级脂肪酸钠盐制成的肥皂,称为钠肥皂,又称 ;由高级脂肪酸钾盐制成的肥皂,称为钾肥皂,又称 。
③硬脂酸钠溶液能与 、 反应,生成难溶物,降低肥皂的洗涤效果。
⑵"肥皂"的去污原理
⑶"肥皂"与"合成洗涤剂"的比较
⑷"合成洗涤剂"的优点、缺点及发展方向
试题枚举:
[例1]下列各组中,所含物质不是同系物的是 ( )
A.硬脂酸甘油酯与三乙酸甘油酯 B.油酸与丙烯酸`
C.甘油与软脂酸 D.丙烯酸与软脂酸
解析:硬脂酸与乙酸同为饱和一元酸,故A组为同系物;油酸与丙烯酸同为含一个C=C的一元酸,故B组为同系物;C组中甘油为醇,D组中软脂酸为饱和一元酸
答案:CD
[例2]下列关于油脂的叙述不正确的是 ( )
A.天然油脂没有固定的熔点和沸点
B.油脂是高级脂肪酸和甘油所生成的酯
C.油脂一般易溶于乙醇、苯、氯仿
D.油脂都不能使溴水和酸性高锰酸钾溶液褪色
解析:天然油脂是混合物,所以A正确;B叙述表达了油脂定义的内涵,B正确;油脂易溶于有机溶剂,C正确;油是不饱和脂肪酸的甘油酯,含有不饱和烃基,D错误。
答案:BC
[例3]某天然油脂1g,需0.24gNaOH才能完全皂化,又知该油脂100g完全催化加氢,需H21.2g,则1mol油脂分子中平均含的双键个数为( )
A.6mol B.3mol C.4mol D.5mol
解析:油脂中含有3个酯基,故1mol的油脂皂化时需3mol的NaOH,所以根据题给条件可算出油脂的相对分子质量为500;100克油脂即0.2mol油脂能与0.6mol的H2加成,故1mol油脂分子中含有的双键个数为3mol。
答案:B
[例4]可以判断油脂皂化反应基本完成的现象是( )
A.反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D.反应后静置,反应液不分层
解析:油脂与NaOH溶液未反应前分层,发生完全皂化反应后,生成高级脂肪酸钠盐,甘油和水的混合物,不会出现分层现象,故C错。高级脂肪酸钠为强碱弱酸盐,水解呈碱性,即皂化反应前后反应液均呈碱性,不能依据石蕊试纸变蓝判断反应是否完成,故A、B错。
答案:D
[例5]如果11.5t硬脂酸甘油酯在NaOH溶液中皂化时,仅有85%的硬脂酸甘油酯反应,得到的硬脂酸钠可制成含硬脂酸钠60%的肥皂多少吨?
解析:油脂都是三元酯,所以皂化反应时,1mol硬脂酸甘油酯在NaOH溶液中生成3mol硬脂酸钠。所以,11.5t×85%×3×306÷890÷60%=16.80t
答案:16.80t
⒈油脂的定义: 。
常见的高级脂肪酸有: 、 、 、 。
⒉油脂的结构通式: 。在结构式中,R1,R2,R3相同的称为 ,不相同的称为 。天然油脂通常为 。
[思考]油脂是不是高分子化合物?混甘油酯是混合物吗?
⒊油脂是 和 的合称。 在常温下呈液态,如:植物油。 在常温下呈固态,如:动物油。
⒋油脂的物理性质:
密度比水 ;不溶于 ,易溶于 ;粘度 ;油腻感;好溶剂;熔点 。
⒌油脂的化学性质
油脂是重要的供能物质。油"所含"烃基"的饱和度低,则其熔点低,常温下呈液态。"脂肪"所含"烃基"的饱和度高,则其熔点高,常温下呈固态。所以,可以采用"加氢"的方法,把饱和度低的烃其变成饱和度高的烃基,从而将"油"变"脂肪"。
⑴氢化反应(硬化反应)
写出油酸甘油酯加氢的化学方程式:
应用: 。
⑵水解反应:
①酸性水解:
写出硬脂酸甘油酯酸性水解的方程式:
应用: 。
②碱性水解(皂化反应):
写出硬脂酸甘油酯碱性水解的方程式:
应用: 。
2. ( 7 分)臭氧可用于净化空气,漂白饮用水,杀菌,处理工业废物和作为漂白剂。但臭氧能刺激粘液膜,空气中臭氧的体积分数超过0.1 PPm ( PPm 表示百力分之一)对人体是不安全的。臭氧能与碘化钾溶液反应: 为测定大气中臭氧的含量,进行如下操作: ① 将标准状况下 33 . 6L的空气试样缓缓通入KI溶液,使之完全反应;
②在所得溶液中用 0 . 01 mol / L 的 Na2S2O3溶液 60 . 00mL 恰好与之完全反应。(反应方程式为:
为测定大气中臭氧的含量,进行如下操作: ① 将标准状况下 33 . 6L的空气试样缓缓通入KI溶液,使之完全反应;
②在所得溶液中用 0 . 01 mol / L 的 Na2S2O3溶液 60 . 00mL 恰好与之完全反应。(反应方程式为:
 设反应过程中溶液的体积变化忽略不 计)
设反应过程中溶液的体积变化忽略不 计)
( l )试通过计算说明该空气试样中臭氧的体积分数对人体是否安全?
( 2 )取步骤 ① 所得溶液的1 / 50 ,欲将其中所含 KOH 完全中和,需 0 . 0012 mol / L 的盐酸体积是多少毫升?
1.(10分)以下是以绿矾、碳酸氢铵和氯化钾为原料制备生产市场较紧俏的硫酸钾产品的新工艺 。已知:反应(Ⅰ)的化学方程式为:
FeSO4•7H2O+2NH4HCO3= FeCO3↓+(NH4)2SO4+CO2↑+H2O
反应(Ⅱ)的化学方程式为:(NH4)2SO4+2KC1=K2SO4+ 2NH4Cl
工艺流程如下:
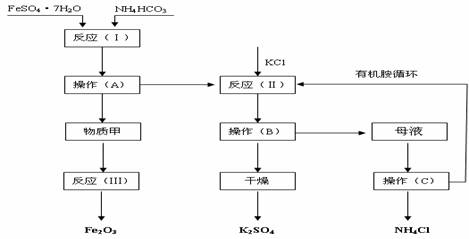
试回答下列问题:
⑴ 该工艺中的副产品是 。(填化学式)
⑵ 操作C的名称为 。
⑶ 原料绿矾、碳酸氢铵的最佳投料比是 (质量比)时,FeSO4的转化率大于95%。
⑷ 物质甲是 (填化学式),反应(Ⅲ)是甲物质与适量空气煅烧,温度为700-800℃,煅烧时间为1-1.5 h时可获得符合国标一级品要求的氧化铁红,其化学方程式是__________。
16.已知函数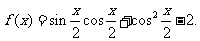
(Ⅰ)将函数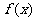 化简成
化简成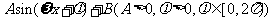 的形式,并指出
的形式,并指出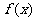 的周期;
的周期;
(Ⅱ)求函数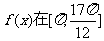 上的最大值和最小值。
上的最大值和最小值。
解:(Ⅰ)f(x)=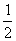 sinx+
sinx+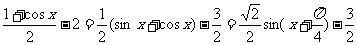 .
.
故f(x)的周期为2kπ{k∈Z且k≠0}.
(Ⅱ)由π≤x≤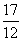 π,得
π,得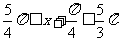 .因为f(x)=
.因为f(x)=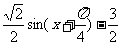 在[
在[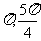 ]上是减函数,在[
]上是减函数,在[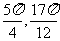 ]上是增函数.故当x=
]上是增函数.故当x=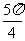 时,f(x)有最小值-
时,f(x)有最小值-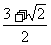 ;而f(π)=-2,f(
;而f(π)=-2,f(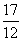 π)=-
π)=-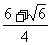 <-2,所以当x=π时,f(x)有最大值-2。
<-2,所以当x=π时,f(x)有最大值-2。
15.已知函数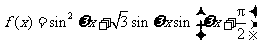 (
( )的最小正周期为
)的最小正周期为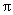
(Ⅰ)求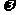 的值;(Ⅱ)求函数
的值;(Ⅱ)求函数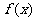 在区间
在区间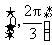 上的取值范围
上的取值范围
解:(Ⅰ)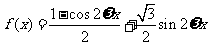
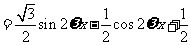
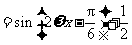 .
.
因为函数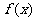 的最小正周期为
的最小正周期为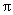 ,且
,且 ,所以
,所以 ,解得
,解得 .
.
(Ⅱ)由(Ⅰ)得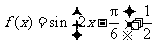 .因为
.因为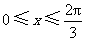 ,所以
,所以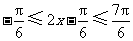 ,所以
,所以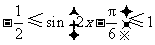 .因此
.因此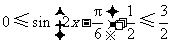 ,即
,即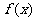 的取值范围为
的取值范围为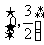 .
.
14.
设△ABC的内角A,B,C的对边分别为a,b,c.已知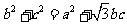 ,求:
,求:
(Ⅰ)A的大小;(Ⅱ)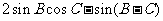 的值.
的值.
解:(Ⅰ) 
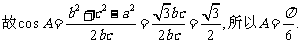
(Ⅱ) 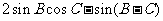

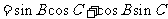
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com