
19.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 ( )
A. 烧杯中有铜无铁 B. 烧杯中有铁无铜
C. 烧杯中铁、铜都有 D. 烧杯中铁、铜都无
18.在稀硫酸酸化的H2O2溶液中,加入乙醚后液体分层,再加入少量K2Cr2O7溶液并振荡,在乙醚层中出现深蓝色,这是因为反应生成的CrO5溶于乙醚所致。CrO5的结构如右 ,上述反应的离子方程式为:Cr2O72- + 4H2O2
+ 2H+ == 2CrO5 + 5H2O 。对以上实验事实分析中正确的是( )
,上述反应的离子方程式为:Cr2O72- + 4H2O2
+ 2H+ == 2CrO5 + 5H2O 。对以上实验事实分析中正确的是( )
A.Cr2O72-被氧化为CrO5 B.化合物CrO5中Cr为+10价
C.该反应不属于氧化还原反应 D.该反应中转移电子数为8e-
17.下列实验过程中,始终无明显现象的是 ( )
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中
16.用高铁酸钠(Na2FeO4)对河湖水清毒是城市饮水处理的新技术。已知反应:
Fe2O3+3Na2O2 =2Na2FeO4+Na2O 下列说法正确的是 ( )
A.Na2O2既是氧化剂又是还原剂
B.Na2FeO4既是氧化产物又是还原产物
C.3 mol Na2O2发生反应,有12mol电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
15.下列叙述正确的是 ( )
A.直径介于1-100nm之间的微粒称为胶体
B.电泳现象可证明胶体属电解质溶液
C.利用丁达尔效应可以区别溶液与胶体
D.胶体粒子很小,可以透过半透膜
14.下列反应的离子方程式正确的是 ( )
A.用FeCl3溶液与铜反应制作印刷电路板:Cu+Fe3+===Cu2++Fe2+
B.碳酸氢镁溶液中加入过量石灰水:
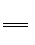 Mg2++2HCO3-+Ca2++2OH-====CaCO3↓+2H2O+MgCO3↓
Mg2++2HCO3-+Ca2++2OH-====CaCO3↓+2H2O+MgCO3↓
C.用惰性电极电解MgCl2溶液:2Cl-+2H2O 2OH-+Cl2↑+H2↑
D.在含有Mn2+的溶液中加入HNO3,再加入PbO2,则反应后溶液显紫红色:
5PbO2+2Mn2++4H+====5Pb2++2MnO4-+2H2O
13.钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应。其过程可以用如下化学方程式表示:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O=3 Na2FeO4+ NH3↑+7NaOH
③Na2FeO2+ Na2FeO4+2H2O=Fe3O4+4NaOH
下列说法正确的是 ( )
A.反应①不是氧化还原反应
B.该生产过程不产生任何污染
C.整个反应过程中,每有5.6gFe参加反应转移0.8mol电子
D.反应②中的氧化剂是NaNO2
12.用NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A. 0.1 mol·L-1稀硫酸100 mL中含有硫酸根个数为0.1. NA
B. 1 mol 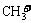 (碳正离子)中含有电子数为10 NA
(碳正离子)中含有电子数为10 NA
C. 2.4 g金属镁与足量的盐酸反应,转移电子数为 2 NA
D. 12.4 g白磷中含有磷原子数为0.4 NA
11.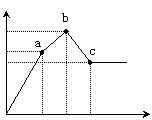 向100 mL 0.1
mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如右图所示。则下列说法中正确的是
( )
向100 mL 0.1
mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如右图所示。则下列说法中正确的是
( )
A.a点的溶液呈中性
B.b点发生反应的离子方程式是:
Al3++2SO42-+2Ba2++3OH- == Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.c点溶液呈碱性
10.在Al2(SO4)3、K2SO4和明矾的混和溶液中,如果c(SO42-)等于0.2mol/L,当加入等体积
的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原和物中K+的物质的浓度为( )
A.0.2mol/L B.0.25mol/L C.0.45mol/L D.0.225mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com