
2. 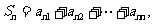 证明:
证明: 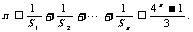 因为
因为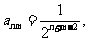 所以Sn是等比数列求和,但却不是等差比数列,也不是等差数列,直接求和变得不可能.观察需要证明的不等式,显然只要1££4n-1即可(数列{4n-1}的前n项和为).这类数列和式的不等式证明的关键是求和,特别是既不是等差、等比数列,也不是等差乘等比的数列求和,要利用不等式的放缩法,放缩为等比数列求和、错位相减法求和、裂项相销法求和,最终归结为有限项的数式大小比较.
所以Sn是等比数列求和,但却不是等差比数列,也不是等差数列,直接求和变得不可能.观察需要证明的不等式,显然只要1££4n-1即可(数列{4n-1}的前n项和为).这类数列和式的不等式证明的关键是求和,特别是既不是等差、等比数列,也不是等差乘等比的数列求和,要利用不等式的放缩法,放缩为等比数列求和、错位相减法求和、裂项相销法求和,最终归结为有限项的数式大小比较.
1. 在涉及指数运算的题目中,应用对数运算,十分重要,而解题过程中,一些近似运算又是十分必要的.
2、如图, 把正三角形ABC分成有限个全等的小正三角形, 且在每个小三角形的顶点上都放置一个非零实数, 使得任意两个相邻的小三角形组成的菱形的两组相对顶点上实数的乘积相等. 设点A为第一行,…, BC为第n行, 记点A上的数为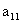 ,…, 第i行中第j个数为
,…, 第i行中第j个数为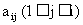 . 若
. 若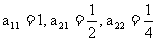 .
.
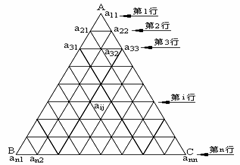 (1)求
(1)求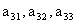 ;
;
(2)试归纳出第n行中第m个数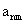 的表达式 (用含n , m的式子表示, 不必证明)
的表达式 (用含n , m的式子表示, 不必证明)
(3)记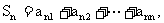 证明:
证明: 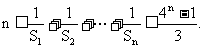




3已知数列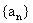 的前n项和为
的前n项和为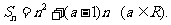

设集合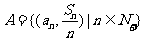 ,
,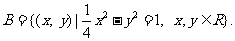

(1) 求数列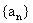 的通项公式;
的通项公式;
(2) 若以集合A中的元素作为点的坐标,则这些点是否都在同一条直线上? 并说明理由;
(3) “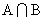 至多只有一个元素”是否正确? 如果正确, 请给予证明; 如果不正确, 请举例说明.
至多只有一个元素”是否正确? 如果正确, 请给予证明; 如果不正确, 请举例说明.


[方法点拨]
1. 某林场原有森林木材量为a,木材以每年的25%增长率生长,而每年冬天要砍伐的木材量为x,为了实现经过20年达到木材存有量至少翻两番的目标,则x的最大值是多少?(lg2=0.3)



5.已知等差数列{an}的前n项和为Sn,且S2=10,S5=55,则过点P(n,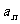 )和Q(n+2,
)和Q(n+2,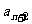 )(n∈N+)的直线的一个方向向量的坐标可以是 ( )
)(n∈N+)的直线的一个方向向量的坐标可以是 ( )
A.(2,) B.(-,-2) C.(-,-1)? D.(-1,-1) 

[例题探究]
4.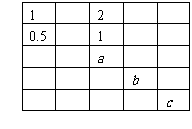 在如图的表格中,每格填上一个数字 后,使每一横行成等差数列,每一纵行成等比数列,则a+b+c的值为
( )
A.1
B.2 C.3 D.4
在如图的表格中,每格填上一个数字 后,使每一横行成等差数列,每一纵行成等比数列,则a+b+c的值为
( )
A.1
B.2 C.3 D.4
3.已知函数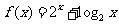 ,数列
,数列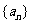 的通项公式是
的通项公式是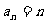 (
( ),当
),当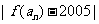 取得最小值时,
取得最小值时,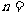

2. △ABC中,a、b、c分别为∠A、∠B、∠C的对边.如果a、b、c成等差数列,
∠B=30°,△ABC的面积为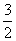 ,那么b= ( )(全国4文理)
,那么b= ( )(全国4文理)
A.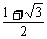 B.
B.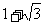 C.
C. D.
D.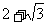

1.甲、乙两个工厂2004年元月份的产值相等,甲厂的产值逐月增加,并且每月增加的产值相同;乙厂的产值也逐月增加,且每月增加的百分率相同.已知2005年元月份两厂的产值又相等,则2004年7月份产值高的工厂是 ( )
A.甲厂 B.乙厂 C.产值相等 D.不能确定
2.电解精炼
电解时,以 作电解液, 作阴极, 作阳极
试题枚举
[例1] 在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2; ②Fe2O3; ③Na; ④Ca(NO3)2。铜粉可溶解的是( )
A.①② B.②④ C.②③ D.①④
解析: 加入Fe2O3反应生成Fe3+能氧化铜,加入Ca(NO3)2后等于铜和硝酸反应而消耗。
答案:B
[变式] 现有下列试剂:①食盐水 ②稀H2SO4 ③氯化铁 ④盐酸 ⑤NaOH溶液 ⑥硝酸银 ⑦硝酸钾,如将Cu转化为CuCl2,可采用的一组试剂是( )
A.④⑤⑥ B.③④⑤ C.①②③ D.④⑤⑦
[例2] 在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量浓度之比为:4:2:1,现加入适量的铁粉,使溶液中的三种离子的物质的量浓度之比为:1:3:9,则投入的铁粉与原溶液中Cu2+的物质的量之比为( )
A.5:4 B.4:5 C.3:5 D.5:6
解析: 溶液中还存在Fe3+,说明溶液中Cu2+没有反应,加入的铁全部反应,将粒子比例调整为:12:6:3和2:6:18,若溶液中由6molCu2+,就有10molFe3+发生反应,消耗5mol铁。
答案: D
[变式]将Cu片放入0.l mol / L FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+)∶c(Fe2+)=2∶3,则Cu2+与Fe3+的物质的量之比为
A.3∶2 B.3∶5 C.4∶3 D.3∶4
[例3] 如图,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一个大烧杯,请回答:
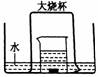 (1)铜与浓硝酸反应的化学方程式:_______________________;
(1)铜与浓硝酸反应的化学方程式:_______________________;
(2)实验中观察到的主要现象是:
①_______________________________ ;
②_______________________________ ;
③_______________________________ ;
④_______________________________ 。
(3)用该装置做铜与浓硝酸反应实验的优点:______________ ;
(4)大烧杯内最终所得气体产物的化学式: ;若要验证此气体产物,最简便的方法:_________________________________________ 。
解析:分析实验现象要从导致产生实验现象的物质开始分析,如从小烧杯发生的反应到产生气体颜色的变化,再到烧杯内液面高度的改变,逐一分析,才能做到全面分析。
答案:(1)Cu+4HNO3 ==Cu(NO3 )2 +2NO↑+2H2O
(2)①铜片表面产生气泡; ②小烧杯中溶液逐渐变成蓝色;③大烧杯中有红棕色气体生成,气体颜色又逐渐褪去;④大烧杯内液面上升,水槽中液面下降。
(3)体系封闭,无氮氧化合物逸出,不污染环境。
(4)NO;轻轻掀起倒扣的大烧杯,放入适量空气,若有红棕色气体生成,最终气体为NO。
[例4] Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu。现有浓硫酸、浓硝酸、稀硫酸、稀硝酸、FeCl3稀溶液及pH试纸,简述如何用简便的实验方法来检验CuO经氢气还原所得红色产物中是否含有碱性氧化物Cu2O。
解析:由题给信息可知,Cu2O是碱性氧化物,可溶于酸溶液:Cu2O+2H+=2Cu++H2O;而Cu+在酸溶液中不稳定,自身歧化成Cu2+和Cu。2Cu+=Cu2++Cu。题给试剂中,浓硫酸、浓硝酸、稀硝酸、FeCl3稀溶液均显酸性,且都能与Cu反应生成Cu2+,如果选用这些试剂,它们和样品反应后的溶液都呈蓝色(Cu2+),但分不清是与Cu还是与Cu2O反应产生的Cu2+,故无法确证样品中是否含有Cu2O。根据以上分析,选用的试剂必须符合两个条件,一是呈酸性,二是不能与Cu反应。在题给试剂中只有稀硫酸符合。
答案:取少量待检样品放入稀硫酸 ,振荡,若溶液变为蓝色,说明样品中有Cu2O,若溶液不变色,说明产物中无Cu2O。
[例5]孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:xCuCO3·yCu(OH)2(x、y为正整数且x≤2,y≤2)
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石消耗的盐酸的物质的量与生成的CO2的物质的量之比为4:1;石青则为3:1,请推算它们的化学组成。
孔雀石__________________________;石青__________________________;
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO2 3.36 L(标准状况下);加热另一份样品使其完全分解,得到CuO 20 g,试通过计算确定该混合物中孔雀石和石青的物质的量之比 。
解析: (1)设孔雀石的化学式为xCuCO3•yCu(OH)2
则依题意 = = 孔雀石的化学式为 CuCO3•Cu(OH)2
又设石青的化学式为 xCuCO3•yCu(OH)2
则依题意 = = 石青的化学式为 CuCO3•Cu(OH)2
(2)设该样品中孔雀石物质的量分数为x,则石青为 1- x
=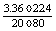 =
=
孔雀石与石青物质的量之比为1:1。
答案:(1)CuCO3•Cu(OH)2;CuCO3•Cu(OH)2 (2) 1:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com