
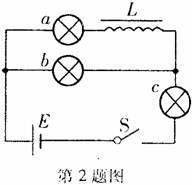
2.如图所示,a、b、c为三个完全相同的灯泡,L为自感线圈(自感系数较大,电阻不计),E为电源,S 为开关。闭合开关S,电路稳定后,三个灯泡均能发光。则
A.断开开关瞬间,c熄灭,稍后a、b同时熄灭
 B.断开开关瞬间,流过a的电流方向改变
B.断开开关瞬间,流过a的电流方向改变
C.闭合开关,a、b、c同时亮
D.闭合开关,a、b同时先亮,c后亮
1. 关于速度和加速度,下列说法小正确的是
关于速度和加速度,下列说法小正确的是
A.速度不变时,加速度可能改变
B.加速度增大时,速度可能减小
C.速度变化得越来越快时,加速度越来越小
D.速度方向改变时,速度的方向也一定改变
19.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容,请选择其中一题,并在相应的答题区域作答。若两题都做,则按A题评分。
A.(12分)已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2-离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。
 请回答下列问题:
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是 ▲ (填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是 ▲ 。
 ⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为 ▲ 。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为 ▲ 。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有 ▲ 。
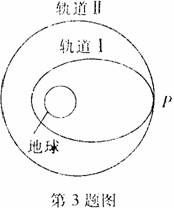
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为 ▲ ;该晶体的化学式为 ▲ 。
 B.(12分)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
B.(12分)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
步骤Ⅰ:称取0.4g花生油样品,置于两个干燥的碘瓶(如图)内,加入10mL四氯化碳,轻轻摇动使油全部溶解。向碘瓶中加入25.00mL含0.01mol IBr的无水乙酸溶液,盖好瓶塞,在玻璃塞与瓶口之间滴加数滴10%碘化钾溶液封闭缝隙,以免IBr的挥发损失。
步骤Ⅱ:在暗处放置30min,并不时轻轻摇动。30min后,小心地打开玻璃塞,用新配制的10%碘化钾10mL和蒸馏水50mL把玻璃塞和瓶颈上的液体冲洗入瓶内。
步骤Ⅲ:加入指示剂,用0.1mol·L-1硫代硫酸钠溶液滴定,用力振荡碘瓶,直至终点。
测定过程中发生的相关反应如下:
①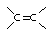 +IBr →
+IBr →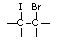
②IBr+KI=I2+KBr
③I2+2S2O32-=2I-+S4O62-
请回答下列问题:
⑴已知卤素互化物IBr的性质与卤素单质类似,实验中准确量取IBr溶液应用 ▲ ,用方程式表示碘瓶必须干燥的原因 ▲ 。
⑵步骤Ⅱ中碘瓶在暗处放置30min,并不时轻轻摇动的原因是 ▲ 。
⑶步骤Ⅲ中所加指示剂为 ▲ ,滴定终点的现象 ▲ 。
⑷反应结束后从液体混合物中回收四氯化碳,则所需操作有 ▲ 。
18.(10分)目前,聚氯乙烯塑料(PVC)占塑料消费量的30%以上,BICM法用乙烯、氯气等为原料合成PVC,其工艺流程如下。
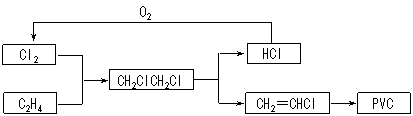

⑴一定条件下,HCl与O2反应制取Cl2的方法称为地康法,其热化学反应方程式为:
4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ΔH=-114.4kJ·mol-1。
2Cl2(g)+2H2O(g) ΔH=-114.4kJ·mol-1。
升高温度,该反应的化学平衡常数K会 ▲ 。
A.增大 B.减小 C.不变 D.无法确定
⑵一定温度下某体积可变的容器中充入4LHCl气体和6L空气(氧气占20%),充分反应后气体体积为9.2L。该反应中HCl气体的转化率为 ▲ 。
⑶假设BICM法中各步反应的转化率均为100%,计算生产1000吨PVC需要购得的氯气质量。
17.(14分)喹硫平可用于精神疾病的治疗,其结构为:
( )2·
)2·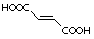 ,它的合成路线如下:
,它的合成路线如下:

已知:(Ⅰ)反应①为取代反应;(Ⅱ)A的系统命名为1,4-二溴―2―丁烯。
请回答下列问题:
⑴写出分子式为C13H9NO4S的物质的结构简式 ▲ 。
⑵物质 中除硫醚键(-S-)外,还含有的官能团名称为 ▲ 。
中除硫醚键(-S-)外,还含有的官能团名称为 ▲ 。
⑶反应③的类型是 ▲ 反应,反应⑤的目的是 ▲ 。
⑷写出反应④的化学方程式 ▲ 。
⑸物质B的同分异构体有多种,其中既含有羟基,又含有醛基的同分异构体有 ▲ 种。
⑹已知:-SH的性质与-OH相似。
物质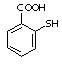 一定条件下形成聚合物的结构简式为 ▲ 。
一定条件下形成聚合物的结构简式为 ▲ 。
16.(10分)烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
⑴烟气脱硫、脱硝的环境意义是 ▲ 。
⑵选择性催化还原法的脱硝原理为:
6NOx+4x NH3  (3+2x)N2+6xH2O
(3+2x)N2+6xH2O
①上述反应中每转移3mol电子,生成标准状况下N2的体积为 ▲ L。
②已知:2H2(g)+O2(g) =2H2O (g) ΔH=-483.6 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH=-180.5kJ·mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH= ▲ 。
⑶目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。


图1 图2
①写出该脱硝原理总反应的化学方程式: ▲ 。
②为达到最佳脱硝效果,应采取的条件是 ▲ 。
15.(10分)下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变混浊,D、E均能使品红溶液褪色;I是一
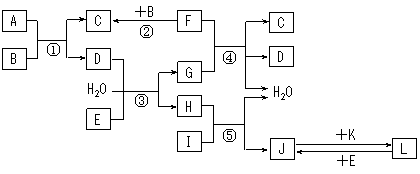 种红棕色固体氧化物。
种红棕色固体氧化物。
请回答下列问题:
⑴C的电子式为 ▲ 。
⑵检验溶液L中金属阳离子的方法是 ▲ 。
⑶反应③的离子方程式为 ▲ 。
⑷F与G的浓溶液反应的化学方程式为 ▲ 。
⑸气体A的密度为2.68g·L-1(标准状况),通过计算、推理,可确定A的分子式为 ▲ 。
14.(8分)某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。
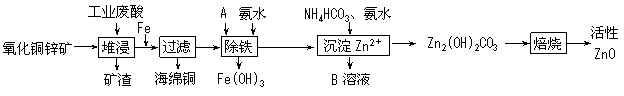

已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
|
离子 |
开始沉淀时的pH |
完全沉淀时的pH |
|
Fe2+ |
6.34 |
9.7 |
|
Fe3+ |
1.48 |
3.2 |
|
Zn2+ |
6.2 |
8.0 |
请回答下列问题:
⑴氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS) ▲ Ksp(ZnS)(选填“>”“<”或“=”)。
⑵物质A可使用下列物质中的 ▲ 。
A.KMnO4 B.O2 C.H2O2 D.Cl2
⑶除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 ▲ 范围之间。
⑷物质B可直接用作氮肥,则B的化学式是 ▲ 。
13.(14分)某化学研究性学习小组通过查阅资料,设计了如下图所示的方法来制备KMnO4。
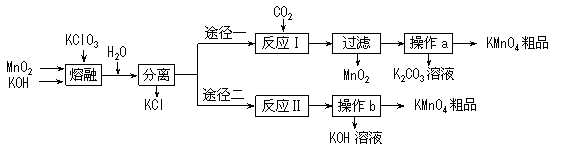
 已知:①3MnO2+KClO3+6KOH
已知:①3MnO2+KClO3+6KOH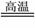 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
②几种物质的溶解度:
|
温度 |
溶解度/g |
||
|
K2CO3 |
KOH |
KMnO4 |
|
|
20℃ |
111 |
112 |
6.38 |
|
60℃ |
127 |
154 |
22.1 |
请回答下列问题:
⑴第一步固体熔融时除三脚架、泥三角、细铁棒、坩埚钳外,还需下列仪器中的 ▲ 。
A.蒸发皿 B.烧杯 C.酒精灯 D.铁坩埚
 ⑵反应Ⅰ中氧化产物与还原产物的物质的量之比为 ▲ ;该反应中可以循环利用的产物是 ▲ 。
⑵反应Ⅰ中氧化产物与还原产物的物质的量之比为 ▲ ;该反应中可以循环利用的产物是 ▲ 。
⑶反应Ⅱ的条件为电解,写出反应Ⅱ的化学方程式 ▲ 。
⑷途径一、二中的操作a、b相同,均包括 ▲ 、过滤等3步。
⑸通过用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①实验时要将草酸晶体(H2C2O4·2H2O)配成标准溶液,则配制100mL1.5mol·L-1的草酸溶液,需要称取草酸晶体的质量为 ▲ 。
②该实验中除草酸晶体的质量外,还需要采集的数据有 ▲ 。
12.下列溶液中微粒的物质的量浓度关系正确的是
A.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4的溶液中,c(NH4+)大小:①=②>③
B.将物质的量相等的KHC2O4和H2C2O4溶于水配成溶液:2c(K+)=c(HC2O4-)+
c(H2C2O4)
C.0.1mol·L-1 K2HPO4和0.2mol/L KH2PO4的混合溶液:c(K+)+c(H+)=c(H2PO4-)+2c(HPO42-)+3c(PO43-)+c(OH-)
D.0.1mol·L-1 CH3COONa与0.15mol·L-1 HCl等体积混合:c(Cl-)>c(H+)>c(Na+)>c(CH3COO-)>c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com