
3. 已知集合A=B=R,x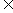 A,y
A,y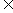 B, f:x→ax+b,若4和10的象分别为6和9,则19在f作用下的象为( )
B, f:x→ax+b,若4和10的象分别为6和9,则19在f作用下的象为( )
A. 18 B. 30 C.
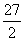 D.
28
D.
28
2、下列哪组中的两个函数是同一函数( )
(A)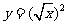 与
与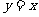 (B)
(B)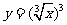 与
与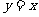
(C)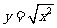 与
与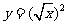 (D)
(D)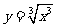 与
与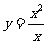
1.若集合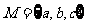 中的元素是△
中的元素是△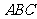 的三边长,则△
的三边长,则△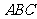 一定不是( )
一定不是( )
A.锐角三角形 B.直角三角形 C.钝角三角形 D.等腰三角形
22、四、计算题(8分)
标准状况下,H2和CO的混合气体共8.96L,测得其质量为6.0g,试计算此混合气体中H2和CO的质量和体积各为多少?
21、 (10分)右图为实验室某浓盐酸试剂瓶标签上的有关数据,
(10分)右图为实验室某浓盐酸试剂瓶标签上的有关数据,
试根据标签上的有关数据回答下列问题:
⑴该浓盐酸中HCL的物质的量浓度为_________mol·L-1 。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体
积的多少而变化的是_________ 。(有1~2个答案)
A、溶液中HCL的物质的量 B、溶液的浓度
C、溶液中CL-的数目 D、溶液的密度
⑶某学生欲用上述浓盐酸和蒸馏水配制500 ml 物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取 ml 上述浓盐酸进行配制。
 ②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
I、用量筒量取浓盐酸进俯视观察凹液面( )
II、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水( )
20、(9分)现有含NaCL、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现CL-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
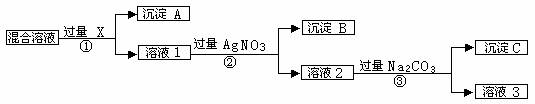
请回答下列问题:
⑴写出实验中下列物质的化学式:试剂X :_______,沉淀A:_______,沉淀B:______。
⑵上述实验流程中加入过量的Na2CO3的目的是___________________________________。
⑶按此实验方案得到的溶液3中肯定含有___________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________ ,之后若要获得固体NaNO3需进行的实验操作是________________(填操作名称)。
19、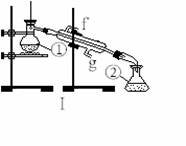
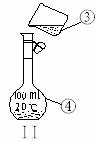 (11分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
(11分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称:
①____________;②;____________
④____________;
⑵仪器①-④中,使用时必须检查是
否漏水的有 。(填序号)

⑶若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有________________,将仪器补充完整后进行的实验操作的名称为;_________________ 。现需配制250 ml 0.2 mol/L NaCL溶液,装置II是某同学转移溶液的示意图,图中的错误是__________________
__________________________________________________________________(指出两处)。
18、(8分)欲除去硝酸钾固体中混有的少量氯化钾杂质,某学生进行如下实验操作。回答下列问题:
⑴溶解样品。该过程所需的仪器有_______________________________________________。
⑵向溶解后的溶液中加入适量的 ____________ (填化学式)溶液,使氯化钾转化为沉淀。
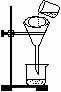 ⑶将混合液进行过滤,过滤装置和操作如图所示,
⑶将混合液进行过滤,过滤装置和操作如图所示,
指出图中的两处错误:
① _____________________________________ ;
② _____________________________________ 。
17、(6分)⑴某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+的物质的量浓度为____________________。(提示:1g=1000mg)
⑵在KCL和CaCL2所组成的某混合物中,K+与Ca2+的物质的量之比为2:1,则KCL与CaCL2的物质的量之比为____________,该混合物中的CaCL2的质量分数为___________。
16、等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应。若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为( )
A、1:2:3 B、1:6:9 C、1:3:3 D、1:3:6
第II卷(非选择题 共52分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com