
16.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为
KOH溶液,其充、放电按下式进行:
.. Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
.. 有关该电池的说法正确的是( )
A.充电时阳极反应:Ni(OH)2 -e- + OH- == NiOOH + H2O
B.电池充电时,电池正极和电源的负极连接。
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
15.某温度下,某容积恒定的密闭容器中发生如下可逆反应:
CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g) H>0当反应达平衡时,测得容器中各物质均 为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可采用的是(
)
H>0当反应达平衡时,测得容器中各物质均 为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可采用的是(
)
A、升温 B、加催化剂
C、再加入n molCO和n molH2O D、再加入2n molCO2和2n molH2
13.高温下,某反应达到平衡,平衡常数K= 。恒容时,温度升高,H2浓 度变大。下列说法正确的是( )
。恒容时,温度升高,H2浓 度变大。下列说法正确的是( )
A.该反应是焓变为负值
B.恒温下,增大压强,H2浓度一定减小
 C.升高温度,逆反应速率减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为CO+H2O CO2+H2


|
为ρ g/cm3)。下列叙述错误的是( )
A.t1时刻锌镀层已完全反应
B.锌镀层的厚度为
C.反应放热也是影响OA段的反应速率的因素之一
D.有原电池反应发生,负极的电极反应式为Zn- 2e → Zn2+
12.常温下,有甲、乙两份体积均为1 L、浓度均为0.1 mol/L的氨水,其pH为11。①甲 用蒸馏水稀释100倍后,溶液的pH变为a;②乙与等体积、浓度为0.2 mol/L的盐酸 混合,在混合溶液中:n(NH4+ )+n(H+)-n(OH-) = b mol。则a、b正确的答案组合是 A.9-11之间;0.1 B.9-11之间;0.2 ( )
C.12-13之间;0.2 D.13;0.1
11.在二氧化碳的水溶液中存在着如下平衡:
C02(g)  C02(aq)
C02(aq)+H20
C02(aq)
C02(aq)+H20 H2C03(aq)
H2C03(aq)
H2C03(aq)
 H+ (aq)+HCO3-(aq)
HCO3-(aq)
H+ (aq)+HCO3-(aq)
HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
下列有关说法正确的是( )
A.水中溶解的二氧化碳的浓度,夏天时比冬天时高
B.如果海水略呈碱性,海水中二氧化碳的浓度比纯水高
C.气压升高,水中c(HCO3-)增大
D.常温下,二氧化碳的水溶液中,由水电离出的c(H+)与c(OH-)的乘积等于1×lO-14
10.将炭粉和铁粉均匀混合,撒入内壁分别用氯化钠溶液和稀醋酸溶液润湿过的具支试管 中,并按下图装置好仪器,观察下图,示意正确的是( )
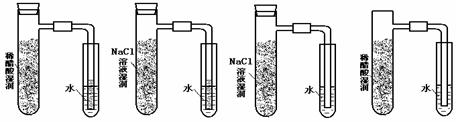
A B C D
9.下列化学反应的离子方程式正确的是( )
A.在稀氨水中通入过量CO2:NH3·H2O+CO2=NH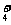 +HCO
+HCO
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3 +2HClO
+2HClO
C.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S
D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO =CaSO4
=CaSO4 +H2O
+H2O
8.下列实验操作正确的是( )
A.减压过滤完毕,先关闭水龙头,后拆下连接抽气泵和吸滤瓶的橡皮管,防止倒吸
B.萃取与分液的操作中,将上层液体从分液漏斗下口放出
C.滴加H2SO4、KI、淀粉溶液,鉴别NaNO2和NaCl
D.向AgNO3溶液中依次滴加同浓度的Na2S、KI、NaCl溶液,实现沉淀的转化
7.下列说法或表示方法正确的是( )
A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由“C(石墨)→C(金刚石) ΔH=+1.9KJ/mol”可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ·mol-1,若将含0.5molH2SO4 的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3KJ
D.在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方 程式表示:2H2(g)+O2(g)=2H20(l)ΔH=+285.8KJ/mol
6.在溶液中有浓度均为0.0lmol/L的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:

当氢氧化物开始沉淀时,下列哪一种离子所需的pH最小( )
A.Fe3+ B.Cr3+ C.Zn2+ D.Mg2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com