
13.试回答下列各问题:
(1)指出下面物质分子或离子的空间构型:
PO43-___________________;CS2_______________;
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
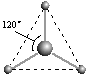 __________________;
__________________;
 __________________。
__________________。
(3)按要求写出第二周期非金属元素构成的中性分子的化学式:
平面形分子_________,三角锥形分子_________,四面体形分子__________。
(4) 1919年美国化学家埃文·朗缪尔(Langmuir)提出:价电子(最外层电子)数和重原子(即比氢重的原子)数相同的分子(或离子)互称为等电子体。由第一、二周期元素组成,与F2互为等电子体的分子有 ____、 (写两种)离子有_______。(写一种)。
(5)下列一组微粒中键角由大到小顺序排列为____________________(用编号填写)。
①HCN ②SiF4 ③SCl2 ④CO32- ⑤H3O+
12.下面我们一起来认识一些硼的化合物:
(1)2008 年北京奥运会主体育场的外形好似“鸟巢” (The Bird Nest )。有一类硼烷也好似鸟巢,故称为巢式硼烷。巢式硼烷除 B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化。下图是三种最简单的巢式硼烷,

这类硼烷的通式可表示为________________。
(2)硼酸是一元酸,它在水中的电离方程式可表示为H3BO3+H2O H++B(OH)4-,H3BO3分子和B(OH)4-离子中硼原子的杂化类型分别是_______、_________。
H++B(OH)4-,H3BO3分子和B(OH)4-离子中硼原子的杂化类型分别是_______、_________。
(3)一种硼镁超导物质的晶体结构单元如右图所示:
 ①试写出这种超导材料的化学式
。
①试写出这种超导材料的化学式
。
②完成并配平下列化学反应方程式。
+ HCl- B4H10+ B+ H2+
③写出B4H10在空气中燃烧的化学方程式 。
11.试用有关知识解释下列原因:(1)有机物大多难溶于水,为什么乙醇和乙酸可与水互溶?_______________
_______________________________________________。
(2)乙醚(C2H5OC2H5)的相对分子质量远大于乙醇,为什么乙醇的沸点比乙醚高得多?_____________________
_______________________________________________。
(3)从氨合成塔里分离H2、N2、NH3的混合物,采用什么方法?_________________;为什么用这种方法?____
_______________________________________________。
(4)水在常温情况下,其组成的化学式可用(H2O)m表示,为什么?______________________________________。
10.往浓CuSO4溶液中加入过量较浓的NH3·H2O直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液。小心加入约和溶液等体积的C2H5OH并使之分成两层,静置。经过一段时间后可观察到在两层“交界处”下部析出深蓝色Cu(NH3)4SO4·H2O晶体,最后晶体析出在容器的底部。请回答:
(1)为什么要加C2H5OH?__________________________
_______________________________________________。
(2)小心慢加和快速加C2H5OH(快加不易形成分层),请估计实验现象有何不同?_________________________。
(3)如将深蓝色溶液加热,可能得到什么结果?________
_______________________________________________。
9.如下图,左图表示白磷(P4)的分子结构,中图表示三氧化二磷(P4O6)的分子结构,右图表示五氧化二磷(P4O10)的分子结构,下列说法中错误的是


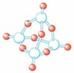
P4 P4O6 P4O10
A.P4O6中的磷原子采用sp2方式杂化
B.三氧化二磷、五氧化二磷这两个名称都只表示原子个数比,不表示分子的实际组成
C.P4、P4O6和P4O10分子中同一P原子上两个化学键之间的夹角都是60°
D.P4O6分子中4个P原子构成正四面体,6个O原子构成正八面体
8.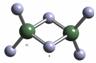 科技日报2007年1月30日讯 美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关说法肯定不正确的是
科技日报2007年1月30日讯 美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关说法肯定不正确的是
A.Al2H6中H为+1价,Al为-3价
B.Al2H6在空气中完全燃烧,产物为氧化铝和水
C.Al2H6分子是非极性分子
D.氢铝化合物可能成为是未来的储氢材料和火箭燃料
7.近年来研制的NF3气体可运用于氟化氢--氟化氚高能化学激光器中的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2=NF3+3NH4F。 下列说法不正确的是
A.NF3的形成过程用电子式可表示为

B.NF3的氧化性大于F2
C.NF3分子空间构型为三角锥形
D.NH4F中既有离子键又有极性共价键
6. 磷酸的结构式如右图所示 ,磷酸分子与磷酸分子的羟基之间可以脱去水。三个磷酸分子可以脱去两个水分子生成三聚磷酸。含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式
磷酸的结构式如右图所示 ,磷酸分子与磷酸分子的羟基之间可以脱去水。三个磷酸分子可以脱去两个水分子生成三聚磷酸。含磷洗衣粉中含有三聚磷酸的钠盐(正盐),则该钠盐的化学式
及1mol此钠盐中P-O单键的物质的量分别是:
A.Na5P3O12 12mol B.Na3H2P3O10 9mol
C.Na5P3O10 9mol D.Na2H3P3O10 12mol
5.氯的含氧酸根离子有ClO-、ClO2-、ClO3-、ClO4-等,有关它们的下列说法正确的是:
A.ClO-中氯元素显+1价,具有氧化性
B.这些离子结合H+的能力,ClO4-最强
C.这些离子加到AgNO3溶液中都会产生沉淀
D.ClO4-是SO42-的等电子体,其空间构型为正四面体
4.以下各分子中,所有原子都满足最外层为8电子结构的是
A.H3O+ B.BF3 C.P4 D.PCl5
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com