
9. X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀H2SO4中时,X溶解,Z极上有H2放出。若电解Y2+和Z2+离子共存的溶液时,Y先析出。又知M2+离子的氧化性强于Y2+离子,则这四种金属的活动性由强到弱的顺序为
( )
A.X > Z > Y > M B.X > Y > Z > M
C.M > Z > X >Y D.X > Z > M > Y
(本题考查学生判断金属的活泼性,是一道结合了原电池、电解、氧化还原知识的综合题)
8.白铁皮发生析氢腐蚀,若有0.2摩电子发生转移,下列说法中不正确的是 (B) A.有6.5克锌被腐蚀 B.2.8克铁被腐蚀 C.正极上H+被还原 D.在标准状况下有2.24升气体放出
(本题考查了析氢腐蚀时发生的电极反应)
7.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:2Ag+Zn(OH)2 Ag2O+Zn+H2O,在此电池放电时,负极上发生反应的物质是 ( )
Ag2O+Zn+H2O,在此电池放电时,负极上发生反应的物质是 ( )
A.Ag B.Zn(OH)2 C.Ag2O D.Zn
(本题考查原电池中电极反应物的判断)
6.按下列图示装置,用导线将电极连接起来放置一段时间后,溶液的pH值下降的是 ( )

(考查学生原电池、电解池中电解质溶液发生的变化)
5.下列各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是: ( )
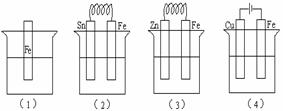
A.(4)>(2)>(1)>(3) B.(2)>(1)>(3)>(4)
C.(4)>(2)>(3)>(1) D.(3)>(2)>(4)>(1)
(本题考查学生金属腐蚀的快慢的判断方法)
4.把a、b、c、d四块金属板浸入稀H2SO4中,用导线两两相连,可以形成原电池。若a、b相连时,a为负极;c、d相连时,c为负极;a、c相连时,c极上产生大量气泡,b、d相连时,b极上有大量气泡。则四块金属的活动顺序是:
( )
A.a>c>d>b B.c>a>b>d
C. a>c>b>d D.c>a>d>b
(本题考查学生应用原电池原理判断金属的活动性的能力)
3.等质量的两份锌粉a、b,分别加入过量的稀H2SO4,同时向a中加入少量的CuSO4溶液,下列图表示产生H2的体积(V)与时间(t)的关系,其中正确的是:( )

(本题考查原电池的形成可加快化学反应)
2.下列关于实验现象的描述不正确的是( )
A. 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B. 用铜板做电极电解硫酸铜溶液,阴极铜板质量增加
C. 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D. 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快。
(考查学生运用原电池原理和电解原理判断电极和溶液中的变化)
1.下列说法正确的是( )
A.原电池是把电能转化为化学能的装置
B.原电池中电子流出的一极是正极发生氧化反应
C.原电池的两极发生的反应均为氧化还原反应
D.形成原电池后,原电池中的阳离子向正极移动
(本题考查学生掌握原电池的原理、定义情况)
4.下图各容器中盛海水,铁会在其中发生变化。按铁极腐蚀的速度由快至慢的顺序为

(本题考查学生对金属腐蚀的快慢的判断能力)
新活题网站
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com