
1、D 2、C 3、D 4、A 5、B 6、D 7、D 8、B 9、A
4. DBACE
新活题网站
3.(1)D (2) 因原电池反应,铜将在银棒(正极)上析出而不是在铁棒上,所以应该是银棒下沉铁棒上升.
讲析:错误的认识是:铜离子与铁发生置换反应,铁棒增重向下沉.实际上应该考虑原电池反应,铜将在银棒上析出而不是在铁棒上,所以应该是银棒下沉铁棒上升.
2.CD 讲析:首先是区别出充电运用的是电解原理,放电则是运用了原电池原理。抓住电解池、原电池各极发生氧化还原反应的特点,结合题给的信息进行分析判断:
A:原电池负极反应式为: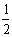 H2+OH-+e-
H2+OH-+e- Ni(OH)2,pH下降。故A不正确。
Ni(OH)2,pH下降。故A不正确。
B:原电池,NiO(OH)→Ni(OH)2,镍被还原。故B也不正确。同理可判断得:正确答案为CD。
1.Al-3e-=Al3+;Ag2S+2e-=2Ag+S2-;
3Ag2S+2Al+6H2O=6Ag+2Al(OH)3↓+3H2S↑。 讲析:要善于抓住题示信息,“黑色褪去而银不会损失”,必然发生变化:Ag2S→Ag,显然这是原电池的正极反应,Ag2S+2e-=2Ag+S2-,负极反应为活泼金属发生氧化反应:Al-3e-=Al3+。正极生成的S2-和负极生成的Al3+在溶液中发生双水解:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑,与题意产生臭鸡蛋气味的气体相吻合。原电池的总反应为上述三个反应的加合:3Ag2S+2Al+6H2O=6Ag+2Al(OH)3↓+3H2S↑。
16.在两烧杯中盛有甲、乙两种不同的稀溶液,用铁丝做电化腐蚀实验,实验进行
 一段时间后,A试管中液面高于烧杯中液面,B试管中液面低于烧杯中液面,试比较甲、乙溶液的pH值,并分别写出铁丝发生腐蚀时的电极反应式。
一段时间后,A试管中液面高于烧杯中液面,B试管中液面低于烧杯中液面,试比较甲、乙溶液的pH值,并分别写出铁丝发生腐蚀时的电极反应式。
15.常用干电池是用锌板围成的圆筒作正极,内充糊状的ZnCl2和NH4Cl。工作时某一阳离子在正极放电产生两种气体,一种气体分子可被MnO2氧化,另一种气体分子有孤对电子。试写出干电池工作时的电极反应,注明反应类型:
负极
反应类型 ;
正极
反应类型 。
14.为了判断电源A、B两极中哪一个是正极,某学生取滤纸一条,用硫酸钠、酚酞溶液湿润,然后从A、B两极中引出两根导线,并把两导线端分别压在滤纸两侧,通电后在滤纸上靠近A极所连导线的一侧呈现红色,试判断哪一极是正极?简述理由。
13. 有A、B、C、D、E、F、G七种金属,可能是钾、银、铁、铜、铂、锡、锌,现进行下列实验: (1)F不能跟热的硝酸反应 (2)将D和E接触后,在潮湿的空气中E容易生锈 (3)这七种金属中,在常温下只有A能跟水反应,D、E、G能跟稀硫酸反应放出氢气 (4)用铂作电极,电解相同物质量浓度B和C的硝酸盐混和溶液时,是C先析出 (5)在D表面涂上G,当表面破损接触电解质溶液时,D发生腐蚀 根据以上实验事实,推测各是何种物质。(填名称)
A、 B、 C、 D、
E、 F、 G、
12.炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。试回答:
(1)铁锅的锈蚀应属于______________,腐蚀的原因是___________________。
(2)铁锅锈蚀的电极反应式为:负极_________,正极________。正负电极反应产物会继续发生反应,反应的离子方程式或化学方程式为
____________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com