
7.(江苏省口岸中学2009届高三年级第二次月考化学试题)25℃时,某硫酸铜溶液的质量分数为w,物质的量浓度为cmol/L,密度为ρg/mL,将此溶液蒸去a g水或再向原溶液中加入b g无水硫酸铜粉末,充分静置并恢复至25℃时,均恰好全部转化为CuSO4·5H2O晶体。则下列关系式正确的是
A.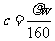 B.
B.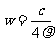 C.
C. D.
D.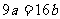
[解析]若100g溶液,溶液体积为100g/ρg.ml-1=1/10ρL,溶质的物质的量为100ω/160moL,则C=(100ω/160)moL÷(1/10ρ)L=1000ρω/160 ,AB错;
设溶液质量为x,当蒸发ag水后获得晶体,则[x(1-ω)-a]/Xω=90/160,当加入bg无水硫酸铜时获得晶体,则x(1-ω)/( Xω+b)= 90/160,联立两式得16a=9b,C正确,D错误.
[答案]C
[考点分析]本题考查溶液溶解度的计算,通过溶解度将几个常见物理量联系起来。
6.(2008-2009学年度启东市汇龙中学第一次月考)阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
⑴0.25molNa2O2中含有的阴离子数为0.5×6.02×1023
⑵7.5gSiO2晶体中含有的硅氧键数为0.5×6.02×1023
⑶2.24LCH4中含有的原子数为0.5×6.02×1023
⑷250mL2mol/L的氨水中含有NH3·H2O的分子数为0.5×6.02×1023
⑸1L 1mol·L―1的HAc溶液中含有6.02×1023个氢离子
⑹18g D2O(重水)完全电解,转移6.02×1023个电子
⑺22.4L SO2气体,所含氧原子数为2×6.02×1023
⑻14g乙烯和丙烯的混合物中,含有共用电子对数目为3×6.02×1023
A.2个 B.3个 C.5个 D.6个
[解析]⑴错,因为0.25molNa2O2中含有的阴离子0.25moL; ⑵正确,n(SiO2)=7.5/60
mol=0.125mol,每摩尔SiO2含有共价键是(1×4+2×2)/2 moL=4mol, 7.5gSiO2晶体中含有的硅氧键数为0.125×4×6.02×1023=0.5×6.02×1023
; ⑶错,不知道气体的存在的条件,无法计算;⑷错,因为氨水中存在这如下平衡NH3 + H2O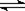 NH3·H2O
NH3·H2O 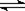 NH4++
NH4++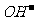 ; ⑸错,因为Hac是弱电解质。⑹错,18g D2O的物质的量小于1mol,⑺错,因为不知道气体的存在条件;⑻正确,因为乙烯与丙烯的最简式都是CH2,1.4g乙烯与丙烯的混合物中相当于含有0.1molCH2。
; ⑸错,因为Hac是弱电解质。⑹错,18g D2O的物质的量小于1mol,⑺错,因为不知道气体的存在条件;⑻正确,因为乙烯与丙烯的最简式都是CH2,1.4g乙烯与丙烯的混合物中相当于含有0.1molCH2。
[答案]A
[考点分析]以阿伏伽德罗常数的计算为背景考查:学生对物质组成的认识、晶体中共价键的数目、气体摩尔体积的应用、溶液中微粒数、转移的电子数、混合气体中共用电子对的数目21世纪教育网
5. (2008镇江期初)在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3, 下列对这四种气体的关系从大到小表达正确的是 ( )
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abc B.bcd C.acd D.abcd
[解析]比较a、c、d时先将不同的物理量转化为物质的量再进行比较,密度直接根据同温同压下,密度之比等于气体的式量之比,直接根据式量判断即可。
[答案]D
[考点分析]本题以物质的量为载体,考查物质的量与其他几个物理量之间的关系,同时考查学生对阿伏伽德罗定律及其推论的应用能力21世纪教育网
4.(2009浙江卷8).用NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5 NA
B.1 mol乙烷分子含有8 NA个共价键
C.58.5 g氯化钠固体中含有NA个氯化钠分子
D.在1 L 0.1 mol/L碳酸钠溶液中阴离总数大于0.1 NA
[解析]考察阿伏加德罗常数。A中NO和O2会反应生成NO2;B中乙烷共价键有7NA;
C中氯化钠含2NA个离子;D中碳酸钠因水解而使阴离子增加。
[答案]D
[考点分析]以阿伏伽德罗常数的计算为背景考查:气体摩尔体积的应用、物质中的共价键数、判断晶体类型以及水解反应对溶液中微粒数的影响。
3.(2009全国Ⅰ卷7)将15 mL 2 mol·L-1 Na2CO3溶液逐滴加入到40 mL 0.5 mol·L-1 MCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是
A.4 B.3 C.2 D.1
[解析]M的化合价为+n,Na2CO3与MCln反应对应的关系式为:2Mn+ ~ nCO32 -
2 n
15×10-3×2 40×10-3×0.5
可得n=3,故选B。
[答案]B
[考点分析]本题以溶液中的离子反应为背景,考查学生物质的量应用于化学方程式的能力。
2.(2009广东卷6)设nA 代表阿伏加德罗常数(NA )的数值,下列说法正确的是
A. 1 mol 硫酸钾中阴离子所带电荷数为nA
B. 乙烯和环丙烷(C3H6 )组成的28g混合气体中含有3nA 个氢原子
C. 标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为nA
D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1nA Fe3+
[解析]K2SO4中阴离子为硫酸根,1mol硫酸根所带电荷为2mol,A错误。乙烯和C3H6的最简式相同均为CH2,28g混合气有2molCH2,所以含4molH原子,B错误。Fe3+在溶液中发生水解,0.1molFeCl3溶液中,Fe3+的物质的量要小于0.1mol,D错误21世纪教育网
[答案]C
[考点分析]以阿伏伽德罗常数的计算为背景考查:溶液中的电荷、混合物中原子数、气体摩尔体积的应用以及水解反应对溶液中微粒数的影响。
该部分知识点主要体现在阿伏伽德罗常数的计算上,也涉及阿伏伽德罗定律及其推论。其他如一定物质的量浓度的计算、物质的量应用于化学方程式的计算往往穿插于大题之中,复习时要引起重视。
[典例精析]
1.(2009江苏高考化学)用NA表示阿伏伽德罗常数的值。下列叙述正确的是:
A.25℃时,pH=13的1.0LBa(OH)2溶液中含有的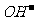 数目为0.2NA
数目为0.2NA
B.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,22.4L甲醇中含有的氧原子数为1.0NA
[解析]pH=13,则c(OH-)=0.1mol·L-1,n(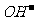 )=0.1mol,则N(OH-)=0.1NA,A错误;Cl2与NaOH 反应时,每摩Cl2转移1mol电子,所以2.24LCl2应转移0.1mol,B错误;
)=0.1mol,则N(OH-)=0.1NA,A错误;Cl2与NaOH 反应时,每摩Cl2转移1mol电子,所以2.24LCl2应转移0.1mol,B错误;
标况下,22.4L甲醇的物质的量远大于1mol,所以D错误;
[答案]C21世纪教育网
[考点分析]以阿伏伽德罗常数的计算为背景考查:溶液中微粒数、氧化还原反应中转移的电子数、混合物中原子数、以及气体摩尔体积的应用21世纪教育网
关于阿伏加德罗常数的高考试题,常常有意设置一些极易疏忽的干扰因素。在分析解答这类题目时,要特别注意下列细微的知识点:①状态问题,如水在标准状况时为液态或固态;SO3在标准状况下为固态、常温常压下为液态,戊烷及碳原子数更多的烃,在标准状况下为液态或固态。②特殊物质的摩尔质量,如D2O、T2O、18 O2 等。③某些物质分子中的原子个数,如Ne、O3、白磷等。④一些物质中的化学键数目,如SiO2、Si、CH4、P4、CO2等。⑤较复杂的化学反应中,转移电子数的求算,如Na2O2+H2O,C12+NaOH、电解AgNO3溶液等。⑥要用到22.4 L/mol时,必须注意气体是否处于标准状况。⑦某些离子或原子团在水溶液中能发生水解反应,使其数目减少。⑧注意常见的一些可逆反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com