
3.下列有关分子和原子的说法正确的是( )
A分子或原子都可以构成物质 B.分子的体积比原子体积大
C.分子可以再分而原子不能再分 D分子是保持物质性质的最小粒子
中考链接
例1:下列有关受热蒸发的说法正确的是( )
A水发生了化学变化 B.水分子运动速率增大
C.水变成了氢气和氧气 D水分子分裂成氢原子和氧原子
本题考查利用分子的知识解释某些自然现象,有利于提高学生运用所学知识解决实际
问题的能力。水受热蒸发是物理变化,水分子本身没有变化,只是运动速率和分子问隔都变大了。所以答案是B。
练习1:“酒香不怕巷子深”这一现象说明了( )
 A.分子体积很大 B.分子分裂了 C.分子在不断运动 D.分子质量很大
A.分子体积很大 B.分子分裂了 C.分子在不断运动 D.分子质量很大
 例2:图3-2-3中,表示氧原子,表示氢原子。
例2:图3-2-3中,表示氧原子,表示氢原子。

(1)根据此图,试分别从物质构成、分子构成的角度各说出一种观点:
a. .
b. .
(2)根据此图,说明化学反应的本质: .
本题考查分子与原子的联系,化学变化实质。解题时应根据图中信息分析所要解答的问题。可看出:氧气、氢气、水都是由分子构成的,而它们的分子是由原子构成的;在氧分子与氢分子反应生成水分子这一化学反应过程中,氧分子分裂成的氧原子和氢分子分裂成的氢原子重新组合构成了水分子。
答案:(1)分子是构成物质的一种粒子;分子由原子构成
 (2)构成反应物的分子分裂为原子原子再重新组合构成新分子
(2)构成反应物的分子分裂为原子原子再重新组合构成新分子
练习2:为了探究水电解的微观过程,某同学做了一些分子、原子的模型,若用
 表示氢原子,用表示氧原子,其中能保持氢气化学性质的粒子模型是( )
表示氢原子,用表示氧原子,其中能保持氢气化学性质的粒子模型是( )
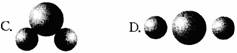

例3:对于Mg2+和Mg两种粒子比较,下列说法不正确的是( )
A.它们的电子数相同 B它们的化学性质相同
C.它们的质子数相同 D.它们都是构成物质的粒子
本题考查原子与离子的区别和联系。Mg2+是由Mg失去2个电子形成的,在这一转化过程中。核外电子数改变,但质子数没有改变,化学性质不再相同。所以答案是AB。
练习3:下列结构示意图中,表示阳离子的是( )

1.1999年度诺贝尔奖获得者艾哈迈德·泽维尔,开创了“飞秒”化学的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为该技术不能观察到的是( )
A化学变化中反应物分子的分离 B.反应中原子的运动
C.化学变化中生成物分子的形成 D.原子核的内部结构
3.M原子得到2个电子变成离子,则该离子的符号可能是( )

知识点4 分子、原子、离子间的转化:
分子、原子、离子间的转化:
练习题组4
2.下列物质是由离子构成的是( )
A.氢氧化铜 B磷 C.氦气 D.铁
1.构成氯化钠的粒子是( )
A氯化钠分子 B氯原子和钠原子C.钠离子和氯离子 D.氯化钠的离子
4.据中央电视台2001年6月3日对抚仙湖底古城考古的现场报道,科学家曾通过测定古生物遗骸中的碳一14含量来推断古城年代。碳一14原子的核电荷数为6,相对原子质量为14。下列关于碳一14原子的说法中,错误的是( )
A.中子数为6 B.质子数为6 C.电子数为6 D.质子数和中子数之和为14
知识点3 离子
(1)带电的原子或原子团叫离子。
(2)离子所带电荷有正、负之分,带正电荷的离子叫阳离子;带负电荷的离子叫阴离子。
(3)表示方法:电荷的正、负分别用“+”“一”表示,电荷个数写在“十”“一”的前面,把离子所带电荷的个数和种类标在元素(或原子团)符号的右上角,如镁离子(Mg2+)、硫酸根离子(SO42-)。当离子所带的电荷个数为1时,省略数字1,如钠离子(Na+),氯离子(Cl一)。
温馨提示:一种离子不能直接构成物质,只有带异种电荷的不同离子才能共同构成物质。
练习题组3
3.下列关于原子的论述正确的是( )
A.原子比分子小 B原子是构成物质的最小粒子
C.原子还可以分成更小的粒子 D.在化学反应里原子不能再分
2.原子核的构成是( )
A原子和中子 B电子和中子 C质子和中子 D质子、中子、电子
1.下列物质由原子直接构成的是( )
A.水 B.二氧化碳 C.铜 D.氧气
3.下列变化中,分子本身发生了变化的是( )
A.冰融化成水 B.二氧化碳变成了干冰
C.氧化汞受热分解生成了汞和氧气 D.碘加热变成了碘的蒸气
知识点2 原子
(1)定义:原子是化学变化中的最小粒子。
(2)基本性质:与分子一样,原子的体积和质量都很小,也是不断运动的,原子之间有间隔。
温馨提示:原子也可以直接构成物质,由原子直接构成的物质有:各种金属、稀有气体中的各种气体、一些固态非金属(如硫、磷)。
(3)原子的结构:原子在化学变化中虽然不能再分,但是它还是可分的,其结构如下:

在原子中,核电荷数=质子数=核外电子数。
温馨提示:原子的质量主要集中在原子核上,即原子的质量≈质子的质量+中子的质量=原子核的质量。
(4)相对原子质量:
①定义:以一种碳原子质量的1/12作为基准,其他原子的质量与这一基准
 的比,称为这种原子的相对原子质量。
的比,称为这种原子的相对原子质量。
②表达式:
温馨提示:相对原子质量=质子数+中子数。
(5)相对分子质量:相对分子质量等于构成分子的各原子的相对原子质量的总和。
易错点:相对原子质量是一个比值,不是原子的实际质量;同样,相对分子质量也不是分子的实际质量。,
练习题组2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com