
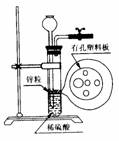
4.右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀 硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是
①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①③⑤ B.②⑥ C.③⑤ D.①②④
3.在给定条件下,下列加点的物质在化学反应中完全消耗的是
A.用50mL 8mol/L的浓盐酸与10g二氧化锰共热制取氯气
B.向100mL 3mol/L的硝酸中加入5.6g铁
C.标准状况下,将1g铝片投入20mL 18.4mol/L的硫酸中
 D.在5×107
Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨
D.在5×107
Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨
2.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,2.24L的苯中含有0.3 NA个碳碳双键
B.常温常压下,0.2mol铁在0.2mol氯气中充分燃烧,转移的电子数为0.6 NA
C.工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上溶解的铜原子数必为0.5NA
D.VLamoL/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA
1.2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程。“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓高亮度LED材料。下列说法正确的是
A.合金的熔点通常比组分金属高,硬度比组分金属小
B.已知Ga处于第ⅢA族,可推知氮化镓化学式为Ga3N2
C.工业上可用金属铝与V2O5在常温下冶炼钒, 铝作还原剂
D.ETFE膜( )是一种可焊接的塑料
)是一种可焊接的塑料
26.(11分)已知A是来自石油的重要有机化工原料,E是具果香味的有机物,F是一种高聚物,可制成多种包装材料:
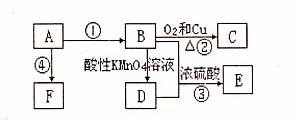
(1)A的最简式为: ,C的名称: 。F的结构简式: 。
(2)D分子中的官能团名称是 ,请设计一种实验来验证D物质中存在该官能团的方法是 。
(3)写出反应③的化学方程式并指出反应类型:
,反应类型 。
25. (8分)下图是A、B、C、D、E、F六种物质的转化关系。其中B是一种常见的无色无味的液体,C是一种有磁性的化合物,E是一种无色无味的有毒气体。
(8分)下图是A、B、C、D、E、F六种物质的转化关系。其中B是一种常见的无色无味的液体,C是一种有磁性的化合物,E是一种无色无味的有毒气体。
请回答下列问题:
(1)写出C的俗名: 。
(2)写出B的电子式: 。
(3)在B、D、E、F四种分子中,含有非极性键的是(填化学式) 。
(4)反应②③都是工业上非常重要的反应,请写出这两个反应的化学方程式。
② ;
③ .
24.(10分)某学生利用以下装置探究氯气与氮气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。请回答下列问题:
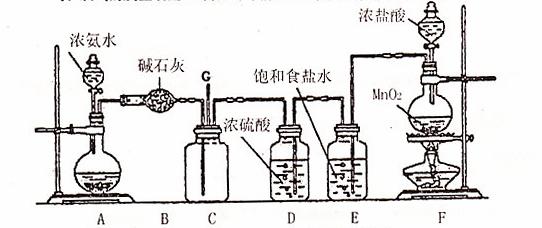
(1)装置A中的烧瓶内固体不可以选用(选填序号) 。
①生石灰 ②碱石灰 ③五氧化二磷 ④烧碱
(2)B装置的作用 ;用装置的用用 。
(3)通入C装置的两根导管左边较长、右边较短,目的是 。
(4)装置F中发生反应的化学方程式是 。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出该反应的化学方程式: 。
23.(7分)一种无色透明的溶液中,可能含有Na+、Ag+、NH4+、Mg2+和NO3-、CO32-、SO32-、MnO4中的某些离子,在三支试管中分别放入一定量的该溶液进行实验,其实验操作、现象或结果如下:
①第一支试管中加入盐酸,没有沉淀生成,但放出无色无味的气体。
②第二只试管中加入NaOH溶液,无沉淀生成;加热放出无色有刺激性气味的气体
③第三支试管中加入过量的BaCl2溶液,生成白色沉淀,将沉淀滤出放入足量的盐酸中,沉淀部分溶解。
(1)原溶液中肯定含有的离子是 ;可能含有的离子是 。
(2)写出实验②中反应的离子方程式 。
22.(8分)请简要说明下列实验失败的主要原因。
(1)把无水乙醇和冰醋酸放在圆底烧瓶中加热、蒸馏,几乎没有得到乙酸乙酯。
。
(2)在庶糖溶液中滴加几滴稀硫酸后水浴加热5min,取出少量溶液加入新制备的Cu(OH)2,后再加热,没有观察到有红色沉淀生成。
。
(3)做氨气的喷泉实验时,喷入烧瓶中的水未变红色。
。
(4)将氯气通入盛有有色布条的广口瓶中,布条未褪色。
。
21.(6分)实验室现有下列试剂:①浓硫酸②稀硫酸③浓硝酸④稀硝酸⑤浓盐酸⑥稀盐酸⑦NaOH溶液⑧浓氨水。请按下列要求填写下列空白(只填序号)
(1)除去镀铜的铁片表面的金属铜,最好选用 。
(2)除去镁片表面沉积的一层金属铝,最好选用 。
(3)配制高锰酸钾的酸性溶液时,所用的酸是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com