
10. 关于下列各实验和装置图的叙述中,不正确的是( )
关于下列各实验和装置图的叙述中,不正确的是( )
























 A.用图①所示的装置和试剂可制得乙酸乙酯
A.用图①所示的装置和试剂可制得乙酸乙酯
 B.装置②可用于测定气体体积,读数前必须把左右两管液面调平
B.装置②可用于测定气体体积,读数前必须把左右两管液面调平
 C.装置③中X若为四氯化碳,可用于吸收氨气,并能防止倒吸
C.装置③中X若为四氯化碳,可用于吸收氨气,并能防止倒吸
 D.装置④可用于收集H2、CO2、Cl2、HCl、NO2等气体(必要时可添加尾气处理装置)
D.装置④可用于收集H2、CO2、Cl2、HCl、NO2等气体(必要时可添加尾气处理装置)
9. 有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、
 NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下,结论不正确的是:( )
NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下,结论不正确的是:( )
|
实验步骤 |
实验现象 |
|
①取少量该溶液,加几滴石蕊试剂 |
溶液变成红色 |
|
②取少量该溶液,加Cu片和浓H2SO4,加热 |
有无色气体产生,在空气中又变成红棕色 |
|
③取少量原溶液,加BaCl2溶液 |
有白色沉淀生成 |
|
④取③中上层清液,加AgNO3溶液 |
有白色沉淀生成,且不溶于稀HNO3 |
|
⑤取少量原溶液,加NaOH溶液 |
有白色沉淀生成,当NaOH过量时有部分沉淀溶解 |
A.溶液中肯定存在的离子是Al3+、NO3-、SO4 、Cl-
、Cl-
 B.溶液中肯定不存在的离子是Fe2+、Ba2+、I-、HCO3-
B.溶液中肯定不存在的离子是Fe2+、Ba2+、I-、HCO3-
 C.无法确定溶液中是否含有Na+ 、Cl-
C.无法确定溶液中是否含有Na+ 、Cl-
 D.要确定溶液中是否含Cl-,可取少量原溶液,加入足量Ba(NO3)2溶液后,取
D.要确定溶液中是否含Cl-,可取少量原溶液,加入足量Ba(NO3)2溶液后,取
 上层清液加入AgNO3溶液和稀HNO3
上层清液加入AgNO3溶液和稀HNO3
7. 设NA表示阿伏加德罗常数,下列说法正确的是( )
设NA表示阿伏加德罗常数,下列说法正确的是( )





















 A.9 g SiO2晶体中含有的硅氧键数目为0.3 NA
A.9 g SiO2晶体中含有的硅氧键数目为0.3 NA
 B.28 g乙烯和28 g丙烯中均含有6 NA对共用电子对
B.28 g乙烯和28 g丙烯中均含有6 NA对共用电子对
 C.在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2 NA
C.在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2 NA
 D.标准状况下,22.4 L氖气与22.4 L氟气所含原子数均为2 NA
D.标准状况下,22.4 L氖气与22.4 L氟气所含原子数均为2 NA

|
 A.工业上用电解法冶炼铝: 2Al2O3
(熔融) ==== 4Al+ 3O2↑
A.工业上用电解法冶炼铝: 2Al2O3
(熔融) ==== 4Al+ 3O2↑
 B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
 C.采用离子交换膜法电解饱和食盐水制烧碱,可防止阴极室产生的Cl2进入阳极室
C.采用离子交换膜法电解饱和食盐水制烧碱,可防止阴极室产生的Cl2进入阳极室
 D.制硅酸盐水泥和普通玻璃都要用到石灰石作为原料
D.制硅酸盐水泥和普通玻璃都要用到石灰石作为原料
6. 对下列叙述中的化学知识,分析正确的是( )
对下列叙述中的化学知识,分析正确的是( )
 A.“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂
A.“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是指纤维素和油脂
 B.某雨水样品放置一段时间后pH由4.68变为4.28,是因为水中溶解的CO2增多
B.某雨水样品放置一段时间后pH由4.68变为4.28,是因为水中溶解的CO2增多
 C.鸡蛋清中加入氯化铵,会使蛋白质变性
C.鸡蛋清中加入氯化铵,会使蛋白质变性
 D.在含硫的燃料中加入适量生石灰,以减少二氧化硫的排放量
D.在含硫的燃料中加入适量生石灰,以减少二氧化硫的排放量
5. 右图曲线显示一个处于安静状态的人在不同气温中,
右图曲线显示一个处于安静状态的人在不同气温中,

 流经皮肤血管的血液相对流量。据此判断,下列叙述
流经皮肤血管的血液相对流量。据此判断,下列叙述
 错误的是( )
错误的是( )
 A.在AB段下丘脑分泌活动加强
A.在AB段下丘脑分泌活动加强
 B.在AB段机体甲状腺激素分泌增加
B.在AB段机体甲状腺激素分泌增加
 C.在D点以后需要及时补充水和无机盐
C.在D点以后需要及时补充水和无机盐
 D.在CD段皮肤血管收缩,汗腺分泌加强
D.在CD段皮肤血管收缩,汗腺分泌加强
4.
 如右图为植物光合作用强度随光照强度变化的坐标曲线图,分析下列叙述,不正确的是( )
如右图为植物光合作用强度随光照强度变化的坐标曲线图,分析下列叙述,不正确的是( )
 A.a点叶肉细胞产生ATP的细胞器只有线粒体,b点植物
A.a点叶肉细胞产生ATP的细胞器只有线粒体,b点植物
 光合作用强度与细胞呼吸作用强度相等
光合作用强度与细胞呼吸作用强度相等
 B.已知某植物光合作用和细胞呼吸最适温度分别为25℃
B.已知某植物光合作用和细胞呼吸最适温度分别为25℃
 和30℃,如图表示该植物处于25℃环境中,则将温度提
和30℃,如图表示该植物处于25℃环境中,则将温度提
 高到 30℃时,a点上移,b点右移,d点上移
高到 30℃时,a点上移,b点右移,d点上移
 C.当植物缺镁时,b点将向左移
C.当植物缺镁时,b点将向左移
 D.如果该图表示阴生植物,若改绘成阳生植物,则b
D.如果该图表示阴生植物,若改绘成阳生植物,则b
 点右移
点右移
3. 下列对于光合作用的叙述中,正确的是( )
下列对于光合作用的叙述中,正确的是( )





















 A.胡萝卜素、叶黄素在光合作用中的作用是吸收光能、转换光能
A.胡萝卜素、叶黄素在光合作用中的作用是吸收光能、转换光能
 B.光反应是把光能变成电能,暗反应是把电能变成化学能
B.光反应是把光能变成电能,暗反应是把电能变成化学能
 C.在相同光照条件下,各种植物的光合作用强度可能不同
C.在相同光照条件下,各种植物的光合作用强度可能不同
 D.大棚中人工补充光照越强,蔬菜产量越高
D.大棚中人工补充光照越强,蔬菜产量越高
2. 下图表示人体通过体液免疫消灭破伤风杆菌外毒素的过程,下列相关叙述正确的是
下图表示人体通过体液免疫消灭破伤风杆菌外毒素的过程,下列相关叙述正确的是

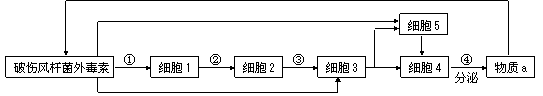




 A.细胞2、细胞3均起源于造血干细胞
,其中细胞2在骨髓中发育
A.细胞2、细胞3均起源于造血干细胞
,其中细胞2在骨髓中发育
 B.④过程高尔基体活动较旺盛
B.④过程高尔基体活动较旺盛
 C.所有细胞中仅细胞4中含有合成物质a的基因
C.所有细胞中仅细胞4中含有合成物质a的基因
 D.细胞4和细胞5具再次识别伤风杆菌外毒素的作用
D.细胞4和细胞5具再次识别伤风杆菌外毒素的作用
选择题一(本题包括21小题,每小题6分,共126分,每小题只有一个选项符合题意)
1.
 下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是( )
下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是( )
A.①过程的主要途径是生物固氮
B.完成②过程的生物可促进氮循环,但不利于土壤保持肥力
C.完成③过程的生物的新陈代谢类型与根瘤菌相同
D.完成⑦⑧过程的生物在生态系统的成分中属于分解者
2.[江苏省兴化市2008-2009学年高三年级第一学期期中调研 ](10分)2008年9月24日,国家重点工程--川维20万吨合成氨项目顺利实现中间交接。合成氨是生产尿素、磷酸铵、硝酸铵等化学肥料的主要原料,工业生产过程是以天然气或煤炭等为原料通过水蒸气重整工艺制得氢气,然后在一定条件下与氮气进行合成制得合成氨。
⑴已知合成氨反应的热化学方程式如下:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H=-92.4KJ/mol
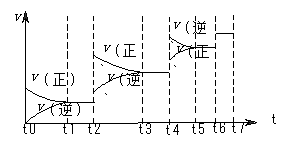
① 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如上图所示。图中t2起平衡移动的条件可能是 。
其中表示平衡混合物中NH3的含量最高的一段时间是 。
②温度为T℃时,将2amolH2和amolN2放入0 . 5L密闭容器中,充分反应后测得N2的转化率为50﹪。则反应的平衡常数为 (用带a的代数式表示)
⑵科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、压力1.0×105 Pa、反应时间3 h):
|
T/K |
303 |
313 |
323 |
353 |
|
NH3生成量/(10-6 mol) |
4.8 |
5.9 |
6.0 |
2.0 |
相应的热化学方程式如下:
N2(g)+3H2O(1)==2NH3(g)+  O2(g) △H1=+765.2 kJ·mol-1
O2(g) △H1=+765.2 kJ·mol-1
回答下列问题:
① 试在答题纸对应的图像中用虚线表示在上述反应中使用催化剂后能量的变化情况。
②与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com