
C4H10表示).电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.
①已知该电池的负极反应为C4H10+13O2--26e-===4CO2+5H2O,则该电池的正极反
应为________________________,电池工作时,电池中O2-向________极移动.
②液化石油气燃料电池最大的障碍是氧化反应不完全而产生的__________(填写物质的
名称)堵塞电极的气体通道.
(3)能源的紧缺在很大程度上制约了我国的经济发展.请你提出解决能源紧缺问题的两
点建议_____________________________________________________________________
________________________________________________________________________.
解析:(1)356 g CH4·9H2O可以释放出2 mol CH4,则甲烷的燃烧热为1 780.6 kJ÷2 mol
=890.3 kJ/mol.
(2)从信息提示,负极反应为C4H10+13O2--26e-===4CO2+5H2O,则正极应该为O2
得到电子生成负极所需的O2-;电池中阴离子向负极移动;液化石油气氧化反应不完全
可能产生CO或C,CO不能堵塞电极的气体通道,故应为固体炭.
(3)可以通过寻找开发新能源、提高现有能源利用率等措施来解决能源紧缺问题.
答案:(1)①“可燃冰”固体是高压下甲烷与水形成的,从海底取出后,压强减小,而
该固体本身分子间的作用力较弱,所以会放出甲烷气体 ②890.3 kJ/mol
(2)①O2+4e-===2O2- 负 ②固体炭
(3)寻找新能源、提高燃料的燃烧效率、提高能源利用率(任写两条即可)
13.(11分)某化学兴趣小组选用下列实验装置测定工业原料气(含SO2、N2、O2)中SO2的含量.
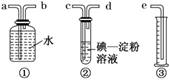
(1)若原料气从左向右流向时,上述装置组装连接的顺序是:原料气→____________(填
a、b、c、d、e).
(2)装置②中发生反应的离子方程式为______________________________;当装置②中
出现____________(填现象)时,立即停止通气.
(3)你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是________.(填序号)
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
(4)若碘溶液的浓度为0.05 mol/L,体积为20 mL,收集到的N2与O2的体积为297.6
mL(已折算为标准状况下的体积),SO2的含量是________mg/L.
解析:根据实验提供的装置及题给信息,要确定SO2的含量,需要知道SO2、N2、O2
的体积;解题要从SO2的性质作为突破点.
(1)可先求出SO2的体积,再利用排水法求出N2、O2的体积,即可解题,所以(1)应为c、
d、b、a、e.
(2)由于SO2+I2+2H2O===H2SO4+2HI的反应发生,利用②中蓝色褪去可确定反应完
全.实际起到一种指示剂的作用.
(3)因SO2具有还原性,②中颜色可以发生明显变化的反应均可代替碘的淀粉溶液,例
如酸性KMnO4溶液、溴水等.
(4)依据I2+SO2+2H2O===H2SO4+2HI,
知n(SO2)=n(I2)
则V(SO2)=0.05 mol/L×20×10-3L×22400 mL/mol=22.4 mL
m(SO2)=0.05 mol/L×20×10-3L×64×103 mg/mol=64 mg
则每升空气中SO2的含量为:
=200 mg/L.
答案:(1)c→d→b→a→e
(2)I2+SO2+2H2O===4H++SO+2I- 蓝色褪去
 (3)AC (4)200
(3)AC (4)200
12.(13分)化学在能源开发与利用中起着十分关键的作用.
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体,我国南海海底有极其丰富的“可燃冰”资源.
①将“可燃冰”从海底取出,“可燃冰”融化即可放出甲烷气体.试解释其原因:
________________________________________________________________________
________________________________________________________________________.
②取356 g分子式为CH4·9H2O的“可燃冰”,将其释放的甲烷完全燃烧生成液态水,
可放出1 780.6 kJ的热量,则甲烷的燃烧热为__________.
(2)设计出燃料电池使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之
11.(13分)裂化汽油中除含有C5-C11的烷烃外,还含有C5-C11的烯烃及甲苯、二甲苯等苯的同系物.要用化学方法检验某裂化汽油样品中含有烯烃及苯的同系物,实验步骤为:
(1)先逐滴加入________,振荡,如果看到________,则证明有________存在.
(2)继续逐滴加入________至________为止,静置,用分液漏斗分出______(填“上”或
“下”)层的裂化汽油样品,再加入__________振荡,如果看到____________,则证明
裂化汽油中有______________存在.
解析:因为烯烃可使溴水、酸性KMnO4溶液褪色,而苯的同系物只能使酸性KMnO4溶液褪色,根据这一性质差异,则先用溴水检验烯烃的存在,再用酸性KMnO4溶液检验苯的同系物的存在.(1)向样品中逐滴加入溴水,振荡,如看到溴水褪色,则证明有烯烃存在.(2)继续逐滴加溴水至不再褪色为止,用分液漏斗分出上层的裂化汽油样品,因为加足量溴水后,生成的卤代烷及水的密度均比烷烃和苯的同系物大,所以上层应是烷烃和苯的同系物的混合物.向分出的上层样品中加入酸性KMnO4溶液,如果紫色褪去,则证明有苯的同系物存在.
答案:(1)溴水 褪色 烯烃
(2)溴水 不褪色 上 酸性KMnO4溶液 溶液褪色 苯的同系物
10.(2009·扬州高三调研)乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源,通过乙醇制取氢气具有良好的应用前景.已知通过乙醇制取氢气有如下两条路线:
a.水蒸气催化重整:CH3CH2OH(g)+H2O(g)4H2(g)+2CO(g) ΔH=+255.58
kJ/mol
b.部分催化氧化:CH3CH2OH(g)+O2(g)3H2(g)+2CO(g) ΔH=+13.76 kJ/mol
则下列说法错误的是 ( )
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.降低温度,可提高b路线中乙醇的转化率
解析:相同质量的乙醇,a路线生成的氢气多;b路线需要的能量远远小于a路线;b
路线属于吸热反应,降低温度,平衡向生成乙醇的方向移动,故乙醇的转化率降低.
答案:D
9.党的十七大报告指出:“加强能源资源节约和生态环境保护,增强可持续发展能力.坚持节约能源和保护环境的基本国策,发展环保产业.”下列做法不符合这一要求的是
( )
A.将煤液化、气化,提高燃料的燃烧效率
B.安装汽车尾气催化转化装置,使之发生如下反应:
4CO+2NO24CO2+N2
C.在大力推广乙醇汽油的同时,研究开发太阳能汽车和氢燃料电池汽车
D.在水力发电、火力发电、核能发电和风力发电中,要大力发展火力发电
解析:火力发电会消耗大量资源,同时对环境造成污染,所以不符合要求.
答案:D
8.已知碳原子数≥3的烷烃均可裂化为碳原子数更少的一种烷烃和一种烯烃.含有5个碳原子的烷烃催化裂化可生成的烯烃最多有 ( )
A.4种 B.5种
C.3种 D.2种
解析:含有5个碳原子的烷烃,催化裂化时可按以下方式键断裂:
①C5H12△CH4+C4H8,②C5H12△C2H6+C3H6,③C5H12△C2H4+C3H8,
④C3H8△CH4+C2H4.在上述反应中生成的烯烃分子为C4H8、C2H4、C3H6,再结合
这些烯烃的同分异构体,可推知共有5种不同的烯烃分子.
答案:B
7.“抓好资源节约,建设环境友好型社会”是我国社会和经济长期发展的重要保证.你认为下列行为与之相悖的是 ( )
A.研制对目标昆虫有毒杀作用的新型、可降解杀虫剂
B.大力发展农村沼气,将废弃的秸秆转化为清洁、高效的能源
C.生活垃圾妥善处置,不污染环境
D.以聚苯乙烯全面代替木材,生产包装盒、快餐盒等以减少木材使用,保护森林
解析:使用新型、可降解杀虫剂,将减少对环境的污染,A正确;沼气属可再生能源,
使用沼气,可减少煤等化石燃料的燃烧量,减少污染,B正确;将生活垃圾分类妥善
处理,不污染环境,C正确;聚苯乙烯不易降解,会造成白色污染,故选D.
答案:D
6.(2009·广东高考)广州将于2010年承办第16届亚运会.下列措施有利于节能减排、改善环境质量的有 ( )
①在大亚湾核电站已安全运行多年的基础上,广东将继续发展核电,以减少火力发电
带来的二氧化硫和二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料
③加速建设地铁、轻轨等轨道交通,促进珠三角城市一体化发展,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾
A.①②③④ B.①②⑤
C.①②④⑤ D.③④⑤
解析:⑤中所述的内容与题干中所要求的“节能减排”无关且采用填埋法并没有真正
改善环境质量,故选A.
答案:A
5.绿色化学对于化学反应提出了“原子经济性”(原子节约)的新概念及要求.理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放.下列几种生产乙苯的方法中,原子经济性最好的是(反应均在一定条件下进行)( )

解析:依据原子经济性的概念,理想的原子经济性反应是原料分子中的原子全部转变
成所需产物,不产生副产物,实现零排放.
答案:C
4.下列符合化学实验“绿色化学”的有 ( )
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水 ②在铜与浓硫酸
反应的实验中,将铜片改为可调节高度的铜丝 ③将实验室的废酸液与废碱液中和后
再排放
A.①② B.①③ C.②③ D.①②③
解析:因为溴易挥发,所以在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃
取碘水;在铜与浓硫酸反应的实验中为避免生成过量的SO2污染空气,将铜片改为可
调节高度的铜丝;将实验室的废酸液与废碱液中和后再排放,可减少水体污染.
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com