
8.标准状况下,将CO2和CO混合气体(密度为1.79g/L)充满一盛有足量Na2O2的密闭容器(体积为22.4L,固体体积可忽略不计)用不间断的电火花引发至充分反应,下列对完全反应后容器里残留物的叙述正确的是
A.有0.125molO2
B. 有0.375molO2 
C. 有0. 5molCO D.
有0.25molNa2CO3
7. 坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现。 某种兴奋剂的结构简式如右图所示,有关该物质及其溶液的说法不正确的是
坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现。 某种兴奋剂的结构简式如右图所示,有关该物质及其溶液的说法不正确的是
A、该分子中所有氢原子不可能在同一个平面上
B、1 mol该物质与H2反应时,最多消耗7 molH2
C、加入FeCl3溶液呈紫色,因为该物质属于酚类物质
D、滴入酸性高锰酸钾溶液,紫色褪去,可证明结构中存在碳碳双键
6.下列物质反应时,生成物只有一种的是
A.镁在空气中燃烧
B.镁在二氧化碳中燃烧
C.磷在氯气中燃烧
D.铁在氯气中燃烧
5.对下列物质 ①氢硫酸 ②亚硫酸钠溶液 ③氯水 ④硫酸亚铁溶液 ⑤氢氧化钠溶液,只需观察试剂瓶内的情况就可作出该试剂是否变质结论的是
A.①②③
B.①②⑤
C.①③④
D.①②③④⑤
4. 欲将混合液中Al3+、Cu2+、Ba2+、Ag+逐一沉淀出来加以分离,加入试剂 ①Cl- ②SO42- ③OH- ④CO2⑤CO32-的正确顺序是
A.①②③④
B.③⑤①②
C.②①③⑤
D.①⑤③②
3.在氯化钡溶液中通入SO2,溶液仍澄清,若将硝酸钡溶液分装入两试管中,一支通氯气,另一支加烧碱溶液,然后再通入SO2,结果两试管都有有白色沉淀。由此得出的下列结论合理的是

 A.硝酸钡具有两性
B.两支试管内白色沉淀均是亚硫酸钡
A.硝酸钡具有两性
B.两支试管内白色沉淀均是亚硫酸钡 
C.SO2有还原性和酸性
D.升高pH一定能使SO2水溶液中SO32-离子浓度增大
2.下列物质在一定条件下一定不能与SiO2反应的是
A.  氢氟酸 B. 氧化钙 C. 碳酸钠固体 D. 浓硝酸
氢氟酸 B. 氧化钙 C. 碳酸钠固体 D. 浓硝酸
1.下列说法正确的是
A.酸雨是指pH小于7的雨水
B.空气中的NO2是造成光化学烟雾的主要因素
C.隐形材料是用肉眼看不见的材料
D.红磷用在安全火柴的火柴头上
30.(16分)资料显示不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。

(1)若在烧瓶中放入1.30g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,量气管的适宜规格是_____________ (选填:200,400,500) mL 。
(2)若1.30g锌粒完全溶解,氢氧化钠洗气瓶增重l.28g ,则圆底烧瓶中发生反应的化学方程式为:________________________________________
(3)若烧瓶中投入ag锌且完全反应,氢氧化钠洗气瓶增重b g.量气瓶中收集到VmL气体,则有:ag/65g·mol-1=bg/64g·mol-1+V mL / 22400 mL·mol-1,依据的原理是____________________________。
(4)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)=_______________(用含字母的代数式表示)。
(5) 反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
、 、
。
29.(14分) 甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
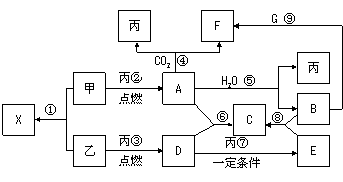
(1)写化学式:丙 E________
(2)X的电子式为_____________。
(3)写出反应⑥的化学反应方程式: 。
(4)写出B与G溶液反应生成F的离子方程式: 。
(5)在上图的反应中,不属于氧化还原反应的是(填序号)____________________。
(6)将8 g 乙在足量丙中燃烧,所得气体D通入100mL 3.5mol·L-1的B溶液中,完全吸收后,溶液中的溶质及其物质的量分别为 ;若同体积的气体D通入100mL 2.5mol·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com