
2.实验室制取气体的典型装置有时候还要根据具体情况加以选择或改进。
(1)制取乙炔气体时,由于反应剧烈,且产生大量泡沫,故应在选择 B 中的 ② 装置时,应在试管内的导管口 ,也可将试管换成 。
(2)加热液体混合物制取气体时,应在圆底烧瓶中加入少量 ,目的是 ;若制取少量气体时,则应 。
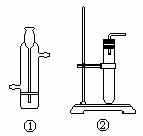
(3)右图①是目前市售的小型简易气体发生装置,该装置的功能与上图中 相同;若制取少量这类气体(无须加热)时,还可用右②这种最简易的装置,该装置的缺点是 。
实验室典型的气体发生装置有三大类:
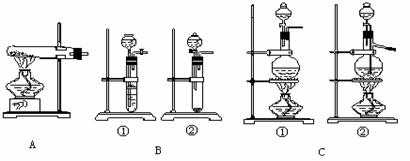
1.气体发生装置的选择要根据反应物的状态和反应条件来决定。
(1)选择 A 装置时,反应物应是 ,反应条件是 。
(2)选择 B 中的 ① 装置时,反应物应是 ,反应条件是 ;选择 B 中的 ② 装置时,反应物应是 ,反应条件是 。
 (3)选择
C 中的 ① 装置时,反应物应是
,反应条件是
;选择 C 中的 ② 装置时,反应物应是
,反应条件是
。
(3)选择
C 中的 ① 装置时,反应物应是
,反应条件是
;选择 C 中的 ② 装置时,反应物应是
,反应条件是
。
实验室制备各种气体应以实验室常用药品为原料,以安全、方便、经济为原则。同时在选择气体制备原理时,还应考虑使用该原理制取气体的装置要简单,所制得的气体要纯净。请你写出中学化学实验室制取下列 9 种气体的化学反应方程式:
|
序号 |
气体 |
反应原理 |
序号 |
气体 |
反应原理 |
|
1 |
O2 |
|
6 |
NO |
|
|
2 |
H2 |
|
7 |
NO2 |
|
|
3 |
CO2 |
|
8 |
C2H4 |
|
|
4 |
Cl2 |
|
9 |
C2H2 |
|
|
5 |
NH3 |
|
|
|
|
2. HN3称为叠氮酸,常温下为无色有刺激性气味的液体。N3-也被称为类卤离子。用酸与叠氮化钠反应可制得叠氮酸。而叠氮化钠可从下列反应制得:NaNH2+N2O=NaN3+H2O
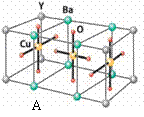 HN3、浓盐酸混合液可溶解铜、铂、金等不活泼金属,如溶解铜生成CuCl2-。铜和铂的化合物在超导和医药上有重要应用,Cu的化合物A(晶胞如图)即为超导氧化物之一,而化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中B异构体具有可溶性,可用于治疗癌症。试回答下列问题:
HN3、浓盐酸混合液可溶解铜、铂、金等不活泼金属,如溶解铜生成CuCl2-。铜和铂的化合物在超导和医药上有重要应用,Cu的化合物A(晶胞如图)即为超导氧化物之一,而化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中B异构体具有可溶性,可用于治疗癌症。试回答下列问题:
⑴ 基态氮原子核外电子排布的轨道表示式为 。
⑵ 元素N、S、P的第一电离能(I1)由大到小的顺序为 。
⑶ HN3属于 晶体,N3-的空间构型是 ,与N3-互为等电子体的分子的化学式为 (写1种)。NH2-的电子式为 ,其中心原子的杂化类型是 。
⑷ CuCl2-中的键型为 ,超导氧化物A的化学式为 。
⑸ 治癌药物B的结构简式为 。
1.(12分)波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料。已知CuSO4·5H2O的部分结构可表示如下:
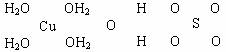
(1)写出铜原子价电子层的电子排布式____________,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有__________(填元素符号)。
(2)请在上图中把CuSO4·5H2O结构中的化学键用短线“--”表示出来。
(3)往浓CuSO4溶液中加入过量较浓的NH3·H2O直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液。小心加入约和溶液等体积的C2H5OH并使之分成两层,静置。经过一段时间后可观察到在两层“交界处”下部析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是______________________________________________。
(4)Cu(NH3)4SO4·H2O晶体中呈正四面体的原子团是______________,杂化轨道类型是sp3的原子是____________________________。
(5)如将深蓝色溶液加热,可能得到什么结果?________________________________。
9.设函数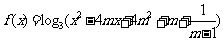 ,其中m是实数,设
,其中m是实数,设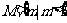
(1) 求证:当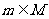 时,
时,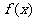 对所有实数x都有意义;反之,如果
对所有实数x都有意义;反之,如果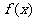 对所有实数x都有意义,则
对所有实数x都有意义,则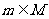 ;
;
(2) 当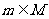 时,求函数
时,求函数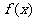 的最小值;
的最小值;
(3) 求证:对每一个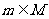 ,函数
,函数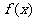 的最小值都不小于1.
的最小值都不小于1.
8.已知函数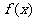 在定义域
在定义域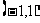 上是减函数,且
上是减函数,且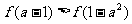
(1) 求a的取值范围;
(2)
解不等式:
7.设函数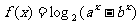 且
且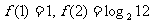
(1) 求a,b的值;
(2)
当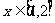 时,求
时,求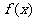 最大值
最大值
6.已知函数 满足:对任意实数
满足:对任意实数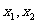 ,当
,当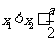 时,总有
时,总有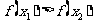 ,那么实数a的取值范围是
,那么实数a的取值范围是
5.函数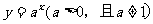 在
在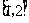 上的最大值比最小值大
上的最大值比最小值大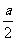 ,则a的值是
,则a的值是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com