
22.根据热化学方程S ( s ) + O2 ( g ) = SO2 ( g ) △H = -297.23 kJ/mol (反应在298K,101kPa下发生)分析下列说法不正确的是( )
A. 标况下,燃烧1mol S放出的热量为297.23 kJ
B. S ( g ) + O2 ( g ) = SO2 ( g ) 放出的热量大于297.23 kJ
C. S ( g ) + O2 ( g ) = SO2 ( g ) 放出的热量小于297.23 kJ
D. 形成1 mol SO2 的化学键所释放的总能量大于断裂 1 molS ( s )和 1mol O2 ( g )的化学键所吸收的总能量
21.从下列实验事实所引出的相应结论正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | H+浓度相同的盐酸和硫酸分别与等质量的形状相同的锌粒反应 | 反应开始速率相同 |
| D | 在容积可变的密闭容器中发生反应H2(g)+ I2(g)  2HI(g),把容积缩小一倍 2HI(g),把容积缩小一倍 | 反应速率不变 |
20.制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现( )
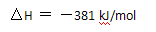 ①
①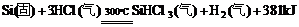
②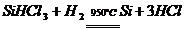
对上述两个反应的下列叙述中,错误的是
A. 两个反应都是置换反应 B. 两个反应都是氧化还原反应
C. 两个反应互为可逆反应 D. 反应②是放热反应
19.下列说法正确的是
A.增大反应物浓度,可增大单位体积内活化分子个数,从而使单位时间内有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
18.下列说法或表示法正确的是( )
A.1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热
B.由C(石墨)→C(金刚石) ΔH = +119 kJ·mol—1可知,石墨比金刚石稳定
C.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+ O2(g)===2H2O(l) ΔH = +285.8 kJ· mol—1
D.在101 kPa,298 K条件下,1 mol S和2 mol S的燃烧热相等
17.某探究小组利用丙酮的溴代反应(CH3COCH3+Br2 CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
| 实验 序号 | 初始浓度c/mol·L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.0010 | 290 |
| ② | 1.60 | 0.20 | 0.0010 | 145 |
| ③ | 0.80 | 0.40 | 0.0010 | 145 |
| ④ | 0.80 | 0.20 | 0.0020 | 580 |
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3), v(Br2)增大 B.实验②和③的v(Br2)相等
C.增大c(HCl), v(Br2)增大 D.增大c(Br2),v(Br2)增大
16.在一定条件下,在体积为VL的密闭容器中发生反应:mA + nB=pC。t秒末,A减少了1 mol,B减少了1.25 mol,C增加了0.5 mol。则m ∶ n ∶ p应为( )
A.4∶ 5∶ 2 B.2∶ 5∶ 4
C.1∶ 3∶ 2 D.3∶ 2∶ 1
15.未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生。下列属最有希望的新能源的是( )
①天然气 ②煤 ③核能 ④水电 ⑤太阳能 ⑥燃料电池 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧
C.③④⑤⑥ D.除①②外
14.用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气的生成速率加快的是( )
A.加入KHSO4固体 B.不用铁片,改用铁粉
C.滴加少量硫酸铜溶液 D.加入KNO3固体
13.已知H—H键能为436 kJ·mol-1,H—N键能为391 kJ·mol-1,根据化学方程式:N2 + 3H2 = 2NH3 ΔH = -92.4 kJ·mol-1,则N≡N键的键能是( )
A.431 kJ·mol-1 B.946 kJ·mol-1
C.649 kJ·mol-1 D.869 kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com