
5. 发现了116号元素R,则下列叙述正确是
( )
①其钠盐的分子式为Na2R;②其最高价氧化物的水化物是强酸;③R是金属元素;④R是非金属元素;⑤其最高价氧化物的分子式为RO3。
A.①③和⑤ B.②和④
C.③和⑤ D.②③和⑤
(本题考查了新元素的性质,要熟练掌握元素周期律和周期表的有关知识。)
4.下列各组属同素异形体的是 ( )
A.16O和18O B.金刚石、石墨和C60
C. O2和O3 D.H2O和H2O2
(本题考查同素异形体的辨析,要熟悉其概念。)
3. 随着核电荷数的递增,下列关于氧族元素(Po
除外)性质的叙述中,错误的是 ( )
A. 固态单质的导电性逐渐增强
B. 元素的非金属性逐渐增强
C. 氢化物的稳定性逐渐减弱
D. 单质的熔、沸点逐渐升高
(本题考查氧族元素的递变规律,要联系元素周期律并熟记!)
2. 过氧化氢沸点比水高,但受热易分解。某试厂
先制得7%-8%的过氧化氢溶液,再浓缩成30%的溶液时,可采用的适宜方法是 ( )
A.常压蒸馏 B.加生石灰常压蒸馏
C.减压蒸馏 D.加压蒸馏
(本题考查物质的浓缩方法,答题时要考虑过氧化氢的化学性质。)
1.下列关于臭氧性质的叙述中不正确的是( ) ( )
A.臭氧比氧气的氧化性更强,常温下能将Ag、Hg等较不活泼的金属氧化
B.臭氧可以杀死许多细菌,是一种良好的消毒剂
C.臭氧和活性炭一样,能够吸附有机色素,是一种很好的脱色剂
D.臭氧和氧气一定条件下可以相互转化
(本题考查O3的简单性质,要识记。)
4.(1997年上海高考题)接触法制硫酸排放的尾气中,含少量的二氧化硫。为防止污染大气,在排放前设法进行综合利用。
(1)某硫酸厂每天排放的1万米3尾气中含0.2%(体积百分数)的SO2。问用氢氧化钠溶液、石灰及氧气处理后,假设硫元素不损失,理论上可得到多少千克石膏。(CaSO4·2H2O)
(2)如果将一定体积的尾气通入100毫升2摩/升的氢氧化钠溶液使其完全反应,经测定所得溶液含16.7克溶质。试分析该溶液的成份,并计算确定各成分的物质的量。
(3)工厂在尾气处理制石膏的过程中,中间产物是亚硫酸氢钠。调节尾气排放的流量,以取得二氧化硫与氢氧化钠间物质的量的最佳比值,从而提高亚硫酸氢钠的产量。现设n(SO2)、n(NaOH)、n(NaHSO3)分别表示二氧化硫、氢氧化钠和亚硫酸氢钠的物质的量,且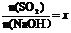
试写出X在不同取值范围时,n(NaHSO3)的值或
n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
|
x |
n(NaHSO3) |
|
|
|
|
|
|
|
|
|
(本题是一道综合计算题,能力要求高,涉及到过量判断及关系式法、极值法、数轴法等多种解题方法。)
新活题网站
3.过氧化氢(H2O2)的水溶液俗名双氧水,医疗上可作外科消毒剂。
(1)向含有酚酞的NaOH溶液中滴加双氧水,溶液由红 色褪至无色,主要原因是双氧水的 性。
(2)将双氧水加入经酸化的高锰酸钾溶液中,溶液的紫 红色消褪了,此时双氧水表现出 性。
(3)久置的油画,白色部位(PbSO4)常会变黑(PbS),用 双氧水揩擦后又恢复原貌,有关反应的化学方程为:
。
(本题主要考察H2O2的化学性质,从氧元素的化合价来分析入手。)
2.(1)(1996年上海高考题)为防治酸雨,降低煤燃烧时向大气排放的SO2,工业上将生石灰和含硫煤混合后使用。请写出燃烧时,有关“固硫”(不使硫化合物进入大气)反应的化学方程式: 、
。
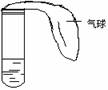 (2)(2000年全国高考题)某学生课外活动小组利用右图所示装置分别做如下实验:
(2)(2000年全国高考题)某学生课外活动小组利用右图所示装置分别做如下实验:
在试管中注入某无色溶液,加热试
管,溶液变为红色,冷却后恢复无
色,则此溶液可能是____________
溶液;加热时
溶液由无色变为红色的原因是:
。
(这两小题实质上都是考查SO2的化学性质。答题时要仔细分析,做到方程式书写合理、语言简洁流畅。)
1.(教育部考试中心1999年试测题)盛有氯化钡稀溶液甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量硝酸,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是 ( )
A .甲、乙两试管都有白色沉淀生成
B .甲、乙两试管都没有白色沉淀生成
C .甲试管没有白色沉淀生成而乙试管有
D .甲试管有白色沉淀生成而乙试管没有
(本题考查了多种物质之间的反应,答题时从SO2的性质入手。)
2. 二氧化硫
(1)物理性质:无色、刺激性气味、有毒气体,
密度比空气大,易溶于水(1∶40),易液化。
(2)化学性质:具有酸性氧化物的性质(与水、碱、碱性氧化物等反应)、较强的还原性(与O2、Cl2、Br2、I2等作用)、漂白性。SO2被O2氧化成SO3,SO3常温下是无色固体,熔沸点低,与水放出大量的热。
(3)SO2污染大气,形成酸雨,主要来源于化石燃料的燃烧、含硫矿石的冶炼和硫酸、磷肥、纸浆生产的工业废气。
典型题点击
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com