
11.2L(标准状况下)B生成,则发生转移的电
子的物质的量为 。
 (3)写出反应③的化学方程式:
。
(3)写出反应③的化学方程式:
。
25. (10分)已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为常见的化合物,乙常温下为液体,丙的焰色反应为
(10分)已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为常见的化合物,乙常温下为液体,丙的焰色反应为
黄色,右图为各种物质之间的转化关系。请回答下列问题:
(1)写出下列物质的化学式:A ,
B ,D 。
(2)甲的电子式为 ,反应②中若有
24.(8分)某气体的摩尔质量是Mg·mol-1,分子数为x,在标准状况下的体积是V L,质量是m g。一个12C原子的质量用m(C)表示。试说明下列各式表示的意义。
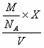
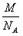
(1) ;(2) ;


(3) ;(4) 。
23.(6分)(1)用质量分数为98%、密度为1.84g·cm-3的浓硫酸配制100mL1.84mol∙L-1的稀硫酸。实验仪器有:A.100mL量筒;B.托盘天平;C.玻璃棒;D.50mL容量瓶;E.10mL量筒,F.胶头滴管;G.50mL烧杯;H.100mL容量瓶,实验时应选用的仪器的先后顺序是(填入编号):____ ____。
(2)在配制一定物质的量浓度的溶液时,如果实验操作不当,会产生误差。判断下列各种不当操作将导致所配溶液浓度偏高的是 。
A.称量时将称量物错放在托盘天平的右盘上;
B.未洗涤溶解用的烧杯和玻璃棒或洗液未转入容量瓶;
C.除洗涤烧杯和玻璃棒外,还洗涤了量筒(或移液管);
D.未等溶液冷却就定容; E.定容时仰视达标线;
F.定容后倒转容量瓶几次,发现液面最低点低于标线,再补滴水至标线;
G.配NaOH溶液,称量NaOH固体时在托盘上垫纸或直接称量;
H.定容时滴水超过了刻度线,后用滴管吸至刻度线;
22.(8分)氯、溴、碘同属于周期表中的VII A族,在上个世纪,人们很早就制得高碘酸及其盐,但得不到含+7价溴的化合物,1968年,化学家用发现不久的XeF2(二氟化氙)和KBrO3首先制得纯净的KBrO4晶体。
(1)高碘酸盐(IO65-)能在一定条件下将Mn2+氧化为MnO4-且自身被还原成碘酸根,其反应平稳而迅速,写出离子反应方程式: ;
(2)在250C,已知pH=2的高碘酸溶液与pH=12的NaOH溶液等体积混合,所得混合液
显酸性;0.01mol·L-1的碘酸或高锰酸溶液与pH=12的NaOH溶液等体积混合,所得
混合液显中性。则高碘酸是 ;高锰酸是 (填“强酸”或“弱酸”);
(3)写出XeF2和含KOH、KBrO3的水溶液反应得到KBrO4的离子方程式____________。
21.(1)(6分)铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
①写出制取铁酸钠的化学方程式: ;
②在制取铁酸钠的反应中 元素被氧化;
③铁酸钠之所以有净水作用,除杀菌外,另一个原因是 。
(2)(4分)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓氢氧化钠溶液。将发生一系列变化。已知,NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:NH4++A1O2-+H2O=Al(OH)3↓+ NH3↑
试回答:①硫酸铝铵在水溶液中的电离方程式为 ;②在逐滴加入浓氢氧化钠溶液的过程中,产生的现象有:a溶液中出现白色沉淀;b有刺激性气体逸出;c白色沉淀量逐渐增多;d白色沉淀完全消失;e白色沉淀逐渐减少。请回答各种现象由先到后出现的顺序是(用序号回答): 。
20. 研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物:

B.Fe在Cl2中的燃烧产物:
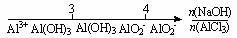
C.AlCl3溶液中滴加NaOH后铝的存在形式:
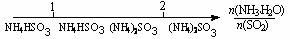
D.氨水与SO2反应后溶液中的铵盐:
19.将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为

18.某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种组成。取该溶液进行如下实验:①取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;②在①所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的有
A.Na+、AlO2-、SO42- B.Na+、AlO2-、CO32-
C.Na+、Al3+、CO32- D.Na+、MnO4-、CO32-
17.某单质X能从盐的溶液中置换出单质Y。由此可知
A.当X是非金属时,Y可能是金属,也可能是非金属
B.当X、Y都是非金属时,Y一定比X活泼
C.当X、Y都是金属时,X一定比Y活泼
D.当X是金属时,Y只能是金属
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com