
① 工业制硝酸:关系式:NH3→HNO3
② NO和O2混合气体溶于水:关系式:4NO→3O2时,无气体剩余。若VNO:VO2 >4:3 则剩余NO, 若VNO:VO2 <4:3则剩余O2。
③ NO2和O2混合气体溶于水:关系式:4NO2→O2时,无气体剩余。若VNO2:VO2 >4:1则剩余NO(不能剩余NO2), 若VNO:VO2 <4:1则剩余O2。
④关于CO2和NO混合气体通过Na2O2的计算规律:
ⅰ、若剩余气体体积大于原混合气体体积的一半时,V剩余=VNO, 剩余气体为NO和NO2。
ⅱ、若剩余气体体积等于原混合气体的一半时,VCO2:VNO≥1:1,如果VCO2:VNO>1:1时,剩余气体为NO2和O2;如果VCO2:VNO=1:1时,剩余气体为NO2。
⑤关于守恒法在金属和硝酸反应计算中的应用:
磷及其化合物的转化关系:
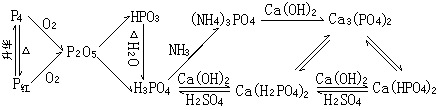
磷酸是一种难挥发的中强三元酸,能与碱反应生成一种正盐和两种酸式盐,除K+、Na+、NH4+、H2PO4-的盐之外,其余均不溶于水。磷酸二氢盐的水溶液以电离为主,显酸性;可溶性磷酸一氢盐的水溶液以水解为主,显碱性。
[练习] 1、关于磷的叙述正确的是( )
A、红磷没有毒性而白磷剧毒。 B、白磷在空气中加热到260℃可转变为红磷。
C、白磷可用于制造安全火柴。 D、少量白磷应保存在水中。
2、26.4g(NH4)2SO4与过量的NaOH共热,放出的气体全被含39.2g H3PO4 的溶液吸收,则产物为( )
(A)NH4H2PO4 (B)(NH4)2HPO4
(C)(NH4)3PO4 (D) NH4H2PO4 和(NH4)2HPO4
4、在浓硝酸中加入铜片:
(1)开始反应的化学方程式为: 。
(2)若铜有剩余,则反应将要结束时的反应方程式是:
。
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是:
3、某浓硝酸与单质反应,若参加反应的单质与硝酸的物质的量之比为1:4时,且还原产物为单一的产物,该元素的化合价可能是( )
A、+1 B、+2 C、+4 D、+5
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com