
4.相同碳原子数的一氯代烷烃的同分异构体沸点如何变化?
3.一氯代烷烃随碳原子数的增多,沸点逐渐 ,密度逐渐 。
2.溶解性:卤代烃难溶于 ,易溶于 。
1.饱和一卤代烃的通式为 。
1.定义:烃分子中的氢原子被卤素原子取代后所生成的化合物。
[过渡]根据卤代烃的定义可知,在卤代烃分子中,卤原子的种类可以不同,烃基可以不同,卤原子的个数也可以不同。那么,这些种类繁多的卤代烃,我们该如何给它归类呢?
[板书]2.分类
[学生讨论后小结并板书]

[过渡]这些种类繁多的卤代烃在性质上有什么差异性和相似性呢?下面我们以一氯代烃为例,首先来看它们的物理性质。
[板书]3.物理性质
[师]请同学们看课本147页表6-1,并结合我们学过的相关知识,分组讨论后回答投影中的问题。
[投影]
(一)本课预习题:
1、密闭容器中气体的压强:
A、是由于气体的重力所产生的;
B、是由于气体分子频繁碰撞容器壁所产生的;
C、是由于分子之间存在相互作用力而产生的;
D、当容器自由下落时,气体的压强将减小。
2、关于大气压强,下列说法中正确的是:
A、是由于地球对大气的吸引作用而产生的;
B、大气压强的方向总是竖直向下的;
C、大气压强的大小随高度的增加而减小;
D、教室里的大气压强比操场上的大气压强小;
3、关于热力学温标,下列说法中正确的是:
A、热力学温标的零度是-273.15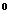 C ,叫做绝对零度;
C ,叫做绝对零度;
B、因为热力学温度的每一度的大小和摄氏温度是相同的,所以0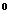 C也就是绝对零度;
C也就是绝对零度;
C、绝对零度已经达到了,温度计可以测出开氏零度;
D、0K是低温的极限,是达不到的。
4、当温度升高30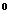 C时,用热力学温标表示升高的温度是:
C时,用热力学温标表示升高的温度是:
A、303K ; B、30K ; C、243K ; D、273K 。
4、气体压强的确定:
气体的三个状态参量中,准确地确定气体压强是解决热学问题的关键。一般的分析方法如 下:
(1)被一段液柱或活塞封闭的气体,其压强可根据液柱或活塞的受力情况来得出。如图所示(P32),一粗细均匀、一端封闭的玻璃管开口向上竖直放置,内有一段液柱,液柱的高度为h,横截面积为S,密度为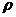 ,液柱受三个力的作用而处于静止状态,它们分别是重力G=mg=
,液柱受三个力的作用而处于静止状态,它们分别是重力G=mg=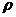 Vg=
Vg=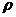 Sgh,方向竖直向下;外界大气压F
Sgh,方向竖直向下;外界大气压F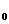 =P
=P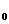 S,方向竖直向下;封闭气体向上的压力F=PS,方向竖直向上,由平衡方程得:
S,方向竖直向下;封闭气体向上的压力F=PS,方向竖直向上,由平衡方程得:
F=F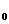 +G ,
+G ,
即PS=P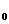 S+
S+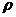 Sgh 。
Sgh 。
所以封闭气体的压强为:
P=P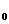 +
+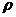 gh= P
gh= P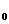 +P
+P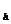 。
。
*若如图所示的装置沿竖直方向以加速度a向上做匀加速直线运动,则牛顿第二定律得:
P= P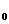 +
+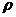 gh+
gh+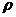 ah 。
ah 。
(2)对于U型管内封闭的气体压强,可用以下方法分析得出。如图所示,U型管的右端封闭,左端开口,里面装有液体,液体的密度为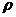 ,左端液面比右端液面高h,外界大气压强为P
,左端液面比右端液面高h,外界大气压强为P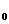 ,封闭气体的压强为P,因为液体内同一高度处的压强相等,即P
,封闭气体的压强为P,因为液体内同一高度处的压强相等,即P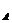 =P
=P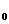 +
+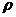 gh ,P
gh ,P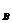 =P
=P
,所以封闭气体的压强为P=P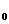 +
+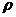 gh=P
gh=P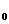 +P
+P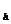 。
。
*注意同一高度处的压强相等的条件是该处下部必须充满同一种液体,即下部不能夹带有气体或其它种类的液体。
4、气体的压强
(1)气体作用在器壁单位面积上的压力称为气体的压强。
气体压强的产生是由于大量气体分子频繁的碰撞器壁的结果,压强的大小取决于单位体积内的分子数和分子的平均速率。若单位体积内分子数增大,分子的平均速率也增大,则气体的压强也增大。
(2)SI制中压强的单位为帕斯卡(Pa),1Pa=1N/m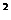 ,压强的单位有时还用到atm ,cmHg,mmHg等。
,压强的单位有时还用到atm ,cmHg,mmHg等。
1atm=76cmHg=1.03×10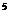 Pa 。
Pa 。
(3)大气压强产生的机理:
大气压是由于空气受到重力的作用紧紧包围地球而对浸在它里面的物体产生的压强。如果没有地球引力作用,地球表面就没有大气,从而也不会有大气压。地面大气压的值与地球表面积的乘积,近似等于地球大气层所受的重力值。
3、气体的体积:
(1)因为气体分子间距离比固体、液体分子间的距离大很多,分子间的相互作用很弱,所以气体很容易扩散,气体的体积就是指气体分子所能够达到的空间,也就是气体所充满的容器的容积。
(2) SI制中单位为m ,常用的有L,1L=10
,常用的有L,1L=10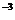 m
m 。
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com