
(二)选考题(请考生从给出的3道物理题、3道化学题、2道生物题中任选一题做答,并用2B铅笔在答题卡上把所选题目的题号涂黑。注意所做题号必须与所涂题目的题号一致,在答题卡区域指定位置大题。如果多做,则每学科按所做的第一题计分。注意:黑龙江考生化学选做题只能从37题“物质结构与性质”和38题“有机化学基础”中选择一题作答,若回答36题“化学与技术”选做题以0分计。)
33.(15分)[物理--选修3-3]
(1)下列说法正确的是: ( )
A.物体放出热量,温度不一定降低
B.物体内能增加,温度一定升高
C.热量能自发的从低温物体传给高温物体
D.热量能自发的从高温物体传给低温物体
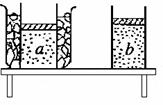
(2)如图所示,教室内用截面积为0.2m2的绝热活塞,将一定质量的理想气体封闭在圆柱形汽缸内,活塞与气缸之间无摩擦,a状态是汽缸放在冰水混合物中气体达到的平衡状态,活塞离汽缸底部的高度为0.6m;b状态是汽缸从容器中移出后达到的平衡状态,活塞离汽缸底部的高度为0.65m。设室内大气压强始终保持1.0×105Pa,忽略活塞质量。
①求教室内的温度;
②若气体从状态a变化到状态b的过程中,内能增加了560J,求此过程中气体吸收的热量。
34.(15分)[物理--选修3-4]
(1)(5分)图是一列简谐横波在某时刻的波形图,已知图中b位置的质点起振比a位置的质点晚0.5 s,b和c之间的距离是5 m,则此列波的波长和频率应分别为( )
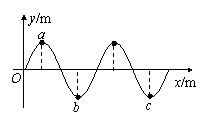
A.5 m,1 Hz B.10 m,2 Hz
C.5 m,2 Hz D.10 m,1 Hz
(2)(10分)图示是一透明的圆柱体的横截面,其半径R=20cm,折射率为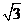 ,AB是一条直径,今有一束平行光沿AB方向射向圆柱体,试求:
,AB是一条直径,今有一束平行光沿AB方向射向圆柱体,试求:
①光在圆柱体中的传播速度
②距离直线AB多远的入射光线,折射后恰经过B点

35.(15分)[物理--选修3-5]
(1)(5分)以下说法正确的是 (填入选项前的字母,有填错的不得分)
A.β射线的穿透能力比α射线强,能穿透几厘米厚的铅板
B.原子核的比结合能越大,表示原子核中核子结合得越牢固,原子核越稳定
C.氢原子从一种定态跃迁到另一种定态过程中,若氢原子放出一个光子,则其电子的动能增大,轨道半径变小
D.在发生光电效应时,若入射光的强度一定,则入射光的频率越高,单位时间内逸出的光电子数越多,打出光电子的最大初动能越大
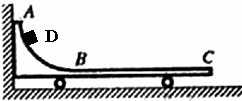
(2)(10分)如图所示,小车质量为M=2.0kg,带有光滑的圆弧轨道AB和足够长的粗糙水平轨道BC,一小物块(可视为质点)质量为m=0.5kg,与水平轨道BC的动摩擦因数为μ=0.1。现将小车置于光滑水平面上,小车左端紧靠竖直墙壁,若小物块从距水平轨道BC高为0.8m的D点由静止释放, 试求小物块能在水平轨道BC上滑行的最大距离(重力加速度g=10m/s2)。
36.(15分)[化学与技术]硫酸在日常生产生活中应用非常广泛。请回答硫酸工业中的如下问题:
(1)早期生产硫酸以黄铁矿为原料,目前很多国家都已经限制以黄铁矿为原料而以硫黄为原料,以硫黄为原料的优点是 。
(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3,是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO27%;O21l%;N2 82%);
  压强/Mpa 压强/Mpa转化率/% 温度/℃ |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
8 5.8 5.8 |
89.5 |
96.4 |
利用表中数据分析。在实际生产中选择的适宜生产条件是:温度_______ ℃,压强 ___________MPa。
(3)选择适宜的催化剂,是否可以提高SO2的转化率? _______(填“是”或“否”),是否可以增大该反应所放出的热量? (填“是” 或“否”)。
(4)为提高SO3吸收率,实际生产中用 吸收SO3。
(5)在催化反应室中设有热交换装置,以下叙述与热交换装置的作用有关的是______(填写序号)。
A.保护环境。防止空气污染 B.充分利用热量,降低生产成本
C.升高温度,提高SO2的转化率 D.防止催化剂中毒
 (6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用
________(填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产水泥的辅料,写出这两步反应的化学方程式_________________________。
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用
________(填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产水泥的辅料,写出这两步反应的化学方程式_________________________。
37.(15分)[物质结构与性质]
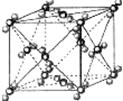
I.固体二氧化碳外形似冰,受热汽化无液体产生,俗称“干冰”,根
据干冰晶胞结构回答:
(1)干冰中一个分子周围有__________个紧邻分子
 (2)堆积方式与干冰晶胞类型相同的金属有_________(从“Cu、
(2)堆积方式与干冰晶胞类型相同的金属有_________(从“Cu、
Mg、K、Po”中选出正确的),其空间利用率为_______
(3)CO2中心原子的杂化方式为_______,有一种与CO2互为等电
子体的离子,能用于鉴别Fe3+ ,写出其电子式___________
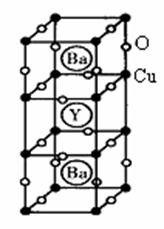
II. 钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元
素有两种价态,+2价和+3价。
(4)写出Cu3+的电子排布式:
(5)根据图示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比,
确定其化学式为:
(6)根据(5)所推出的化合物的组成,(该化合物中各元素的化合价
为Y +3、Ba +2),计算该物质中+2价和+3价的Cu离子个数比为
_______________。
38.(15分)[有机化学基础]
某有机物X(C12H13O6Br)遇到FeCl3溶液显紫色,其部分结构简式如下:

已知:X在足量的氢氧化钠水溶液中加热,可以得到A、B、C三种有机物。(1)C用核磁共振氢谱分析,发现只有一个吸收峰。(2)室温下A经盐酸酸化可以得到苹果酸E,试回答:
(1)B中所含官能团的名称是_______。
(2)C的结构简式为________________。
(3)E能发生的反应类型是_______(填序号)。
①加成反应 ②消去反应
③氧化反应 ④酯化反应
(4)E的一种同分异构体F有如下特点:1molF可与3mol金属钠发生反应放出33.6LH2(标准状况下),1molF也可与足量NaHCO3溶液反应生成1molCO2 ,1molF 还可与足量的银氨溶液反应生成2molAg。则F的结构简式可能是(请写出两种)________________。
(5)在一定条件下两分子E可以生成六元环酯,写出此反应的化学方程式:
_______________________________ ________。
39.(15分)[生物技术实践]
啤酒是我们日常生活中最常见的饮料之一。在啤酒生产过程中,发酵是重要环节。生产过程大致如下:将经过灭菌的麦芽汁充氧,接入啤酒酵母菌菌种后输入发酵罐。初期,酵母菌迅速繁殖,糖度下降,酒精浓度渐渐上升,泡沫不断增多。当糖度下降到一定程度后,结束发酵。最后分别输出有形物质和啤酒。根据上述过程,回答以下问题:
(1)具有耐高糖和耐酸特性的酵母菌是理想的酒精发酵菌种,对野生酵母菌进行诱变后通过筛选可以得到具有这些特性的突变菌,诱变及筛选过程如下:
步骤1:野生菌液体培养一段时间后接受紫外线照射诱变处理。
步骤2:制备选择培养基。在基本培养基的基础上,注意 和 ,加琼脂后灭菌,制成固体平板。
步骤3:将紫外照射后的菌液稀释涂布平板。
步骤4:根据 筛选出突变菌。
(2)酿酒过程中,经检测活菌数量适宜但却不产生酒精,应采取的措施是 。
(3)为研究发酵罐中酵母菌的生长状况,常要取样统计分析,并测定pH值,判断取样先后顺序的主要依据是 。
(4)小麦脱粒以后还有大量的麦秆,主要成分为木质素、纤维素和半纤维素,但是酵母菌无法直接利用,原因是 。请提出解决该问题的方法。(列举两种方法)
(5)突变菌往往带有一些特殊的基因。在获得这些基因的过 程中,PCR技术相当重要。PCR扩增反应中加入引物的作用是
,加入DNA聚合酶的作用是
。
程中,PCR技术相当重要。PCR扩增反应中加入引物的作用是
,加入DNA聚合酶的作用是
。
40.(15分)[现代生物科技]
转基因植物油是由转基因植物通过压榨或浸出法加工制得的,因其出油率高而被广泛应用。我国是植物油消费大国,每年都从国外进口大量的转基因植物油。
(1)在培育转基因油料植物的过程中,基因操作需要的工具酶是 。在基因表达载体中,目的基因的首端必须含有 ,它是 识别和结合位点。
(2)请写出一种将目的基因导入油料植物细胞可以采用的方法:
。若受体细胞为植物体细胞可采用
技术获得转 基因植物体,该技术所依据的原理是
。
基因植物体,该技术所依据的原理是
。
(3)若要检测⑵中获得的植物细胞染色体上是否含有目的基因,可采用 技术。
(4)若利用蛋白质工程继续提高油料植物的出油率,其设计流程应从预期的 出发,设计预期的 结构,推测出应有的 序列,然后找到相对应的________ 序列,再用转基因技术改变现有性状。我国种植转基因油料作物同时仍保留原来非转基因的油料作物等其他原有作物这是依据生态工程中的 原理。
(一)必考题
22.(6分)某学生用打点计时器研究小车的匀变速直线运动。他将打点计时器接到频率为50Hz的交流电源上,实验时得到一条如图所示的纸带。他在纸带上便于测量的地方选取第一个计时点,在这点下标明A,第六个计时点下标明B,第十一个计时点下标明C,第十六个计时点下标明D,测得AC长为14.56cm,BD长为19.72cm,则C点时小车的瞬时速度大小为 m/s。小车运动的加速度大小为 m/s2,(保留3位有效数字)
23. (9分)电流表A1的量程为0~200μA、内电阻约为500Ω,现要测其内阻,除若干开关、导线之外还有器材如下:
(9分)电流表A1的量程为0~200μA、内电阻约为500Ω,现要测其内阻,除若干开关、导线之外还有器材如下:
电流表A2:与 A1规格相同
A1规格相同
滑动变阻器R1:阻值0~20Ω
电阻箱R2:阻值0~9999Ω
保护电阻R3:阻值约为3kΩ
电源:电动势E约1.5V、内电阻r约2Ω
①如图所示,某同学想用替代法测量电流表内阻,他设计了
部分测量电路,在此基础上请你将滑动变阻器接入电路中,
使实验可以完成。
②电路完整后,请你完善以下测量电流表A1内电阻的实验步
骤。
a.先将滑动变阻器R1的滑动端移到使电路安全的位置,再把电阻箱R2的阻值调到 (填“最大”或“最小”)
b.闭合开关S1、S,调节滑动变阻器R1,使两电流表的指针在满偏附近,记录电流表A2的示数I
c.断开S1,保持S闭合、R1不变,再闭合S2,调节电阻箱R2,使电流表A2的示数 ,读出此时电阻箱的示数R2 ,则电流表A1内电阻 r=
24.(14分)如图所示,倾角q=30°、宽度L=1.0m的足够长的U形平行光滑金属导轨固定在磁感应强度B=1.0T、范围充分大的匀强磁场中,磁场方向垂直导轨平面斜向上,现用一平行导轨的牵引力牵引一根质量m=0. 20kg、电阻R=1.0
20kg、电阻R=1.0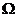 、垂直导轨的金属棒ab,由静止沿导轨向上移动(ab棒始终与导轨接触良好且垂直,不计导轨电阻及一切摩擦)。若牵引力功率恒为72W,经时间t=2.0s达到稳定速度,此过程金属棒向前滑行的位移S=4.0m。求金属棒的稳定速度及此过程金属棒上产生的热量(结果保留两位有效数字)。
、垂直导轨的金属棒ab,由静止沿导轨向上移动(ab棒始终与导轨接触良好且垂直,不计导轨电阻及一切摩擦)。若牵引力功率恒为72W,经时间t=2.0s达到稳定速度,此过程金属棒向前滑行的位移S=4.0m。求金属棒的稳定速度及此过程金属棒上产生的热量(结果保留两位有效数字)。
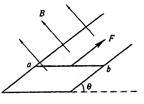
25.(18分)在如图所示的空间里,存在垂直纸面向里的匀强磁场,磁感应强度为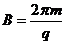 。在竖直方向存在交替变化的匀强电场(竖直向上为正),电场大小为
。在竖直方向存在交替变化的匀强电场(竖直向上为正),电场大小为 。一倾角为θ、长度足够的光滑绝缘斜面放置在此空间。斜面上有一质量为m,带电量为-q的小球,从t=0时刻由静止开始沿斜面下滑,设第1秒内小球不会离开斜面,重力加速度为g。求:
。一倾角为θ、长度足够的光滑绝缘斜面放置在此空间。斜面上有一质量为m,带电量为-q的小球,从t=0时刻由静止开始沿斜面下滑,设第1秒内小球不会离开斜面,重力加速度为g。求:
(1)第1秒末小球的速度
(2)第2秒内小球离开斜面的最大距离。
(3)若假设第5秒内小球未离开斜面,θ角应满足什么条件?

26.(15分)蓝铜矿主要含2CuCO3·Cu(OH)2,还含有少量Fe、Si的化合物,工业上以蓝铜
矿为原料制备Cu及CaCO3,方法有多种。
(1)蓝铜矿与焦炭加热可以生成铜、二氧化碳和水,写出该反应的化学方程式
。
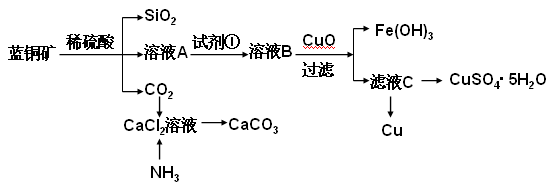 具体方法步骤如下:
具体方法步骤如下:
请回答下列问题:
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:检验溶液A中含有Fe2+的最佳试剂为 (填代号),实验步骤中试剂①为 (填代号)。
a.KMnO4 b.(NH4) 2S c.H2O2 d.KSCN
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发,冷却结晶、过滤等操作,加热蒸发至 ___________________时停止加热。玻璃棒在整个操作中的作用是 ________________ 。
(4)制备CaCO3时,应向CaCl2溶液中先通入(或先加入) (填化学式)。若实验过程中有氨气逸出、应选用下列 装置吸收尾气(填代号)。
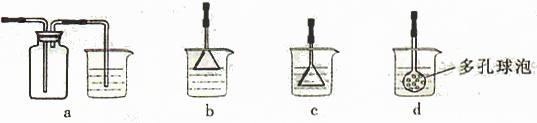
(5)从溶液C中获得Cu的方法有 (写出两种不同方法)
(6)用惰性电极电解硫酸铜溶液一段时间后,加入2molCu(OH)2固体使硫酸铜溶液复原(复原是指溶液溶质成分及浓度与原来完全相同),则此电解过程中共转移电子 mol。
27.(14分)现有A、B、C、D四种物质,B、D的焰色反应均为黄色。C是一种酸式盐,将C加入BaCl2溶液有不溶于盐酸的白色沉淀生成,D晶体在干燥空气中容易逐渐失去结晶水变成白色粉末。对A、B、C、D进行下列实验,实验过程和记录如下图所示(无关物质已略去),请回答:

(1)X与B反应的离子方程式为 。
(2)D溶液pH值大于7,原因是(用离子方程式表示) 。
(3)写出C与过量B反应(加热)的离子方程式 __________________ 。
(4)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序_____________________.
(5) Y在同主族的同类物质中分子稳定性最强( ),也是沸点最高的( )。(判断正误填"是"或"否")
(6)若向三份足量的B的稀溶液中分别加入少量稀醋酸、稀硝酸、浓硫酸,均生成1molH2O时的反应热分别为 △H1 ,△H2 ,△H3 ,则三者由大到小排序为:______________.
28.(14分)向某密闭容器中加入0.6molA、0.2molC和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如甲图所示(其中t0-t1阶段c(B)未画出)。乙图为反应体系中反应速率随时间变化的情况,且四个阶段都只改变一种条件(催化剂、温度、浓度、压强,每次改变条件均不同),已知t3-t4阶段为使用催化剂。
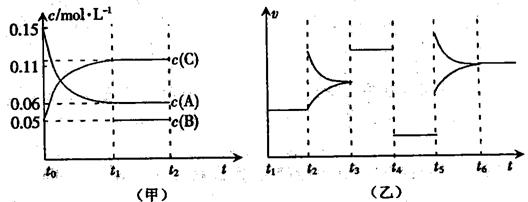
(1)若t1=5s,则t0-t1阶段以C浓度变化表示的反应速率为v(C)=________mol/(L•s)。
(2)若t2-t3阶段,C的体积分数变小,此阶段v(正)___v(逆)(填“>”、“=”或“<”)。
(3)t4-t5阶段改变的条件为_______,B的起始物质的量为_______。
(4)t5-t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式:__________________________________。
(5)该反应的化学平衡常数K可表示为_______________。[用含c(A) 、c(B) 、c(C)的式子表示]
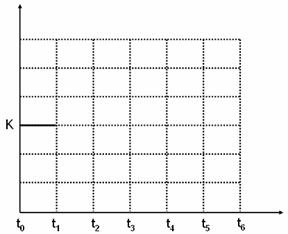 并在下图中补画出t1-t6 各阶段K的变化趋势图像
并在下图中补画出t1-t6 各阶段K的变化趋势图像
29.(10分)春天日照逐渐延长时,鸟类大多数进人繁殖季节。调节鸟类繁殖活动的图解如下:
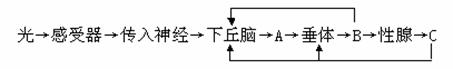
(1)鸟类的繁殖活动是通过机体的 和 两种调节方式完成的。机体中既能传导兴奋,又能分泌激素的细胞位于 。
(2)上面图解中的A、B、C分别代表由下丘脑、垂体和性腺分泌的物质,则它们分别是 、 和 。C进人血液后,通过 作用来调节下丘脑和垂体中激素的合成和分泌。
(3)据图判断,若要验证B的生理作用,
(能、不能)用去除性腺的鸟作为实验动物, 其原因是
。
其原因是
。
30.(9分)请回答下列有关遗传的问题。
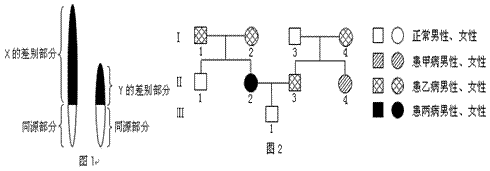
(1)图1是人类性染色体的差别部分和同源部分的模式图。有一种遗传病,仅表现为父亲传给儿子不传给女儿,该致病基因位于图中的 部分。
(2)图2是某家族遗传系谱图,据图回答。
①甲病属于 染色体 遗传病。
②从理论上讲,Ⅱ-2和Ⅱ-3的女儿都患乙病,儿子患乙病的几率是1/2。由此可见,乙病属于____ 染色体 遗传病。
③若Ⅱ-2和Ⅱ-3再生一个孩子,这个孩子同时患两种病的几率是 。
④该家系所在地区的人群中,每50个正常人中有1个甲病基因携带者,Ⅱ-4与该地区一个表现正常的女子结婚,则他们生育一个患甲病男孩的几率是 。
31.(8分)下图1表示生态系统中各成分之间通过含碳化合物构成的联系,图2为一定时间内某一生态系统中构成一条食物链的几个种群数量变化曲线,请据图回答:
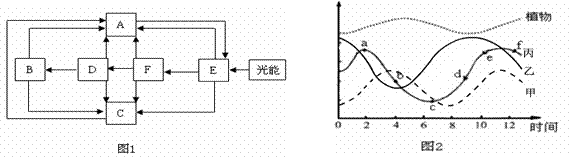 (1) 图1中能构成群落的是
,图2中的乙相当于图1中的
。
(1) 图1中能构成群落的是
,图2中的乙相当于图1中的
。
(2)图1中流入D的总能量小于F获得的总能量,主要原因是F获得的能量除了被自身消耗以及未被利用外,还有部分能量被 所利用。
(3)种群丙在a、d、c、d四个时期中种群增长率最大的是 期。
(4)某地区因环境污染造成E中出现部分白化苗,对F、D数量的影响是 。
(5)F中某蛋白质由m条肽链、n个氨基酸组成。该蛋白质至少有氧原子的个数是( )
A. n-m B. n-2m C. n+m D. n+2m
32.(12分)下图 甲表示两种不同的植物(阳生植物和阴生植物)随着日光照射强度的变化,吸收CO2量与放出CO2量的变化曲线图,图乙表示某植物细胞的部分细胞结构和相关代谢情况,c-h指的是O2或CO2。请据图回答:
甲表示两种不同的植物(阳生植物和阴生植物)随着日光照射强度的变化,吸收CO2量与放出CO2量的变化曲线图,图乙表示某植物细胞的部分细胞结构和相关代谢情况,c-h指的是O2或CO2。请据图回答:
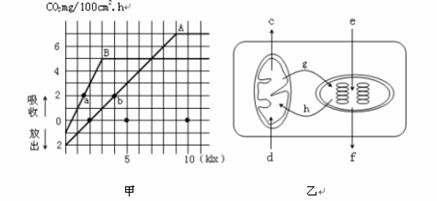
(1) 曲线B所表示的是 植物的光强度和光合作用合成量的关系。
(2) 假设B植物光合作用产生的有机物都是葡萄糖, B植物在光照强度为10千勒克斯(klx)时,总的光合速度的值是C6H12O6 mg/100cm2.h。
(3)甲图中,A、B两种植物处于光照强度为10千勒克斯(klx)时,指出乙图对应的c-h过程中能发生的是: 。只发生c、d过程时所进行的反应式为_______________________
(4)白天和黑夜的时间各为12 h,在 千勒克斯以上的光照强度下才能使A植物一天内吸收的CO2量超过放出的CO2量,B植物白天在1千勒克斯的光照强度下,一昼夜中植物能否生长?为什么?
(5)图乙中的h若指的是葡萄糖,图示还正确吗?为什么?
(6)细胞作为一个基本的生命系统,需要外界的能量供应,而光合作用和呼吸作用是物质和能量转变的两个重要生理过程。从能量输入叶肉细胞到能被生命活动所直接利用,其能量转移的具体途径是光能 → → → 。
14.某同学通过以下步骤测出了从一 定高度落下的排球对地面的冲击力:将一张白纸铺在水平地面上,把排球在水里弄湿,然后让排球从规定的高度自由落下,并在白纸上留下球的水印。再将印有水印的白纸铺在台秤上,将球放在纸上的水印中心,缓慢地向下压球,使排球与纸接触部分逐渐发生形变直至刚好遮住水印,记下此时台秤的示数即为冲击力的最大值。下列物理学习或研究中用到的方法与该同学的方法相同的是 ( )
定高度落下的排球对地面的冲击力:将一张白纸铺在水平地面上,把排球在水里弄湿,然后让排球从规定的高度自由落下,并在白纸上留下球的水印。再将印有水印的白纸铺在台秤上,将球放在纸上的水印中心,缓慢地向下压球,使排球与纸接触部分逐渐发生形变直至刚好遮住水印,记下此时台秤的示数即为冲击力的最大值。下列物理学习或研究中用到的方法与该同学的方法相同的是 ( )
A.建立“合力与分力”的概念
B.建立“点电荷”的概念
C.建立“瞬时速度”的概念
D.研究加速度与合力、质量的关系
15. 如图所示,跳水运动员最后踏板的过程可以简化为下述模型:运动
如图所示,跳水运动员最后踏板的过程可以简化为下述模型:运动
员从高处落到处于自然状态的跳板(A位置)上,随跳板一同向下
做变速运动到达最低点(B位置)。对于运动员从开始与跳板接触到
运动至最低点的过程,下列说法中正确的是 ( )
A.运动员到达最低点时,其所受外力的合力为零
B.在这个过程中,运动员的动能一直在减小
C.在这个过程中,运动员的机械能先增加后减少
D.在这个过程中,运动员所受重力对他做的功小于跳板的作用力对他做的功
16.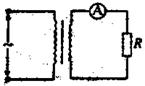 如图所示,理想变压器原线圈通入交流电流
如图所示,理想变压器原线圈通入交流电流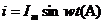 ,副
,副
线圈接有一电流表,与负载电阻串联,电流表的读数为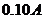 ,
,
在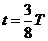 时,原线圈中电流的瞬时值为0.03
时,原线圈中电流的瞬时值为0.03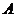 ,由此可知该变
,由此可知该变
压器的原、副线圈的匝数比为 ( )
A.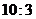 B.
B.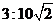 C.
C. 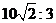 D.
D. 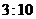
17.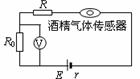 酒精测试仪用于机动车驾驶人员是否酗酒及其他严禁酒后作业人员的现场检测。它利用的是一种二氧化锡半导体型酒精气体传感器,酒精气体传感器的电阻随酒精气体浓度的变化而变化,在如图所示的电路中,不同的酒精气体浓度对应着传感器的不同电阻,这样,电压表的指针就与酒精气体浓度有了对应关系。如果二氧化锡半导体型酒精气体传感器电阻的倒数与酒精气体的浓度成正比,那么,电压表示数U与酒精气体浓度c之间的对应关系正确的是 ( )
酒精测试仪用于机动车驾驶人员是否酗酒及其他严禁酒后作业人员的现场检测。它利用的是一种二氧化锡半导体型酒精气体传感器,酒精气体传感器的电阻随酒精气体浓度的变化而变化,在如图所示的电路中,不同的酒精气体浓度对应着传感器的不同电阻,这样,电压表的指针就与酒精气体浓度有了对应关系。如果二氧化锡半导体型酒精气体传感器电阻的倒数与酒精气体的浓度成正比,那么,电压表示数U与酒精气体浓度c之间的对应关系正确的是 ( )
A.U越大,表示c越大,c与U成正比
B.U越大,表示c越大,但是c与U不成正比
C.U越大,表示c越小,c与U成反比
D.U越大,表示c越小,但是c与U不成反比
18.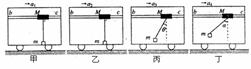 一辆小车静止在水平地面上,bc是固定在车上的一根水平杆,物块M穿在杆上,M通过细线悬吊着小物体m,m在小车的水平底板上,小车未动时细线恰好在竖直方向上。现使小车如下图分四次分别以
一辆小车静止在水平地面上,bc是固定在车上的一根水平杆,物块M穿在杆上,M通过细线悬吊着小物体m,m在小车的水平底板上,小车未动时细线恰好在竖直方向上。现使小车如下图分四次分别以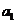 ,
,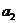 ,
,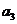 ,
,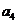 向右匀加速运动,四种情况下M、m均与车保持相对静止,且图甲和图乙中细线仍处于竖直方向,已知
向右匀加速运动,四种情况下M、m均与车保持相对静止,且图甲和图乙中细线仍处于竖直方向,已知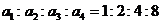 ,M受到的摩擦力大小依次为
,M受到的摩擦力大小依次为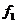 ,
,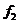 ,
,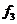 ,
,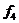 ,则( )
,则( )
A.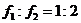 B.
B.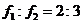 C.
C.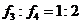 D.tanα=2tanθ
D.tanα=2tanθ
19.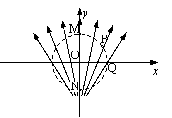 如图所示,一簇电场线的分布关于y轴对称,O是坐标原点,
如图所示,一簇电场线的分布关于y轴对称,O是坐标原点,
M、N、P、Q是以O为圆心的一个圆周上的四个点,其中
M、N在y轴上,Q点在x轴上,则 ( )
A.M点的电势比P点的电势低
B.O、M间的电势差小于N、O间的电势差
C.一正电荷在O点时的电势能小于在Q点时的电势能
D.将一负电荷由M点移到P点,电场力做负功
20.甲、乙两物体在同一水平轨道上,一前一后相距S,乙在前,甲在后,某时刻两者同时开始运动,甲做初速度为v0,加速度为a1的匀加速运动,乙做初速度为零,加速度为a2的匀加速运动,假设甲能从乙旁边通过,下述情况可能发生的是 ( )
A.a1=a2,可能相遇一次 B.a1<a2,可能相遇二次
C.a1>a2,可能相遇二次 D.a1<a2,只能相遇一次
21.某游乐场开发了一个名为“翻天滚地”的游乐项目。原理图如图所示:一个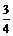 圆弧形光滑圆管轨道ABC,放置在竖直平面内,轨道半径为R,在A 点与水平地面AD相接,地面与圆心O等高,MN 是放在水平地面上
圆弧形光滑圆管轨道ABC,放置在竖直平面内,轨道半径为R,在A 点与水平地面AD相接,地面与圆心O等高,MN 是放在水平地面上 长为3R、厚度不计的减振垫,左端M正好位于A点.让游客进入一个中空的透明弹性球,人和球的总质量为m,球的直径略小于圆管直径。将球(内装有参与者)从A处管口正上方某处由静止释放后,游客将经历一个“翻天滚地”的刺激过程。
长为3R、厚度不计的减振垫,左端M正好位于A点.让游客进入一个中空的透明弹性球,人和球的总质量为m,球的直径略小于圆管直径。将球(内装有参与者)从A处管口正上方某处由静止释放后,游客将经历一个“翻天滚地”的刺激过程。 不考虑空气阻力.那么以下说法中错误的是 ( )
不考虑空气阻力.那么以下说法中错误的是 ( )
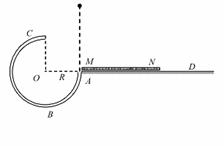
A.要使球能从C点射出后能打到垫子上,则球经过C点时的速度至少为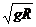
B.要使球能从C点射出后能打到垫子上,则球经过C点时的速度至少为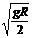
C.若球从C点射出后恰好能打到垫子的M端,则球经过C点时对管的作用力大小为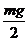
D.要使球能通过C点落到垫子上,球离A点的最大高度是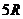
II卷(非选择题、本卷共14题。)
13.观察下列几个装置示意图,有关叙述正确的是 ( )
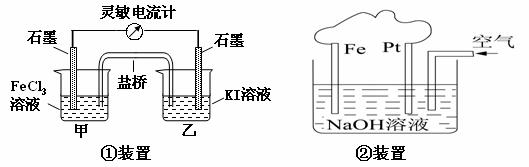
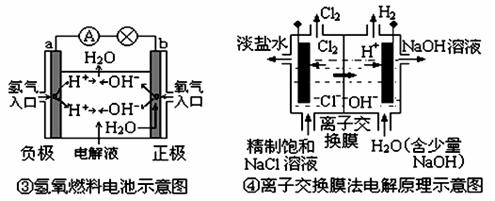
A.①装置的总反应为2Fe3++2I-=2Fe2++I2[来源:]
B.②装置中Fe为阴极,电极反应为 Fe-2e -+ 2OH-=Fe(OH)2
-+ 2OH-=Fe(OH)2
C.③装置中外电路电子由b极流向a极
D.④装置的离子交换膜允许阳离子、阴离子、水分子自由通过
12.下列离子方程式正确的是 ( )
A.Ag2S沉淀溶解平衡表达式:Ag2S  2Ag+ + S2-
2Ag+ + S2-
B.硫代硫酸钠溶液和稀硫酸反应:SO42--+S2O32-+6H+=3SO2↑+3H2O
C.碳酸氢钠溶液与足量的氢氧化钡溶液混合:HCO3-+Ba2++OH- = BaCO3↓+H2O
D.酸性高锰酸钾与草酸反应:MnO4-+H2C2O4+2H+=MnO2+2CO2↑+2H2O
11.NA代表阿伏加德罗常数的值,下列说法正确的是 ( )
A.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
B.pH=2、体积为1L的醋酸溶液中含醋酸分子的数目为0.01NA
C.7.8g Na2O2 晶体中阴、阳离子总数为0.3NA
D.常温常压下,17g甲基(-14CH3)所含的中子数为9NA
10.某合作小组讨论辨析以下说法不正确的是 ( )
A.粗盐和酸雨都是混和物
B.沼气和水煤气都是可再生能源
C.不锈钢和目前流通的硬币都是合金
D.豆浆和雾都是胶体
9.某烃含碳、氢原子物质的量之比为1∶2,该烃对氮气的相对密度为2,该烃可使溴水褪色,该烃与氢气加成的产物的二氯代物有三种同分异构体.该烃为 ( )
A.CH2=CH-CH2-CH3
B.CH2=CH-CH3
C.CH2=C(CH3)2
D.环丁烷
8.有关下列说法正确的是 ( )
①由乙烯制取1,2-二氯乙烷属于加成反应
②葡萄糖和蔗糖都属于糖类,它们互为同系物
③将铜丝在空气中灼烧变黑后,插入到乙醇中铜丝又变红
④油脂中的碳链含碳碳双键时,主要是高沸点的脂肪
⑤酯在碱性条件下的水解反应叫皂化反应
A.①③⑤ B.①③ C.①④⑤ D.②③⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com