
4.工业上利用氢气在氯气中燃烧,所得产物再溶于水的方法制得盐酸,流程复杂且造成能量浪费。有人设想利用原电池原理直接制盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是
A.两极材料都用石墨,用稀盐酸做电解质溶液
B.通入氢气的电极为原电池的正极
C.电解质溶液中的阳离子向通氯气的电极移动
D.通氯气的电极反应式为Cl2+2e-=2Cl―
3.下列叙述中正确的是
A.氯碱工业中,阳极放出氢气、阴极放出氯气
B.将钢铁与电源的正极相连可以起到保护钢铁的作用
C.用电解法精炼粗铜时,粗铜作阴极,纯铜作阳极
D.电镀时,应把镀件置于电解槽的阴极,电镀液应含有镀层金属的阳离子
2.关于下列装置说法正确的是
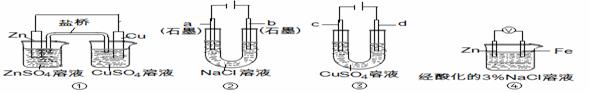
A.装置①中,盐桥中的K+移向ZnSO4溶液
B.装置②工作一段时间后,a极附近溶液的pH增大
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,装置中有Fe2+生成
1.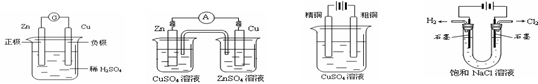 下图有关电化学的示意图正确的是
下图有关电化学的示意图正确的是
A. B. C. D.
2.市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li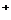 的高分子材料。这种锂离子电池的电池反应为: Li+2Li
的高分子材料。这种锂离子电池的电池反应为: Li+2Li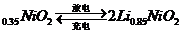
下列说法不正确的是
A.放电时,负极的电极反应式:Li-e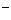 =Li
=Li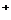
B.充电时,Li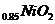 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
 C.该电池不能用水溶液作为电解质
C.该电池不能用水溶液作为电解质
D.放电过程中Li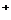 向负极移动
向负极移动
[解析]A项,Li从零价升至正价,失去电子,作为负极,正确;B项,反应逆向进行时。反应物只有一种,故化合价既有升,又有降,所以既发生氧化反应又发生还原反应,正确;C项,由于Li可以与水反应,故应为非水材料,正确;D项,原电池中阳离子应迁移至正极失电子,故错。答案D。
[随堂训练][1-8为单选,9-10为双选]
1.下列叙述中正确的是
A.构成原电池正极和负极的材料必须是两种金属。
B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极。
C.马口铁(镀锡铁)破损时与电解质溶液接触锡先被腐蚀。
D.铜锌原电池工作时,若有13克锌被溶解,电路中就有0.4mol电子通过。
 [解析] 两种活动性不同的金属与电解质溶液能够组成原电池,但不能因此说构成原电池电极的材料一定都是金属,例如锌和石墨电极也能跟电解质溶液组成原电池。在原电池中,活动金属中的电子流向不活动的电极,因此活动金属是负极。镀锡铁表皮破损后与电解质溶液组成原电池,铁较锡活泼,铁先失电子被腐蚀。铜锌原电池工作时,锌负极失电子,电极反应为Zn –2e==Zn2+,1molZn失去2mol电子,0.2mol锌(质量为13克)被溶解电路中有0.4mol电子通过。故选D
[解析] 两种活动性不同的金属与电解质溶液能够组成原电池,但不能因此说构成原电池电极的材料一定都是金属,例如锌和石墨电极也能跟电解质溶液组成原电池。在原电池中,活动金属中的电子流向不活动的电极,因此活动金属是负极。镀锡铁表皮破损后与电解质溶液组成原电池,铁较锡活泼,铁先失电子被腐蚀。铜锌原电池工作时,锌负极失电子,电极反应为Zn –2e==Zn2+,1molZn失去2mol电子,0.2mol锌(质量为13克)被溶解电路中有0.4mol电子通过。故选D
21.(本小题满分13分)
已知点F1,F2为椭圆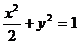 的两个焦点,点O为坐标原点,圆O是以F1,F2为直径的圆,一条直线
的两个焦点,点O为坐标原点,圆O是以F1,F2为直径的圆,一条直线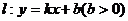 与圆O相切并与椭圆交于不同的两点A,B。
与圆O相切并与椭圆交于不同的两点A,B。
(1)设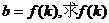 的表达式;
的表达式;
(2)若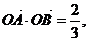 求直线
求直线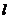 的方程;
的方程;
(3)若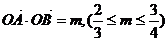 ,求三角形OAB面积的取值范围。
,求三角形OAB面积的取值范围。
20.(本小题满分13分)
已知函数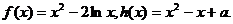
(1)求函数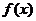 的极值;
的极值;
(2)设函数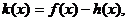 若函数
若函数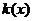 在[1,3]上恰有两个不同零点,求实数a的取值范围。
在[1,3]上恰有两个不同零点,求实数a的取值范围。
19.(本小题满分13分)
某种有奖销售的饮料,瓶盖内印有“奖励一瓶”或“谢谢购买”字样,购买一瓶若其瓶盖内印有“奖励一瓶”字样即为中奖,中奖概率为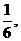 甲、乙、丙三位同学每人购买一瓶该饮料。
甲、乙、丙三位同学每人购买一瓶该饮料。
(1)求甲中奖且乙、丙都没有中奖的概率;
(2)求中奖人数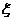 的分布列及数学期望
的分布列及数学期望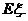
18.(本小题满分13分)
已知向量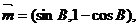 且与向量
且与向量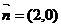 所成角为
所成角为 ,其中A,B,C是
,其中A,B,C是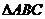 的内角。
的内角。
(1)求角B的大小;
(2)求 的取值范围。
的取值范围。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com