
9.下列实验方案设计中,可行的是
A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铁粉
B.用萃取的方法分离汽油和煤油
C.用溶解和过滤的方法分离硝酸钾和氯化钠固体混合物
D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
8.配制100 mL浓度为0.5mol/L CuSO4溶液过程中,下列部分实验操作正确的是
A.称取8.0g CuSO4固体放入烧杯中,加入100 mL蒸馏水,并不断搅拌至固体溶解
B.称取8.0g CuSO4固体,放入100 mL容量瓶中,加入蒸馏水使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
C.称取8.0g CuSO4固体,放入100 mL量筒中,加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL
D.称取12.5g CuSO4.5H2O固体放入烧杯中,加入适量蒸馏水溶解,冷却后将烧杯中溶液注入100 mL容量瓶后,用少量蒸馏水洗涤烧杯内壁2-3次
7.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.17g氨气中所含原子数为NA
B.标准状况下,1 L水中所含分子数为NA
C.常温常压下,16 g O2含有的氧原子数为NA
D.0.3 mol /L的MgCl2溶液中含Cl-数目0.6 NA
6.从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是
A.氧化铜和硝酸反应 B.铜和稀硝酸反应
C.铜和浓硝酸反应 D.氯化铜和硝酸银反应
5.下列离子方程式书写正确的是
A.硅酸钠和盐酸反应: Na2SiO3+2H+=H2SiO3↓+2Na+
B.铁与稀硝酸反应:2Fe+6H+=2Fe3++3H2↑
C.硫酸与氢氧化钡反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.氯化铁溶液与铜反应:2Fe3++Cu=2Fe2++Cu2+
4.如果长期敞口放置下列各物质,其中不会变质的是
A.过氧化钠 B.氯化钠 C.漂白粉 D.新制氯水
3.我国重点城市近年来已发布“空气质量日报”。下列物质中不列入首要污染物的是
A.二氧化硫 B.二氧化氮 C.二氧化碳 D.可吸入的颗粒物
2.光导纤维被认为是20世纪最伟大的发明之一,它使信息高速公路在全球迅猛发展,它的发明者是被誉为“光纤之父”的华人科学家高锟。光导纤维的主要成分是
A.CaCO3 B.SiO2 C. Si D. SiC
1.进行化学实验必须注意安全。下列说法正确的是
A.不能用手直接接触药品
B.剩余的药品倒入水池
C.用鼻孔凑到容器口去闻气体的气味
D.尝一下实验室酒精的味道
25.(2010贵州铜仁,25,14分)如图所示,矩形OABC位于平面直角坐标系中,AB=2,OA=3,点P是OA上的任意一点,PB平分∠APD,PE平分∠OPF,且PD、PF重合.
(1)设OP=x,OE=y,求y关于x的函数解析式,并求x为何值时,y的最大值;
(2)当PD⊥OA时,求经过E、P、B三点的抛物线的解析式;
(3)
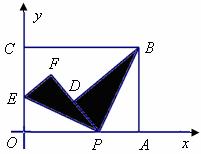

[答案]解:(1)由已知PB平分∠APD,PE平分∠OPF,且PD、PF重合,则∠BPE=90°.
∴∠OPE+∠APB=90°.又∠APB+∠ABP=90°,∴∠OPE=∠PBA.
∴Rt△POE∽Rt△BPA.
∴ .即
.即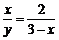 .∴y=
.∴y=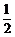 x(3-x)=-
x(3-x)=-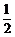 x2+
x2+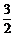 x(0<x<3).
x(0<x<3).
且当x=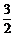 时,y有最大值
时,y有最大值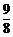 .
.
(2)由已知,△PAB、△POE均为等腰三角形,可得P(1,0),E(0,1),B(3,2).
设过此三点的抛物线为y=ax2+bx+C,则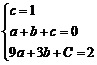 ∴
∴
∴y=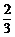 x2-
x2- x+1.
x+1.
(3)由(2)知∠EPB=90°,即点M与点B重合时满足条件.
直线PB为y=x-1,与y轴交于点(0,-1).
将PB向上平移2个单位则过点E(0,1),
∴该直线为y=x+1.
由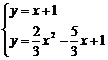 得
得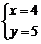 ∴M(4,5).
∴M(4,5).
故该抛物线上存在两点M(3,2),(4,5)满足条件.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com