
26.下表中物质的分类组合完全正确的是( )
|
编号 |
A |
B |
C |
D |
|
强电解质 |
Ba(OH)2 |
盐酸 |
HClO4 |
BaSO4 |
|
弱电解质 |
HI |
CaCO3 |
HClO |
NH3·H2O |
|
非电解质 |
SO2 |
NH3 |
Cl2 |
乙醇 |
25.根据下列四个反应方程式判断:氧化性由强到弱的顺序正确的是( )
①2 A-+B 2 ==== 2 B-+A 2 ②2 A-+C 2 ==== 2 C-+A 2
③2 B-+C 2 ==== 2 C-+B 2 ④2C-+D 2 ==== 2 D-+C2
A.D 2>C 2>B 2>A 2 B.A 2>B 2>C 2>D 2
C.C2>A 2>B 2>D 2 D.B 2>D 2>C 2>A 2
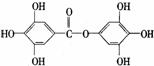
24.已知A物质的分子结构简式如下: , lmol A与足量的
NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
A.6mol B.7mol
C.8mo1 D.9mo1
23.0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度大小顺序正确的是( ) 
A.c(Na+)>c(Cl-)>c(OH-)>c(H+) B.c(Na+)=c(Cl-)>c(H+)>c(OH-)
 C.c(Na+)=c(Cl-)>c(OH-)>c(H+) D. c(Cl-)>c(Na+)>c(OH-)>c(H+)
C.c(Na+)=c(Cl-)>c(OH-)>c(H+) D. c(Cl-)>c(Na+)>c(OH-)>c(H+)
22.在由水电离产生的H+浓度为1×10-13mol/L的溶液中,一定能大量共存的离子组是( )
① K+、Cl-、NO3-、S2- ② K+、Fe2+、I-、SO42- ③ Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HCO3- ⑤ K+、Ba2+、Cl-、NO3-
A.①③ B.③⑤ C.③④ D.②⑤

21.已知NaHSO4在水中的电离方程式为:NaHSO4 = Na++H++SO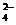 。某温度下,向pH=6
。某温度下,向pH=6
的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃

B.由水电离出来的H+的浓度是1.0×10-10mol/L
C.加入NaHSO4晶体抑制了水的电离
D.该温度下加入等体积pH = 12的NaOH溶液可使该溶液恰好呈中性
20.意大利科学家合成一种新型氧分子,它由4个氧原子构成,专家认为它液化后的能量、
密度都比普通氧分子高得多,下列关于该分子叙述正确的是( )
A.它是氧元素的另一种同位素 B.它是氧元素的另一种同素异形体
C.它的摩尔质量是64 D.它将成为一种新型强力火箭推进燃料
19.在一种无色溶液中,可能存在Na+、Ca2+、Fe3+、Br-、CO32-、SO42-、Cl-中的几种。某学生进行了下列实验:取少量原溶液,向其中滴加足量氯水,有无色无味气体产生,溶液仍为无色;将反应后的溶液分为2份,向其中一份溶液中滴加AgNO3溶液,有白色沉淀产生;向另一份溶液中加BaCl2溶液,有白色沉淀产生。该溶液中一定大量存在的离子组是( )
A.Na+、Fe3+、SO42-、
B.CO32-、Cl-、SO42-
C.Ca2+、Br-、SO42-
D.Na+、SO42-、CO32-

18.用特殊方法把固体物质加工到纳米级(1-100nm,1nm=10-9m)的超细粉末粒子,然后制
得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A.溶液 B.悬浊液 C.胶体 D.乳浊液
17.下列实验中操作及现象与结论对应关系正确的一组是(
) 
|
|
实验操作 |
实验现象 |
实验结论 |
|
A |
适量二氧化碳通入氯化钡溶液中 |
产生白色沉淀 |
碳酸的酸性比盐酸弱 |
|
B |
二氧化硫通入溴水中 |
溶液褪色 |
二氧化硫有漂白性 |
|
C |
取少量某无色溶液,先滴加氯水,再加入少量四氯化碳,振荡、静置 |
溶液分层,下层呈紫红色 |
原无色溶液中一定有碘离子 |
|
D |
淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 |
产生红色沉淀 |
淀粉水解可生成葡萄糖 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com