
23.(12分)为研究铁质材料与热浓硫酸的反应,某小组进行了以下探究活动:
[探究一]
(1)称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分应后得到溶液X并收 集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为____(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KmnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4
然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y 中SO2的体积分数为____。
[探究二]
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
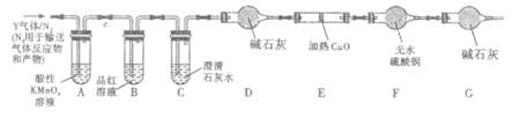
(2)写出产生CO2的化学方程式___ _。
(3)装置A中试剂的作用是____ 。
(4)简述确认气体Y中含有CO2的实验现象 。
(5)如果气体Y中含有H2,预计实验现象应是 。
22.(8分)链烃A不能使溴的CC14溶液褪色,1mol A完全燃烧消耗6.5mol O2,B、C均是 A的一氯代物,A~I有如下转化关系:
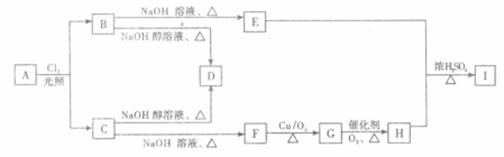
回答下列问题:
(1)D的名称 。
(2)写出下列转化的化学方程式:
F→C: 。
E+H→I: 。
(3)B→E的反应类型是 。
(4)H有多种同分异构体。写出满足下列两个条件的同分异构体的结构简式(只要求写出其中二个):
①分子结构中有羟基,且只有一个甲基。
②与新制Cu(OH)2共热生成红色沉淀。
21.(8分)A-N是中学化学中常见的单质及化合物,A、B、F三种分子中的电子总数相同,A、C、D均为可燃性气体,B为无色液体;D、E、G、J、M为单质,其中J为黑色粉末,M为中学常见的金属,N可用作耐高温材料。各物质间存在下列转化关系(部分产物略去):
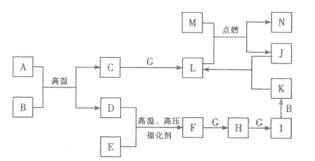
请回答下列问题:
(1)B的电子式为
(2)写出M与L反应的化学方程式____
(3)写出加热条件下J与K的浓溶液反应的化学方程式
(4)简述实验室保存K的浓溶液的方法 。
10.(9分)甲、乙、丙、丁是原子序数不超过20的元素组成的物质(单质或化合物),且存在如下转化关系:甲+乙一丙+丁。依次回答下列问题:
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水时:
 ①若丙为可燃性气体,分子的空间构型为直线形结构。写出实验室制备丙的化学 方程式
。
①若丙为可燃性气体,分子的空间构型为直线形结构。写出实验室制备丙的化学 方程式
。
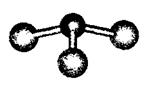
②若甲是由N和Cl元素组成的化合物,其分子球棍
模型如右图所示,丙具有漂白性。则甲中Cl元素的化
合价是 。
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水时:
①若甲可用于防毒面具、潜艇等常用的供氧剂,写出发生反应的化学方程式
。
②若丙和丁都是可燃性气体,其中丙是工业炼铁过程中还原剂。写出甲+乙→+丙+丁的化学方程式____ 。
③若甲是由N和0元素组成的气态物质,呈红棕色。将3. 36 g Fe加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是 (用一个离子方程式表示)。
19. (9分)在t cI二时,向容积为2L的密闭容器甲中加入1mol A气体、3mol B气体及少量 固体催化剂,发生下列反应:A(g)+3B(g)
2C(g);△H <0,10min后各物质的浓度不再变化,测得气体C的体积分数为25%。请填空:
(9分)在t cI二时,向容积为2L的密闭容器甲中加入1mol A气体、3mol B气体及少量 固体催化剂,发生下列反应:A(g)+3B(g)
2C(g);△H <0,10min后各物质的浓度不再变化,测得气体C的体积分数为25%。请填空:
(1)计算该反应在0-10min时间内,B的平均反应速率为= ,A的转化率为= 。
(2)在T1℃时,若起始在容器甲中只加人1.0 mol C,则达到平衡时c的体积分数
(填选项字母)。
a.大于25% b.等于25% c.小于25%
(3)右图分别表示的是在T1℃和T2℃时,密闭容器甲中气B的
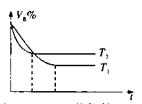 体积分数随时间变化的曲线。试判断T1
T2
体积分数随时间变化的曲线。试判断T1
T2
(填“>”、“<”或“=”),理由是 。
(4)若保持t℃,在体积也为2L的密闭容器乙中通人一定量的
A、B、C三种气体,欲使平衡时容器乙中各物质的物质的
量与容器甲中完全相同,且起始时反应向正反应方向进行,
则通入B的物质的量x的取值范围是 。
18.m g铝镁合金与一定浓度的稀硝酸恰好完全反应(假定质子交
换膜硝酸的还原产物只有N0)o向反应后的混合溶液中滴加
a mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰
好为最大值n g,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(n-m)g
②恰好溶解后溶液中的NOf离子的物质的量为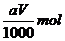
③反应过程中转移的电子的物质的量为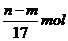
④生成NO气体的体积室温下为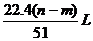
⑤与合金反应的硝酸的物质的量为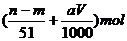
A.2项 B.3项 C.4项 D.5项
第Ⅱ卷(非选择题,共46分)
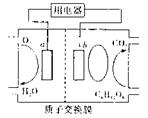
17.以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
( )
 A.该电池能够在高温下工作
A.该电池能够在高温下工作
B.放电过程中,图中0为电池的负极,6为正极
C.放电过程中,H。从正极区向负极区迁移
D.电池的负极反应为:C6H12O6+6H2O-24e-→6CO2↑+24H+
16.下列有关化学研究的正确说法是 ( )
A.同时改变两个变量来研究反应速率的变化,能更快得出有关规律
B.对于同一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的
C.依据丁达尔效应可将分散系分为溶液、胶体与浊液
D.从HF、HCI、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律
15.在测定中和热的实验中,下列说法中正确的是 ( )
A.该实验需要用的主要玻璃仪器有:两个大小相同的烧杯、两只大小相同的量筒、温
度计、环形玻璃搅拌棒
B.不能用保温杯代替烧杯做有关测定中和热的实验
C.该实验至少需要测定并记录温度的次数是6次
D.若NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高
13.火法炼铜过程中发生下列反应:3Cu2S+2O2 6Cu+3SO2。下列说法不军确的是( )
A.Cu2S只做还原剂
B.氧化剂与还原剂的物质的量之比为2:1
C.1 mol Cu2S和O2反应生成2 molCu,转移电子的物质的量为6mol
D.反应消耗3 mol Cu2S时,被O2氧化的硫(S)的物质的量为2 mol
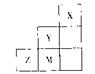 14.右图为元素周期表中短周期的一部分,关于推断Y、Z、M的说法正确的是 ( )
14.右图为元素周期表中短周期的一部分,关于推断Y、Z、M的说法正确的是 ( )
A.非金属性:Y>Z>M
B.离子半径:M- >Z2->Y-
C.ZM:分子中各原子的最外层均满足8电子稳定结构
D.三种元素中,Y的最高价氧化物对应的水化物酸性最强
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com