
23、空气中的SO2含量和可吸入颗粒的含量(可用g/cm3表示)都是重要的空气质量指标。在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02mg/L。
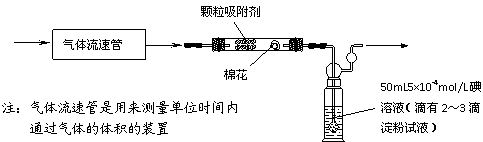 ⑴为测定某地方的空气中SO2和可吸入颗粒的含量,甲同学设计了如下图所示的实验装置:
⑴为测定某地方的空气中SO2和可吸入颗粒的含量,甲同学设计了如下图所示的实验装置:
应用上述装置测定空气中的SO2含量和可吸入颗粒的含量,除测定气体流速(单位:cm3/min)外,还需要测定
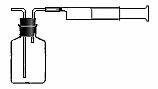 ⑵乙同学拟用下列简易装置测定空气中的SO2含量:准确移取50mL5×10-4mol/L的标准碘水溶液,注入右图所示广口瓶中,加2-3滴淀粉指示剂,此时溶液呈蓝色。在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n)。
⑵乙同学拟用下列简易装置测定空气中的SO2含量:准确移取50mL5×10-4mol/L的标准碘水溶液,注入右图所示广口瓶中,加2-3滴淀粉指示剂,此时溶液呈蓝色。在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止,记录抽气次数(n)。
①假设乙同学的测量是准确的,乙同学抽气的次数至少为 次,方可说明该地空气中的SO2含量符合排放标准。
②如果乙同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,请你对其可能的原因(假设溶液配制、称量或量取及各种读数均无错误)提出合理假设:_________________________________________________ __________。
③丙同学认为:乙同学的实验方案需要抽气的次数太多,操作麻烦。与乙讨论后,决定将抽气次数降到100次以下,请你设计合理的改进方案:
。
⑶改变合适的吸收液,乙同学使用的装置还可以测定新装修的居室空气中甲醛的浓度,吸收剂最好选用 (选填:①浓硫酸、②银氨溶液、③新制的氢氧化铜、④酸化的高锰酸钾溶液)。
22、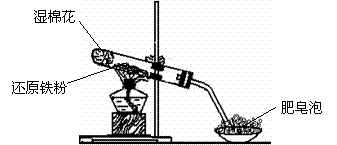 某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是 ,若溶液未变红色则说明硬质试管中固体物质的成分是 。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:
(用离子方程式表示)。
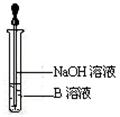 (4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程
式:
。
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有 性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是 ,并且配制含Fe2+的盐溶液时应加入少量 。
21、固体A、B都由两种相同的元素构成。在A、B中两种元素的原子个数比分别为1:1和1:2。将A和B在高温时煅烧,产物都是 C(固体)和D(气体)。由D最终可制得E(酸),E和另一种酸组成混合液,常用于制取有机炸药。E的稀溶液和A反应,生成G(气体)和F(溶液),G通入D的水溶液,有浅黄色沉淀生成。在F中滴入溴水后,加入KOH溶液,有红褐色沉淀生成,该沉淀加热时又能转化为C。
根据以上事实回答:(1)A的化学式是 ,B的化学式是 。
(2)写出下列反应的化学方程式:
① B煅烧生成C和D 。
② G通入D溶液 。
③ 在F中滴入溴水 。
20、下列说法中,完全正确的一组是
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过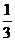 的试管加热至沸腾
的试管加热至沸腾
③等体积的浓氨水与蒸馏水混合后,其中氨水的溶质质量分数一定等于稀释前的一半
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤硝酸、溴水可长期盛放在棕色的滴瓶中
⑥将烧瓶放在桌上,再用力塞进塞子
⑦熔融氢氧化钠要在耐高温的石英坩埚中
⑧将滴管垂直伸进试管内滴加液体
A.①④ B.①④⑤⑦ C.②③⑤⑥ D.①②③④⑤⑥⑦⑧
第Ⅱ卷(非选择题,共50分)
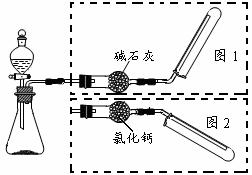
19、下图是实验室制取气体装置,其中发生装置相同(省去了铁架台和锥形瓶中的药品),干燥和收集装置有二套,分别用图一和图二。下列选项中不正确的是
|
A |
锌和稀盐酸 |
选用图1 |
|
B |
碳化钙和饱和食盐水 |
选用图1 |
|
C |
铜和浓硫酸 |
选用图2 |
|
D |
过氧化钠和水 |
选用图2 |
18、下列有关溶液配制说法错误的是
①.取58.5gNaCl固体放入1L水中充分溶解,所得溶液中NaCl的物质的量浓度为1mol•L-1
②.称取12.5g胆矾[CuSO4·5H2O]溶于水中, 并加水稀释至500mL, 所得溶液物质的量浓度为0.1mol•L-1
③.将100g 5%的食盐水加热蒸发掉50g水后, 所得溶液中NaCl的质量分数为10%
④.将浓度为2 mol•L-1的硫酸钠溶液10mL加水稀释至200mL, 所得溶液浓度为0.1mol•L-1
⑤.欲配制质量分数为10%的ZnSO4溶液,将10gZnSO4·7H2O溶解在90g水中
A. ①⑤ B. ①②⑤ C. ①②③⑤ D.①③④⑤
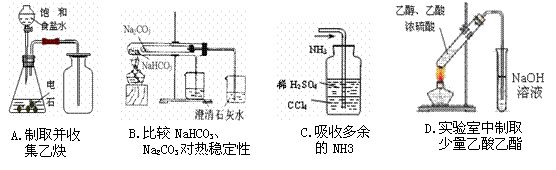
17、用下列实验装置完成对应的实验,能达到实验目的的是
16、化工厂厂址选择是一个复杂的问题,涉及原料、水源、能源、土地供应、市场需求、交通运输和环境保护等诸多因素的制约,硫酸厂应建在
①靠近原料产地,远离消费中心 ②靠近消费中心,稍偏离原料产地 ③交通便利,人口稠密的居民区 ④建在环保要求高的地区,便于“三废”的治理
A.①②③④ B.①③④ C.①②④ D.只有②
15、下列实验中,有关仪器的下端必须插入液面以下的是
①制备乙烯时用的温度计;②制备氯气装置中的分液漏斗;③制取氨水时氨气溶于水的导管;④制备氢气的简易装置中加入稀硫酸用的长颈漏斗;⑤分馏石油时的温度计;⑥制备乙酸乙酯时,将乙酸乙酯蒸气通入饱和Na2CO3溶液的导管。
A.①④ B.①②④ C.①②③⑥ D.①②③④
14、下列实验能证明有SO2存在的是(1)能使澄清石灰水变浑浊 (2)能使湿润的蓝色石蕊试纸变红 (3)能使品红溶液褪色 (4)通入足量的NaOH溶液中,再滴加BaCl2溶液有白色沉淀生成,该沉淀能溶于盐酸。 (5)通入Br2水中能使Br2水褪色,再加Ba(NO3)2溶液有白色沉淀。
A.都能证明 B.都不能证明 C.(3)(4)(5)能证明 D.只有(5)能证明
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com