
23、(6分)右图是某温度时,在容
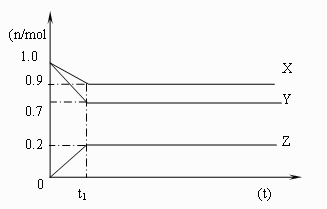 积为1L的容器中X、Y、Z三
积为1L的容器中X、Y、Z三
种物质的物质的量随时间的变
化曲线,根据图中的曲线变化
情况可知:
(1)t1点表示的意义是:
(2)t1时刻之前各物质的浓度变化情况:
(3)试写出该反应的化学方程式:
22、(10分)实验室中制备氯气的原理是:MnO2和浓盐酸,在加热的条件下反应原理方程式:MnO2 + 4HCl(浓) 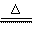 MnCl2
+ Cl2↑+ 2H2O
MnCl2
+ Cl2↑+ 2H2O
分析回答下列问题:
(1)该反应属于离子反应,请写出该反应的离子方程式:
(2)从化合价变化的角度分析,该反应属于氧化-还原反应,其中,氧化剂是 、还原剂是 、氧化产物是 、还原产物是
(3)根据上述反应方程式得知,当有4molHCl参加反应时,有 molHCl发生氧化反应,生成 molCl2。
(4)比较Cl2和空气的密度大小 ,你的理由是:
,
所以,如果采用排空取气法收集气体,应当采用 。
21、(5分)锌锰干电池是用锌制圆筒为外壳,石墨碳棒上盖铜冒在中央,筒中填充NH4Cl和淀粉糊作为电解质,同时还填入MnO2和炭黑,故称为锌锰干电池。回答下列问题:
(1)判断该电池的正负极:
正极: 、负极:
(2)电池的总反应式为:Zn+2NH4++2MnO2=Zn2++2NH3+Mn2O3+H2O
则两个电极的电极反应式分别是:
正极: 、负极:
(3)该类电池用久了会变形外鼓、漏液,请解释:
20、在1L浓度为c mol/L的弱酸HA中,HA、A-和H+的物质的量之和为nc mol,
则HA的电离度是 ( )
A、100n% B、c/n×100% C、100(n-1)% D、n%
山东省新泰市高三开学考试
化 学 试 题
第Ⅱ卷 非选择题部分(50分)
19、下列说法中正确的是 ( )
A、所有的物质都存在化学键
B、在同一个分子中所有的原子之间都存在化学键
C、没有化学键就不会存在化合物
D、化学反应中,不一定破坏化学键
18、将铁钉和碳棒用导线连接后,同时浸入0.01mol/L的NaCl溶液中,可能发生的反应是 ( )
A、碳棒上放出氢气 B、碳棒附近产生OH-
C、碳棒上放出氧气 D、铁钉被氧化
16、X、Y、Z、R分别代表四种元素,若aXm+ bYn+ cZn- dRm- 四种离子
的核外电子排布相同,且m>n,则下列关系不正确的是 ( )
A、a-c=m-n B、b-d=m+n C、a>b>d>c D、a>b>c>d
15、向一定浓度的下列物质的澄清溶液中通入过量的CO2气体,最后可能会有沉淀生成的是 ( )
A、Ca(OH)2 B、Na2CO3 C、CaCl2 D、苯酚钠
14、下列说法正确的是 ( )
A、溶液一定都是混合物 B、含氧元素的化合物都是氧化物
C、纯净物都能用化学式表示 D、只含有一种元素的物质一定是纯净物
12、下列说法中正确的是 ( )
A、在氧化-还原反应中,不一定所有元素的化合价都发生变化
B、非金属单质在氧化-还原反应中一定作氧化剂
C、化合反应和复分解反应不可能是氧化-还原反应
D、置换反应中,做为生成物的单质一定是还原产物

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com