
5.下列有关晶体的叙述中错误的是 ( )
A.离子晶体中,一定存在离子键 B.原子晶体中,一定存在共价键
C.金属晶体的熔沸点均很高 D.稀有气体能形成分子晶体
4.下列说法错误的是 ( )
A.油脂在碱性条件下水解生成甘油和高级脂肪酸盐
B.苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应
C.蛋白质在酶的催化作用下水解的最终产物为氨基酸
D.淀粉和纤维素水解最终产物都是葡萄糖
3. 在通常条件下,下列各组物质的性质排列不正确的是( )
A.熔点:CO2<KCl<SiO2 B.沸点:乙烷>戊烷>2-甲基丁烷
C.密度:苯<水<1,1,2,2-四溴乙烷 D.热稳定性:HF>HCl>H2S
2.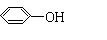 “5.12”汶川大地震后,没有出现大的疫情,各种消毒剂的作用功不可没。下列物质不能用作饮用水消毒剂的是(
)
“5.12”汶川大地震后,没有出现大的疫情,各种消毒剂的作用功不可没。下列物质不能用作饮用水消毒剂的是(
)
A.O3 B.ClO2 C.Cl2 D.
1.现代以石油化工为基础的三大合成材料是( )
①合成氨、②塑料、③合成盐酸、④合成橡胶、⑤合成尿素、⑥合成纤维、⑦合成洗涤剂 。
A.①③⑤ B.②④⑥ C.②④⑦ D.④⑤⑥
11.四种晶体的比较
|
|
离子晶体 |
原子晶体 |
分子晶体 |
金属晶体 |
|
构成 粒子 |
阴阳离子 |
原子 |
分子 |
金属阳离子和自由电子 |
|
粒子间 作用力 |
离子键 |
共价键 |
分子间作用力 |
金属键 |
|
熔沸点 |
较高 |
很高 |
低 |
一般较高,部分低 |
|
导电性 |
水溶液或熔融态均导电 |
不导电 (Si为半导体) |
不导电 |
电的良导体 |
|
溶解性 |
易溶于极性溶剂 |
难溶于任何溶剂 |
结构相似相溶 |
难溶于任何溶剂 |
|
溶化时 |
破坏离子键 |
破坏共价键 |
破坏分子间作用力或氢键 |
破坏金属键 |
|
溶解时 |
破坏离子键 |
不溶于水 |
破坏分子间作用力或氢键,可能破坏共价键 |
不溶于水 |
(1)在NH3、HF、H2O中存在特殊的分子间作用力(氢键),熔沸点反常的高。
(2)分子极性:极性键构成的非极性分子 CO2、CH4、CCl4、CS2、C2H4、C2H2、苯等。
 (3)物质的熔、沸点的比较
(3)物质的熔、沸点的比较
①一般规律:原子晶体>离子晶体>分子晶体。如:SiO2>NaCl>CO2(干冰)
②同属原子晶体,一般键长越短,键能越大,共价键越牢固,晶体的熔、沸点越高。如:金刚石>金刚砂>晶体硅
③同类型的离子晶体,离子电荷数越大,阴、阳离子核间距越小,则离子键越牢固,晶体的熔、沸点一般越高。如:MgO>NaCl
④分子组成和结构相似的分子晶体,一般分子量越大,分子间作用力越强,晶体熔、沸点越高。如:F2<Cl2<Br2<I2
⑤金属晶体:金属原子的价电子数越多,原子半径越小,金属键越强,熔、沸点越高。如:Na<Mg<Al
(4)根据物质在同条件下的状态不同。一般熔、沸点:固>液>气
 如果常温下即为气态或液态的物质,其晶体应属分子晶体(Hg除外)。如惰性气体,虽然构成物质的微粒为原子,但应看作为单原子分子。因为相互间的作用为范德华力,而并非共价键。
如果常温下即为气态或液态的物质,其晶体应属分子晶体(Hg除外)。如惰性气体,虽然构成物质的微粒为原子,但应看作为单原子分子。因为相互间的作用为范德华力,而并非共价键。
10.合成材料
 (1)关注本章第一节的“链节”、“聚合度”、“单体”等概念。
(1)关注本章第一节的“链节”、“聚合度”、“单体”等概念。
(2)线性结构的有机高分子:有热塑性,在有机溶剂中有一定的溶解性。
(3)体性结构的有机高分子:有热固性,不溶于有机溶剂。
(4)合成材料:塑料、合成纤维(棉花、羊毛、木材和草类都是天然纤维;合成纤维中,涤纶、锦纶、晴纶、丙纶、维纶、氯纶被称为“六大纶”)
(5)新型有机高分子材料:高分子膜;具有光、电、磁等特殊功能的高分子材料、生物高分子材料、医用高分子材料、隐身材料、液晶高分子材料。
9.糖类、油脂、蛋白质
(1)糖类、油脂、蛋白质、维生素、无机盐、水通称为营养素。
(2)糖类、油脂、蛋白质都是天然的有机化合物。
(3)蔗糖、麦芽糖、淀粉、纤维素水解的化学方程式。
(4)实验设计:加热淀粉、硫酸的混合液
①怎么验证淀粉是否发生了水解(注意要中和酸);②怎么验证淀粉是否完全水解。
(5)在规定范围内使用食品添加剂,一般认为对人体健康无害。
(6)硝酸纤维:属于硝酸酯,含氮量高的称为火棉,含氮量低的称为胶棉。
(7)醋酸纤维:属于醋酸酯。
(8)黏胶纤维:植物秸秆的富含纤维素的物质经过氢氧化钠和二硫化碳等处理后,得到的一种纤维状物质,黏胶纤维中的长纤维俗称人造丝,短纤维俗称人造棉。
(9)硬脂酸:C17H35COOH、软脂酸:C15H31COOH、油酸的分子式:C17H33COOH。
(10)肌肉、皮肤、发、毛、蹄、角等主要成分都是蛋白质。
(11)关注甘氨酸、丙氨酸、谷氨酸的结构。
(12)蛋白质的盐析:浓的无机盐,如硫酸氨、硫酸钠。盐析是可逆过程,用来分离、提纯蛋白质。
(13)蛋白质的变性:加热,紫外线,X射线,强酸、强碱,铅、铜、汞等重金属盐,以及一些有机化合物,如甲醛、酒精、苯甲酸等。变性是不可逆过程。
(14)颜色反应
8.烃的衍生物
(1)卤代烃水解、消去反应的化学方程式、卤离子的检验(注意要加硝酸酸化)
(2)乙醇可作车用燃料,是一种可再生能源。
(3)苯酚有毒,浓溶液对皮肤有强烈的腐蚀性,皮肤上的苯酚应立即用酒精洗涤。苯酚的稀溶液可直接用作防腐剂和消毒剂(如药皂)。
(4)醛与银氨溶液、新制Cu(OH)2反应的化学方程式。银氨溶液、新制Cu(OH)2的配制。
(5)甲醛又叫蚁醛,是无色、有刺激性气味的气体,35%-40%的甲醛水溶液叫做福尔马林。工业上,甲醛是重要的有机合成原料;农业上,甲醛可用作农药,用于制缓效肥料等。稀释的福尔马林溶液用于浸制生物标本。
(6)酯化反应的实验、反应方程式。
(7)酯的水解(酸性条件下是可逆反应,碱性条件下是不可逆反应)
7.烃
(1)乙烯是衡量一个国家石油化学工业水平的重要标志之一。
(2)乙炔是没有颜色、没有气味的气体,由电石产生的乙炔因常混有PH3H2S等杂质而有难闻的气味。可用氧炔焰来焊接或切割金属。
(3)苯是一种重要的化工原料,它用于生产合成纤维、合成橡胶、塑料、农药、医药,也可作有机溶剂。
 (4)溴苯是无色液体,密度大于水;硝基苯是一种带有苦杏仁味的、无色的油状液体,密度比水大,有毒。
(4)溴苯是无色液体,密度大于水;硝基苯是一种带有苦杏仁味的、无色的油状液体,密度比水大,有毒。
(5)石油主要是由各种烷烃、环烷烃和芳香烃组成的混合物。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com