
19、 (10分)右图所示转化关系中,A、E、G是分别由短周期元素形成的单质,且A元素的原子半径在短周期元素
(10分)右图所示转化关系中,A、E、G是分别由短周期元素形成的单质,且A元素的原子半径在短周期元素
中最大。在同周期元素形成的氧化物中,G的氧化物既可以和强酸反应,又可以和强碱反应。C在常温下为无色液体,B为日常生活中的常见金属(反应条件和有些反应的部分产物已略去)。试回答下列问题:
(1)单质E的电子式为 ,反应⑤的离子方程式为 ;
(2)写反应②的化学方程式为 ;
(3)当反应④生成1mol B时,转移的电子数物质的量为
(4)B的两种氯化物形成的混合溶液中,加入适量 (填化学式),可以转化成单一溶质的溶液(不考虑水解),相应的离子方程式是 (写出一种方法即可)。
18、(8分)在一定体积的密闭容器中,进行如下化学反应:
A(g)+2B(g) C(g)+3D(g),△H=Q kJ/mol
C(g)+3D(g),△H=Q kJ/mol
其化学平衡常数K和温度t的关系如下表,回答下列问题:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(1)该反应的化学平衡常数表达式为K = 。
(2)根据以上信息,请你判断该反应△H、△S的关系正确的是( )
A、△H>0、△S<0 B、△H>0、△S>0
C、△H<0、△S>0 D、△H<0、△S<0
(3)能判断该反应是否达到化学平衡状态的依据是 。
a.容器中压强不变 b.混合气体中 c(D)不变
c.2υ正(B)=3υ逆(D) d.c(A)=c(C)
(4)某温度下,平衡浓度符合下式:c(A)·c2(B)=c(C)·c3(D),试判断此时的温度为 ℃。
17、( 11分)四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
性质 结构 信息 |
室温下单质呈粉末状固体,加热易熔化。 单质在空气中燃烧,发出明亮的蓝紫色火焰。 |
单质常温、常压下是黄绿色气体,能溶于水。常用作自来水的消毒。 |
单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 |
原子最外层电子数等于内层电子总数的2倍。 单质为空间网状晶体,具有很高的熔、沸点。 |
⑴ B元素在周期表中的位置 ,
⑵ 写出C单质与水反应的化学方程式 。
A与C形成的化合物溶于水后,溶液的pH 7(填“大于”、“等于”或“小于”),理由是 。(用离子方程式表示)
⑶ D元素最高价氧化物晶体的硬度 (填“大”、“小”),其理由是 。
⑷ A、B两元素非金属性较强的是(写元素符号) 。写出证明这一结论的一个实验事实 。
16、某有机物结构如图 下列关于该有机物的说法正确的是( )
①该物质属于芳香烃 ②可发生加成、消去和硝化反应 ③在酸性条件下水解生成两种有机物 ④1mol该物质与足量NaOH溶液共热,充分反应最多消耗6molNaOH ⑤1mol该物质最多可与7molH2反应
A. ①②⑤ B.③④⑤ C. ③④ D.④
第Ⅱ卷
15、将0.1mol/L的下列物质的水溶液,从常温加热到80℃(不计水的蒸发),溶液的PH不变的是( )
A. NaCl B. (NH4)2SO4
C. H2SO4 D. Ba(OH)2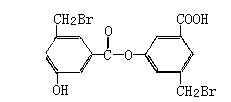
14、据报道,我国拥有完全自主产权的氢氧燃料电池车将在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是( )
A.正极反应式为:O2+2H2O+4e- ===4OH-
B.工作一段时间后,电解液中的KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.1mol电子转移
13、往氯化钡溶液中通入适量的二氧化硫气体,没有沉淀生成。然后再往此溶液中加入足量的下列物质:①氨气;②二氧化氮;③稀硫酸;④硫化氢;⑤氯化氢。一定能生成沉淀的是( )
A.①②③④. B.②③④ C. ①②④ D.①②④⑤
12、25℃时有关物质的颜色和溶度积(KSP)如下表:
|
物质 |
AgC1 |
AgBr |
AgI |
Ag2S |
|
颜色 |
白 |
淡黄 |
黄 |
黑 |
|
KSP |
1.8×10-10 |
7.7×10-13 |
1.5×10-16 |
1.8×10-50 |
下叙述中不正确的是( )
A.向AgC1的白色悬浊液中加入少量KI固体,有黄色沉淀产生
B.25℃时,AgCl、AgBr、Agl、Ag2S等四种饱和水溶液中Ag+的浓度相同
C.25℃,AgC1固体在等物质的量浓度NaCl、CaCl2溶液中的溶度积相同
D.在10 mL l.8×10-5mol·L-1NaC1溶液中,加入1滴(20滴约为1 mL)
1×10-5mol·L-1AgNO3溶液,不能产生白色沉淀。
11、c(NH4+)相同的下列溶液 ①NH4Cl ②(NH4)2SO4 ③NH4HSO4 ④NH4HCO3,其物质的量浓度由大到小的顺序是( )
A、②③①④ B、①④③② C、④①③② D、②④①③
10、在一定温度不同压强(p1<p2)下,可逆反应2X(g)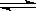 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(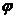 )与反应时间(t)的关系有以下图示,正确的是( )
)与反应时间(t)的关系有以下图示,正确的是( )
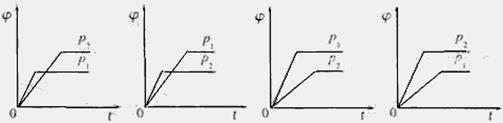
A B C D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com