
12.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O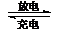 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是
A、充电时阳极反应:Ni(OH)2 -e- + OH- ﹦ NiOOH + H2O
B、充电过程是化学能转化为电能的过程
C、放电时负极附近溶液的碱性不变
D、放电时电解质溶液中的OH-向正极移动
11.设NA为阿伏加德罗常数,下列叙述正确的是
A.24 g镁的原子最外层电子数为NA B.1 L 0.1 mol·L-1乙酸溶液中H+数为0.1NA
C.1 mol甲烷分子所含质子数为10NA D.标准状况下,22.4 L乙醇的分子数为NA
10.下列各组离子,在指定的环境中一定能大量共存的是
A.澄清透明的无色溶液中:Cl-、MnO4-、Ag+、SO42-
B.在能使pH试纸变深蓝色的溶液中:Al3+、NO3-、S2-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、K+、SO42-、NO3-
D.在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、I-
9.下列反应的离子方程式书写正确的是
A.98.3%的硫酸加入到稀氢氧化钡溶液中:
H+(aq)+OH-(aq)=H2O(aq); ΔH=-57.3kJ/mol
B.100mL0.1mol·L-1的Na2CO3溶液中逐滴加入0.01molCH3COOH
CO32-+ 2CH3COOH = CO2↑+ 2CH3COO-+ H2O
C.铜片插入氯化铁溶液中: Cu+2Fe3+=Cu2++2Fe2+
D.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4+
8.铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第6周期。Tl3+与Ag在酸性介质中发生反应:Tl3++ 2Ag ==Tl+ + 2Ag+。下列推断正确的是
A.Tl+ 的最外层有1个电子 B.Tl3+ 的氧化性比Al3+弱
C.Tl能.形成+3价和+1的化合物 D.Tl+ 的还原性比Ag强
7.实验室用Al2(SO4)3溶液制取Al(OH)3,最合适的试剂是
A.NaOH B.H2SO4 C.NH3·H2O D.KOH
6.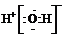 水是最宝贵的资源之一。下列表述正确的是
水是最宝贵的资源之一。下列表述正确的是
A.H2O的电子式为 B.4℃时,纯水的pH=7
C.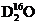 中,质量数之和是质子数之和的两倍
中,质量数之和是质子数之和的两倍
D.273K、101kPa,水分子间的平均距离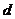 :
: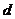 (气态)>
(气态)>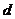 (液态)>
(液态)>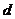 (固态)
(固态)
5.利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是
A. 电解时以精铜作阳极 B.电解时阴极发生氧化反应
C.粗铜连接电源负极,其电极反应是Cu =Cu2+ + 2e
D.电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥
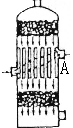
4.在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有
热交换器的接触室(右图)。按此密闭体系中气体的流向,则在A处流出的气体为
A、SO2 B、 SO3,O2 C、SO2,SO3 D、SO2,O2
3.下列有关晶体的叙述中,错误的是
A.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子
 B.在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或Na+)
B.在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-(或Na+)
C.白磷晶体中,微粒之间通过共价键结合,键角为60°
D.离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键不被破坏
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com