
8.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):
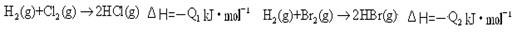
有关上述反应的叙述正确的是 ( )
A.Q1>Q2
B.生成物总能量均高于反应物总能量
C.生成1molHCl气体时放出Q1热量
D.1mol HBr(1)具有的能量大于1mol HBr(g)具有的能量
7.电解100mL含c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是 ( )
A.0.20mol/L Cu2+ B.0.02mol/L Zn2+
C.0.20mol/L Pb2+ D.0.10mol/LAg+
6.能正确表示下列反应的离子方程式是 ( )
A.向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO
B.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O= CaSO3↓+2HClO
5.某同学在实验报告中记录下列数据,其中正确的是 ( )
A.用25 mL量筒量取12.36 mL盐酸
B.托盘天平称取8.75克食盐
C.用电子天平称取1.2355克无水碳酸钠
D.用广泛pH试纸测得某溶液pH为3.5
4.下列叙述中正确的是 ( )
A.向含有CaCO3沉淀的水中通入CO2 至沉淀恰好溶解,再向溶液中加入饱和NaHCO3溶液,又有CaCO3沉淀生成
B.向Na2 CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2 CO3的物质的量之比为1:2
C.等质量的NaHCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2 CO3饱和溶液中通入CO2,有NaHCO3结晶析出
3.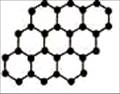 石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),
石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),
可由石墨剥离而成,具有极好的应用前景。下列说法正确的是( )
A.石墨烯与石墨互为同位素
B.0.12g石墨烯中含有6.02×1022个碳原子
C.石墨烯是一种有机物
D.石墨烯中的碳原子间以共价键结合
2.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA
B.标准状况下,22.4 L己烷中共价键数目为19NA
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.1 L浓度为1 mol·L-1的Na2CO3溶液中含有NA个CO32-
1.根据陈述的知识,类推得出的结论正确的是 ( )
A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O
B.乙烯可使酸性高锰酸钾溶液褪色,则丙烯也可以使其褪色
C.CO2和SiO2 化学式相似,则CO2与SiO2的物理性质也相似
D.金刚石的硬度大,则C60的硬度也大
16、已知A、B、C、D、E是核电荷数依次增大的五种短周期元素,且原子半径按D、E、B、C、A的顺序依次减小,B和E同族,则下列推断中不正确的是( )
A、D位于第二周期 B、A、B、E一定位于不同周期
C、A、D可能属于同一主族 D、C和D的单质有可能化合形成离子化合物

版权所有:()
版权所有:()

15、R为短周期元素,其原子所具有的电子层数为最外层电子数的1/2。它可能形成的含氧酸根离子有①R2O42-、②RO42-、③R2O32-、④RO32-。下列判断正确的是 ( )
A、当它形成①时,不可能形成④ B、当它形成②时,不可能形成③、④
C、当它形成①时,不可能形成②、③ D、当它形成②时,可以形成①
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com