
7.过抛物线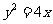 的焦点
的焦点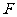 作直线
作直线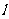 交抛物线于
交抛物线于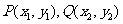 两点,若
两点,若 ,则
,则 ( )
( )
A.5 B.6 C.8 D.10
6.用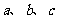 表示三条不同的直线,
表示三条不同的直线, 表示平面,其中正确的命题是 ( )
表示平面,其中正确的命题是 ( )
①若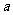 //
//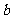 ,
,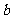 //
// ,则
,则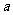 ∥
∥ ; ②若
; ②若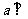
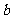 ,
,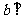
 ,则
,则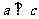 ;
;
③若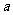 //
// ,
,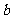 //
// ,则
,则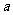 ∥
∥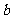 ; ④若
; ④若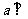
 ,
,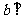
 ,则
,则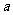 ∥
∥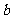 .
.
A.①④ B.②③ C.①② D.③④
5.设等比数列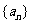 的公比
的公比 , 前n项和为
, 前n项和为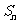 ,则
,则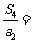 ( )
( )
A.2 B.4 C. D.
D.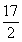
4.在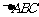 中,“
中,“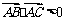 ”是“
”是“ 为锐角三角形”的 ( )
为锐角三角形”的 ( )
A.充分不必要条件 B.必要不充分条件
C.充要条件 D.既非充分又非必要条件
3.在复平面内,复数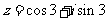 对
对
应的点位于 ( )
A.第一象限 B.第二象限
C.第三象限 D.第四象限
2.执行右面的框图,若输出结果为 ,
,
则输入的实数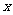 的值是( )
的值是( )
A.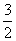 B.
B.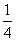
C.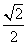 D.
D.
1.集合A=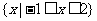 ,B=
,B=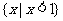 ,则
,则 ( )
( )
 A.
A.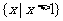 B.
B.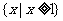
C. D.
D.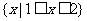
22.(15分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
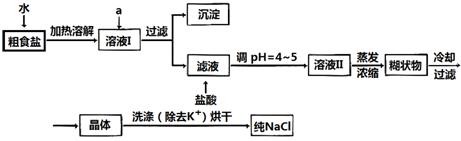
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液
Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为_______ __(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_____ ____。
 (2)用提纯的NaCl配制500 mL4.00 mol·L-1NaCl溶液,
(2)用提纯的NaCl配制500 mL4.00 mol·L-1NaCl溶液,
所用仪器除天平、药匙、玻璃棒外还有___ _____
(填仪器名称)。
(3)电解饱和食盐水的装置如图所示,若收集的H2为2 L,
则同样条件下收集的Cl2_____(填“>”、“=”或“<”)2 L,
原因是_________。装置改进后,可用于制备NaOH溶液,
若测定溶液中NaOH的浓度,常用的方法是__________。
(4)实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4 ZnSO4+H2↑;MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置_________(填代号)。
可选用制备气体的装置:
21.(11分)二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)煤的气化的主要化学反应方程式为:_______________________。
(2)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g)+ CO(g)CH3OH(g);ΔH=-90.8 kJ·mol-1
② 2CH3OH(g)CH3OCH3(g)+H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g)+H2O(g)CO2(g)+ H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g)+ 3CO(g)CH3OCH3(g)+CO2 (g)的ΔH=___________;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是__________(填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(3)已知反应②2CH3OH(g)CH3OCH3(g)+H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
|
物质 |
CH3OH |
CH3OCH3 |
H2O |
|
浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
①比较此时正、逆反应速率的大小: v正______ v逆 (填“>”、“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) =_________;该时间内反应速率v(CH3OH) =__________。
20.(12分)有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有 (选填序号)。
①加成反应 ②酯化反应 ③加聚反应 ④氧化反应
(2)B分子所含官能团的名称是 。
(3)B分子中没有支链,其结构简式是 ,B的具有相同官能团的同分异构体的结构简式是 。
(4)由B制取A的化学方程式是 。
 (5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
天门冬氨酸的结构简式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com