
2. 有机物分子结构的确定--物理方法(波谱法)
化学方法以官能团的特征反映为基础,鉴定出官能团,还要制备它的衍生物以进一步确认其结构。当化合物结构比较复杂时,往往要耗费大量时间。物理方法(波谱法)具有微量、快速、准确、信息量大等特点。(1)质谱--可快速、准确测定有机物的相对分子质量。(2)红外光谱--可以获得分子中含有何种化学键或官能团的信息。⑶核磁共振氢谱--可推知有机物分子中有几种不同类型的氢原子及它们的数目之比。
[典型例析]
例1:已知某有机物 A 的式量为 128。
(1)若 A 物质中只含有碳、氢、氧三种元素,且 A 分子中含有一个酯的结构,则 A 的分子式为__________,结构简式为____________(任写出一种)。
(2)若 A 物质中只含有碳、氢、氮三种元素,且 A 分子中氮原子数目最少,则 A 的分子式为__________,若 A 分子中有一个由氮原子和其他碳原子形成的六元环,则 A 的结构简式为__________(任写一种)。
变式训练:
某有机物仅含C、H、N三种元素,其相对分子质量不超过200,其中氮元素的质量分数为10.85%,下列关于该有机化合物的说法正确的是
A.可能是芳香烃 B.不可能是芳香族化合物
C.该物质的熔点较高 D.分子结构中可能只含有单键
例2:A是烃,B是烃的含氧衍生物,A、B均为常见的有机物。由等物质的量A和B组成的混合物0.05 mol在0.125 mol O2中恰好完全燃烧生成0.1 mol CO2和0.1 mol H2O。试回答下列问题:
⑴混合物中A、B的组合可能有_________种。
⑵另有一种组合的A和B,以任意比混合,且物质的量之和为a mol。①若耗氧量一定,则A、B的分子式分别是A_________,B_________,耗氧量为_________mol(用a表示)。②若生成的CO2和H2O的物质的量一定,则A、B的分子式分别是A_________,B_________。③若生成CO2的量为定值,则生成物H2O的质量范围为_________(用a表示)。
变式训练:
现有0.1 mol某有机物A在8.96 L O2中充分燃烧后,气体体积变为6.72 L,通过足量碱石灰吸收后剩余2.24 L(气体体积均在标准状况下测定)。
(1)燃烧后所得混合气体中CO2的物质的量为___________,2.24L剩余气体可能是________或___________;
(2)若A是烃,其化学式可能是_______或_______;若A是烃的衍生物,其化学式可能是_______或_______。
(3)若A由丁醛(C4H8O)与气体B等物质的量混合得到,则气体B的化学式为_______。
例3:胡椒酚A是植物挥发油中的一种成分。某研究性学习小组对其分子组成结构的研究中发现:A 的相对分子质量不超过150;A中C、O的质量分数分别为:w(C)=80.60%,w(O)=11.94%,完全燃烧后产物只有CO2和H2O。根据以上信息,填写下列内容:
(1)A的摩尔质量为 。
(2)光谱分析发现A中不含甲基(-CH3),苯环上的一氯取代只有2种;1molA与足量溴水反应,最多消耗3molBr2。A的结构简式为 。
(3)A的一种同分异构体中,苯环上含有两个取代基,取代基位置与A相同,且能发生银镜反应。
①符合条件的A的同分异构体的结构简式 。
②上述A的一种同分异构体发生银镜反应的化学方程式 。
变式训练:
有机物A与乙酸无论以何种比例混合,只要质量一定,完全燃烧后产生的水的质量也一定,试回答:
(1)若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为_____________。
(2)若A由四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为_____________。
(3)若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为___________。如果A分子每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为________________________。
[当堂反馈]
1. 有机物分子结构的确定--化学方法
由于有机化合物中存在同分异构现象,除少数的分子式只对应一种结构外,一般一种分子式对应有多种结构。我们常从以下两方面确定其结构:
(1)根据有机物的特殊反应,确定物质分子中的官能团,从而进一步确定其结构。常见有机物中,能使酸性高锰酸钾溶液褪色的烃类物质有烯烃、炔烃、苯的同系物;能与溴水产生白色沉淀有机物是苯酚;能发生与银氨溶液或新制Cu(OH)2反应的物质有醛类、甲酸、甲酸某酯、葡萄糖、麦芽糖等;能与碳酸钠反应产生气体的有机物是羧酸。
(2) 有机物实验式的确定
①实验式(又叫最简式)是表示化合物分子所含各元素的原子数目最简单整数比的式子。
②若有机物分子中 w(C)=a%、w(H)=b%、w(O)=c%,则:N(C) : N(H) : N(O)=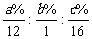 ,即可得到实验式。实验式也可以通过燃烧产物的物质的量等方法确定。确定实验式前必须先确定元素的组成,如某有机物完全燃烧的产物只有 CO2 和 H2O,则其组成元素可能为C、H 或 C、H、O;若燃烧产物 CO2 中的碳元素的质量和燃烧产物 H2O 中氢元素的质量之和等于原有机物的质量时,则原有机物组成中不含O元素。
,即可得到实验式。实验式也可以通过燃烧产物的物质的量等方法确定。确定实验式前必须先确定元素的组成,如某有机物完全燃烧的产物只有 CO2 和 H2O,则其组成元素可能为C、H 或 C、H、O;若燃烧产物 CO2 中的碳元素的质量和燃烧产物 H2O 中氢元素的质量之和等于原有机物的质量时,则原有机物组成中不含O元素。
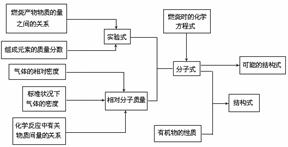
(3)确定有机物分子式和结构式的过程可简单归纳如下:
7、除去括号中的杂质,写出所加试剂的化学式
⑴Cl-(SO42-) ⑵SO42-(CO32-)
⑶NaCl(NaOH) ⑷Fe2+(Cu2+)
6、能在无色溶液中大量共存的一组离子是 ( )
A.Cu2+、SO42-、OH-、K+ B.Fe3+、NO3-、Cl-、H+
C.K+、CO32-、Cl-、H+ D.H+、Na+、Cl-、SO42-
5、只能表示一个化学反应的离子方程式是 ( )
A.H++OH-=H2O
B.2H++CO32-=H2O+CO2↑
C.Zn(OH)2+2H+=Zn2++2H2O
D.Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓
4、下列各组中两种溶液间的反应,不能用同一离子方程式来表示的是 ( )
A.HCl+Na2CO3;H2SO4+K2CO3
B.Fe+HCl;Fe +H2SO4
C.BaCl2+Na2SO4;Ba(OH)2+(NH4)2SO4
D.KOH+CH3COONH4;Ba(OH)2+NH4Cl
3、下列化学反应中,能用离子方程式H++OH-=H2O 表示的是 ( )
A.硝酸溶液和氢氧化钠溶液 B.氢氧化铁溶液和盐酸溶液
C.氢氧化钠溶液和盐酸溶液 D.氢氧化铜和硫酸溶液
2、下列化学方程式与相应的离子方程式都正确的是 ( )
A.2FeCl3+Cu=2FeCl2+CuCl2
2Fe3++Cu=2Fe2++Cu2+
B.2HNO3+CaCO3=Ca(NO3)2+CO2↑+H2O
2H++CO32-= CO2↑+H2O
C.Fe+2HCl=FeCl2+H2↑
Fe+2H+=Fe2++H2↑
D.Cu(OH)2+2HCl=CaCl2+2 H2O
OH-+H+= H2O
1、正确书写离子方程式时,应使等号两边 ( )
A.离子的数目相等 B.粒子的总的物质的量相等
C.正电荷或负电荷总数应相等 D.各元素原子的数目应相等
3、复分解反应型离子反应发生的条件:生成沉淀或放出气体或生成水。
[思考与交流]
下列各组离子在溶液中不能大量共存的是 ( )
A.Na+、Ba2+、Cl-、SO42- B.K+、SO42-、NO3-、OH-
C.H+、NH4+、Fe3+、SO42- D.H+、Cl-、CO32-、NO3-
[归纳与整理]
判断溶液中有关离子能不能大量共存,事实上是判断它们在给定的条件下能不能形成难溶化合物、难电离的物质以及气态物质,要考虑元素及其化合物的离子性质;此外解题时还要特别注意试题的前提设置。
[回顾与总结]
本节课我们主要学习了离子反应与其发生的条件,以及离子方程式的书写。
补充练习
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com