
7.如图所示,a、b分别为两种不同物质的熔化曲线,关于这两种物质,下列判断正确的是( )。 A.a曲线对应的物质是非晶体 B.b曲线对应的物质是晶体 C.a曲线对应的物质微粒是有规则地在空间排成阵列的 D.a曲线对应的物质的物理性质一定是各向同性的
6.频率不同的两束单色光1和2 以相同的入射角从同一点射入一厚玻璃板后,其光路如图所示。关于单色光1和2,下列说法正确的是 ( )。
A.在玻璃中单色光1的波长较长
B.在玻璃中单色光1的传播速度较大
C.从玻璃射向空气,玻璃对单色光1的全反射临界角较小
 D.若增大入射角,单色光2先发生全反射
D.若增大入射角,单色光2先发生全反射
5. 在杨氏双缝干涉实验中,( )。
A.若用白光作为光源,屏上将呈现黑白相间的条纹
B.若将红光改用紫光作为光源,屏上呈现的条纹的间距将变大
C.用红光照射一条狭缝,用紫光照射另一条狭缝,屏上仍将呈现干涉条纹
D.用紫光作为光源,遮住其中一条狭缝,屏上将呈现紫黑相间且间距不等的条纹
在杨氏双缝干涉实验中,( )。
A.若用白光作为光源,屏上将呈现黑白相间的条纹
B.若将红光改用紫光作为光源,屏上呈现的条纹的间距将变大
C.用红光照射一条狭缝,用紫光照射另一条狭缝,屏上仍将呈现干涉条纹
D.用紫光作为光源,遮住其中一条狭缝,屏上将呈现紫黑相间且间距不等的条纹
4. 关于液体中布朗运动和气体分子统计观点,下列说法中正确的是( )。 A.布朗运动是液体分子的无规则运动 B.悬浮颗粒越大,在相同时间内撞击它的分子数越多,布朗运动越显著 C.某温度下,气体的多数分子的速率表现出“中间多、两头少”的分布规律 D.温度升高时,“中间多、两头少”的分布规律是不变的,但分布曲线的峰值向速率小的一方移动
3. 关于麦克斯韦的电磁场理论,下列说法中正确的是( )。 A.在电场周围一定产生磁场,磁场周围一定产生电场 B.周期性变化的电场周围一定产生周期性变化的磁场 C.均匀变化的电场周围一定产生均匀变化的磁场 D.在变化的电场周围一定产生变化的磁场,变化的磁场周围一定产生变化的电场
2. 关于液晶和表面张力,下列说法中正确的是( )。 A.液晶是液体和晶体的混合物 B.液晶具有流动性、连续性和各向同性 C.蜥蜴能在水面上行走是由于受到表面张力和重力平衡的结果 D.在完全失重的环境下,熔化的金属在表面张力作用下呈标准的球体
1. 关于光的现象,下列说法正确的是( )。
A.用光导纤维束传送图象信息,这是光的衍射的应用
B.太阳光通过三棱镜形成彩色光谱,这是光的干涉的结果
C.眯着眼睛看发光的灯丝时能观察到彩色条纹,这是光的偏振现象
D.在照相机镜头前加装偏振滤光片拍摄日落时水面下的景物,可使景像清晰
30. (8分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)
(8分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),右下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
(1)关于该反应的下列说法中,正确的是_______。
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0。
(2)该反应平衡常数K的表达式为_______________。
(3)温度降低,平衡常数K_____(填“增大”、“不变”或“减小”)。
 (4)为探究反应原理,现进行如下实验:在体积为2L的密闭容器中,充入2mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如右图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2) 为:
(4)为探究反应原理,现进行如下实验:在体积为2L的密闭容器中,充入2mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化如右图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2) 为:
________________________
(5)下列措施中能使n(CH3OH)/n(CO2)增大的有______。
A.升高温度; B.加入催化剂;
C.将H2O(g)从体系中分离; D.再充入1molCO2和3molH2;
E.充入He(g),使体系总压强增大。
季延中学2009-2010学年度第二学期期末考试
29.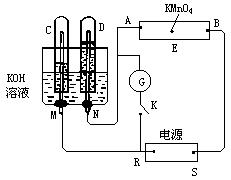 (7分)如下图,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞。A,B分别为Pt片,压在滤纸两端,R、S为电池的电极。M、N是多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极。G为电流计, K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生。根据图分析回答:
(7分)如下图,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞。A,B分别为Pt片,压在滤纸两端,R、S为电池的电极。M、N是多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极。G为电流计, K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生。根据图分析回答:
(1)R为____极,S为_____极。
(2)A附近溶液的现象是__________,B附近发生的电极反应式为:
。
(3)滤纸上的紫色点向哪方移动____(填A或B)。
(4)当C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,有关的电极反应式为(−) (+) 。
28.(8分)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
(1)向该溶液中加入少量盐酸时,发生反应的离子方程式是
向其中加入少量KOH溶液时,发生反应的离子方程是
(2)现将0.04 mol·L-1HA溶液和0.02 mol·L-1NaOH 溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该溶液显碱性,则溶液中c(Na+) c(CN−)(填“<”“=”“>”)
②若HA为CH3COOH ,该溶液显酸性。溶液中所有的离子按浓度由大到小排列的顺序是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com