
4.已知x与y之间的一组数 据:
据:
|
x |
0 |
1 |
2 |
3 |
|
y |
1 |
3 |
5 |
7 |
则y与x的线性回归方程为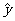 =
=
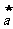 必过 ( )
必过 ( )
A.点 B.点
B.点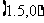 C.点
C.点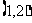 D.点
D.点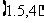
3.若由一个2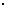 2列联表中的数据计算得
2列联表中的数据计算得 的观测值
的观测值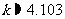 ,那么认为两个变量有关系的把握程度为 ( )
,那么认为两个变量有关系的把握程度为 ( )
A.95% B.97.5% C.99% D.99.9%
2.若函数 ,则
,则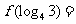 ( )
( )
A. B.
B. C.
C. D.
D.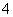
填入答题卡相应的格子中.
1.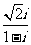 的共轭复数是 ( )
的共轭复数是 ( )
A.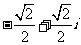 B.
B.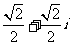
C.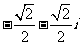 D.
D.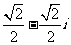
23. (7分)一定量的氢气在氯气中燃烧,所得混合物用100mL 4.00mol/L的NaOH溶液(密度为1.20g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.
(7分)一定量的氢气在氯气中燃烧,所得混合物用100mL 4.00mol/L的NaOH溶液(密度为1.20g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0. 0800mol。(以下计算要有计算过程)
0800mol。(以下计算要有计算过程)
 (1)求原NaOH溶液的质量分数为多少?
(1)求原NaOH溶液的质量分数为多少?
 (2)求所得溶液中Cl-的物质的量。
(2)求所得溶液中Cl-的物质的量。
 (3)所用氯气和参加反应的氢气的物质的量之比为多少?
(3)所用氯气和参加反应的氢气的物质的量之比为多少?
22.(8分)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
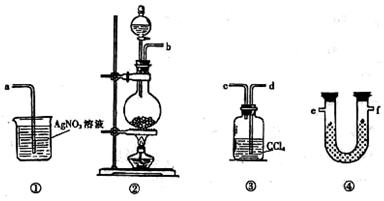
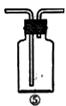
⑴请根据甲同学的意图 ,连接相应的装置,接口顺序:
,连接相应的装置,接口顺序:
b接________,__________接 _________,_________接a。
⑵U形管中所盛试剂的化学式为________ _____________________ 。
_____________________ 。
⑶装置③中CCl4的作用是___________________________________。
⑷乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_____________之间(填装置序号)。瓶中可以放入______________________________________。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成 __________________________,如果观察到_______________________________________的现象,则证明制Cl2时有HCl挥发出来。
__________________________,如果观察到_______________________________________的现象,则证明制Cl2时有HCl挥发出来。
21.(8分)要配制450mL 0.2mol·L-1FeSO4溶液,实验操作步骤有:①在天平上称取a g绿矾(FeSO4·7H2O),将它放在烧杯中,用适量蒸馏水使其完全溶解 ②将所得溶液 沿玻璃棒注入500mL容量瓶中 ③继续向容量瓶中加水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至凹液面底部与刻度线相切 ④用少量水洗涤烧杯和玻璃棒2~3次,每次洗液都转入容量瓶 ⑤将容量瓶塞紧,充分摇匀
沿玻璃棒注入500mL容量瓶中 ③继续向容量瓶中加水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至凹液面底部与刻度线相切 ④用少量水洗涤烧杯和玻璃棒2~3次,每次洗液都转入容量瓶 ⑤将容量瓶塞紧,充分摇匀
填写下列空白
⑴a g绿矾的实际质量为____________g。
⑵上述操作步骤的正确顺序为__________________。
⑶下列操作会使所配溶液的浓度偏高的是__________
 A.若配制时遗漏步骤④; B.定容时俯视刻度线;
A.若配制时遗漏步骤④; B.定容时俯视刻度线;
C.称量时物 、码放反了;
D.绿矾样品已部
、码放反了;
D.绿矾样品已部 分风化
分风化
E.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切;
F.引流时玻璃棒靠在刻度线上方
⑷若加蒸馏水时不慎超过刻度线,处理方法是________________;
若操作步骤②时有溶液溅在容量瓶外,处理方法是__________________。
20. (7分)检查装置气密性是化学实验中的重要操作之一。试按要求回答下列问题:
(7分)检查装置气密性是化学实验中的重要操作之一。试按要求回答下列问题:
 (1)下列仪器或装置在使用前一定要检查气密性的是 (填序号,下同)。
(1)下列仪器或装置在使用前一定要检查气密性的是 (填序号,下同)。
 A.容量瓶 B.洗气瓶
C.分液漏斗 D.酸(碱)式滴定管
A.容量瓶 B.洗气瓶
C.分液漏斗 D.酸(碱)式滴定管

 (2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是 。
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是 。
 A.收集不到气体
A.收集不到气体
B.造成环境污染
 C.观察到的实验现象有误
C.观察到的实验现象有误
D.引发爆炸事故
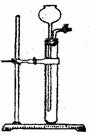
 (3)检查右图所示简易气体发生装置的气密性操作是:___________
(3)检查右图所示简易气体发生装置的气密性操作是:___________

 (4)该装置能做到关闭活塞,随后反应停止。它的原理是:_________
(4)该装置能做到关闭活塞,随后反应停止。它的原理是:_________
19.(10分)某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加人铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加人氨水有白色沉淀生成,继续加人过量氨水,沉淀不消失;
④取溶液少许,滴人氯化钡溶液产生白色沉淀;
⑤取实验 ④ 后的澄清溶液,滴人硝酸银溶液产生白色沉淀,再加人过量的稀硝酸,沉淀不消失。

请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是_____________ ______(填代号)。
______(填代号)。
(2)根据上述实验判断原溶液中肯定存在的离子是____________________,肯定不存在的离子是_______________。
(3)写出与实验②有关的离子方程式:____________________________。
18.
 (8分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):
(8分)某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl2、NaCl中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下体积):




 请回答:
请回答:
 (1)混合物中是否存在FeCl2_________(填“是”或“否”);
(1)混合物中是否存在FeCl2_________(填“是”或“否”);
 (2)混合物中是否存在(NH4)2SO4_____(填“是”或“否”),你的判断依据是_______。
(2)混合物中是否存在(NH4)2SO4_____(填“是”或“否”),你的判断依据是_______。
 (3)写出反应⑤的离子反应方程式;___________________________________。
(3)写出反应⑤的离子反应方程式;___________________________________。
 (4)请根据图中数据分析,原固体混合物的成分为
(4)请根据图中数据分析,原固体混合物的成分为 ______________________(写化学式)。
______________________(写化学式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com