
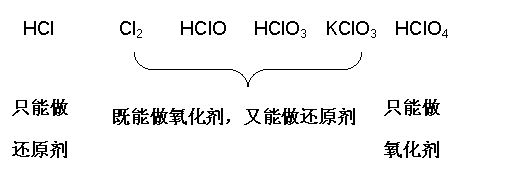
1.元素处于不同的化合价在氧化还原反应中可能表现哪些性质?并以氯元素的不同价态的代表物质进行分析。
|




|
4.在同一个化学反应中,元素得电子数和失电子数有何关系?
[叙述]讲述如何用“双线桥”法表示上面所得到的信息。
[板书]

[叙述] 氧化还原反应是有电子转移的反应。
氧化还原反应的方程式的系数是与反应过程中得失电子的数目相关的。
在氧化还原反应中,失去电子的物质叫做还原剂,还原剂发生氧化反应,表现还原性。可以这样记忆:还原剂化合价升高、失电子、具有还原性,被氧化。
[思考与讨论]辨析在2Na+Cl2=2NaCl的反应中,氧化剂和还原剂分别是什么?
怎样判断元素在氧化还原反应中是被氧化还是被还原呢?
[板书]

还原剂 氧化剂
有还原性 有氧化性
被氧化 被还原
[思考与讨论]
3.在同一个化学反应中,元素化合价升高和降低的数目有何关系?
2.元素的化合价在何种情况下会发生变化?
[情景引入]由复习上节课氯气有关反应引入本节课的研究主题。先由学生书写氯气与钠、铁、氢气和水,次氯酸分解、此氯酸钙和二氧化碳、水反应的化学方程式。
[练习]学生自己书写方程式,并留待后面的学习继续使用。
[过渡]我们结合在第一章中学过的氧化还原反应的定义,来判断一下这些化学反应应属于氧化还原反应,还是非氧化还原反应。。
[媒体]
2Na+Cl2=2NaCl
2Fe + 3Cl2  2FeCl3
2FeCl3
H2 + Cl2  2HCl
2HCl
Cl2+H2O HCl+HClO
HCl+HClO
Ca(ClO)2+CO2+H2O=CaCl2+2HClO
2HClO O2↑+ 2HCl
O2↑+ 2HCl
[练习]学生自己进行判断,或可小组讨论、分析。
[叙述]现在请大家在氯气与钠反应的方程式上,标出化合价发生改变的元素,在反应前后的化合价。
[思考与讨论]学生解决下列问题:
1.元素的化合价是由什么决定的呢?
由复习氯气主要化学性质所涉及的化学反应引入,结合专题1中的氧化还原反应和非氧化还原反应对这些反应进行判断,从而分析氧化还原反应和非氧化还原反应的本质区别,并从电子转移等角度进行系统分析,再升华到构建氧化还原反应和四种基本反应类型之间关系的概念。
重点:氧化还原反应。
难点:氧化还原反应中化合价变化与电子得失的关系,氧化剂、还原剂的判断。
5.理解氧化反应和还原反应、得电子和失电子之间相互依存、相互对立的关系。
4.辨析氧化还原反应和四种基本反应类型之间的关系,并用韦恩图表示之,培养比较、类比、归纳和演绎的能力。
3.理解氧化还原反应的本质。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com