
2.
(1)离子方程式 。
(2)物质的量是 。
(3)氧化性由弱到强的顺序是_____________ ____。
1.
(1)分子式为:
(2)分子式为:
(3)分子式: 。
7.与淀粉相关的物质间转化关系如下图所示。其中B的分子中含有一个甲基,B与羧酸和醇均能发生酯化反应;C的催化氧化产物既是合成酚醛树脂的原料之一,又是常见的居室污染物;E能使Br2的CCl4溶液褪色。

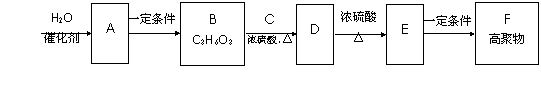
(1)B的结构简式是 。
(2)E→F的化学方程式是 。
(3)某同学欲验证淀粉完全水解的产物A,进行如下实验操作:
①在试管中加入少量淀粉 ②加热3-4 min ③加入少量新制的Cu(OH)2悬浊液 ④加入少量稀硫酸 ⑤加热 ⑥待冷却后,滴加NaOH溶液至溶液呈碱性。
则以上操作步骤正确的顺序是(填选项序号) 。
a.①②④⑤③⑥ b.①④②③⑤⑥ c.①④②⑥③⑤ d.①⑤③④⑥②
北京市日坛中学2010-2011学年度第一学期
摸底考试高三年级
化学 答题纸2 010.8
010.8
常用原子量:C-12 H-1 O-16 S-32 Na-23 Cl-35.5 K-39 I-127 Mn-55
6.合成氨工业对化学和国防工业具有重要意义。
(1)实验室欲用下图所示装置(夹持固定装置略去)制备并收集氨气。
 ① 请在图中烧瓶内绘出导管所缺部分。
① 请在图中烧瓶内绘出导管所缺部分。
② 试管中反应的化学方程式是:
。
③ 为吸收多余的氨气,烧杯中的试剂是 。
(2)氨有很多重要性质。
① 将酚酞溶液滴加到氨水中溶液呈红色,其原因是 。
② 管道工人曾经用浓氨水检验氯气管道是否漏气,如出现白烟,说明有氯气泄露,同时还有一种相对分子质量为28的气体生成,该反应的化学方程式
是 。
5.中学化学中几种常见物质的转化关系如下:(提示:A与硫反应生成低价态)
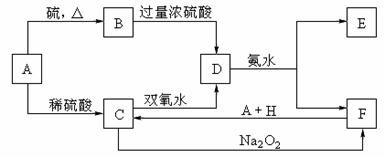
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体F粒子直径大小的范围: 。
(2)A、B、H的化学式:A ,B ,H 。
(3)①H2O2分子的电子式:
②写出C的酸性溶液与双氧水反应的离子方程式: 。
4.如图,将铜片和锌片焊接在一起组成A电极,B为碳棒进行电解实验,电解液中含硝酸银和硝酸铜各0.1 mol。已知电路中通过0.2 mol电子。
(1)请写出A.B两极发生反应的电极反应式A:
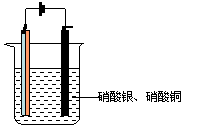 B:
B:
(2)请分析A.B两极质量变化情况为
A:
B:  A
B
A
B
3.现有A、B、C、D、E五种盐溶液,分别由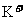 、
、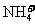 、
、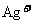 、
、 、
、 、
、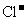 、
、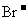 、
、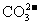 、
、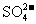 、
、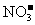 中的阳离子和阴离子各一种组成(五种盐所含阴、阳离子各不相同)
中的阳离子和阴离子各一种组成(五种盐所含阴、阳离子各不相同)
已知:①A+B→白↓ ②A+D→白↓ ③B+C→白↓
④D+C→白↓ ⑤A溶液中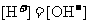
⑥B溶液中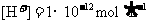 ⑦C、D、E三种溶液的pH<7,
⑦C、D、E三种溶液的pH<7,
根据以上实验事实可以推出(用分子式表示)
A为___________________;B为__________________;
C为___________________;D为__________________;E为___________________.
写出以上①②③④各步反应的离子方程式:
①_________________________________________________________________________
②_________________________________________________________________________
③_________________________________________________________________________
④_________________________________________________________________________
2.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式 。
(2)实验②中化学反应转移电子的物质的量是 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是_____________ ____。
1.硫通常是一种淡黄色晶体,它的蒸气有橙色、无色、红棕色三种,它们都是硫的单质,但是每个分子中硫原子的个数不同,可用SX表示,对三种蒸气测定的结果是:
(1)橙色蒸气的密度折算成标准状况后是11.34克/升,它的分子式为:
(2)红棕色蒸气的质量是相同状况下同体积空气的6.62倍,则它的分子式为:
(3)无色蒸气的密度是同状况下氢气密度的64倍,则它的分子式: 。
25.下列溶液中,物质的量浓度为1mol/L的是
A、将40克NaOH固体溶解于1L水中
B、将22.4L的HCl气体溶于水配成1L溶液
C、将1L10mol/L的浓盐酸与9L水混合
D、10克NaOH固体溶解于水配成250ml溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com