
3.对试剂瓶的一般要求
固体药品保存在________中,以便用___________取用,液体药品保存在____________中;_________________等见光易分解的试剂要保存在________中。
2. 特殊保存的几种试剂
|
类别 |
常见药品 |
有关特性 |
保存方法 |
|
见光易 变质 |
氯水、硝酸、AgNO3、双氧水 |
见光易分解、有强氧化性 |
棕色瓶中,冷暗处,不用橡皮塞 |
|
易燃 |
⑴ 红磷、硫、镁 |
遇火易燃 |
远离火种,单独存放 |
|
⑵ 汽油、苯、乙醇、低级酯 |
易燃有机溶剂 |
远离火种,不用橡皮塞 |
|
|
易爆 |
⑴ KMnO4、KClO3、NH4NO3、KNO3 |
受热易分解,强氧化性 |
远离易燃物,防受热撞击 |
|
⑵ 硝酸纤维、银氨溶液 |
不稳定、易引起爆炸 |
随用随制 |
|
|
强 腐 蚀 性 |
⑴ 液溴 |
易挥发的强氧化剂 |
棕色瓶中,玻璃塞,水封 |
|
⑵ 氢氟酸 |
腐蚀玻璃 |
塑料瓶中 |
|
|
剧毒 |
P4、Hg、HgCl2、可溶钡盐、KCN |
对人和生物有剧毒 |
单独存放、专人管理 |
化学试剂的保存一般要根据物质本身的性质和可能变质的原因,选用不同的保存方法,以保证药品完好无损,同时不影响周围环境。
1.需密封保存的试剂
⑴由于试剂与空气中的某种成分作用而要密封保存
①能与CO2作用的:碱类如_______________________等,含比碳酸更弱的酸的盐如______________________等,另外还有碱石灰、过氧化钠等等。
②能与水作用的:与水反应的单质有____________________等,与水反应的氧化物有____________________________等,与水反应的盐有________________________等;易潮解的物质有______________________________________________等;易吸水的液态物质有 _______________________。
③能与O2反应的:还原性较强的物质常温下一般都易与O2反应,如______________等单质,____________等盐, 等有机物。
⑵由于试剂易挥发应密封保存,如______________等无机试剂以及____________等有机溶剂,这些物质除了密封外,还要注意置于阴凉处。
18.聚氯乙烯[(CH2CHCl)n]是最早工业化生产的重要塑料品种之一,其具有价格低廉、难燃烧等优点,因此产量仅次于聚乙烯居第二位,约是世界热塑性塑料产品的23%。但是,其加工过程需要使用许多有毒添加剂。有毒的添加剂会渗出对人类造成危害;另外,其燃烧值低,聚乙烯[(CH2CH2)n]等烯烃聚合物废物燃烧产生的能量与燃油相当,而聚氯乙烯产生的能量仅与纸张相当,且有剧毒的二恶英的深沉(二恶英是目前对人类最毒的物质)。
(1)计算聚氯乙烯中氯的质量分数(相对原子质量数据:氯-35.5;氢-1;碳-12;)。
(2)聚氯乙烯、聚乙烯的原料都是石油。其中。聚乙烯中的CH2=CH2都是来自石油;而聚氯乙烯中的CH2=CHCl,除来自石油外,还有HCl。现有1吨石油,试计算可得到多少吨聚乙烯和聚氯乙烯(理论上假设石油的全部成分为碳和氢,并且在生产聚乙烯、聚氯乙烯的过程中没有碳原子和氢原子的损失)。
(3)如果地球目前所蕴藏的石油全部生产聚乙烯仅可以用50年,则生产聚氯乙烯可以用多少年?
(4)试根据上述信息及计算结果,谈谈人类该如何对待聚氯乙烯的使用。
17.美国《科学美国人》杂志在1971年7月刊登的“地球的能量资源”一文中提供了如下数据:到达地球表面的太阳辐射能的几条主要去路
|
直接反射 |
52,0000×109
千焦/秒 |
|
以热能的方式离开地球 |
81,000×109
千焦/秒 |
|
水循环 |
40,000×109
千焦/秒 |
|
大气流动 |
370×109 千焦/秒 |
|
光合作用 |
40×109 千焦/秒 |
请选用以上数据计算:
(1)地球对太阳能的利用率约为
(2)通过光合作用,每年有 千焦的能转化为化学能(每年按365天计)。
(3)每年由绿色植物通过光合作用(6CO2+6H2O→C6H12O6+6O2)为我们生存的环境除去二氧化碳的质量。试根据能量关系列出的计算式。列式中缺少的数据用符号表示。
A= (千克)所缺数据的化学含义为
16.为测定一种复合氧化物开支的磁性粉末材料的组成,称取12.52克样品,将其全部溶于过量稀硝酸后,配成100毫升溶液。取其一半,加入过量K2SO4溶液,生成白色沉淀,经过滤、洗涤、烘干后得4.66克固体。在余下的50毫升溶液中加入少许KSCN溶液,显红色;如果加入过量NaOH溶液,则生成红褐色沉淀,将沉淀过滤、洗涤、灼烧后得3.20克固体。(1)计算磁性粉末材料中氧元素的质量百分含量。(2)确定该材料的化学式
15.利用天然气合成氨的工艺流程示意如下:
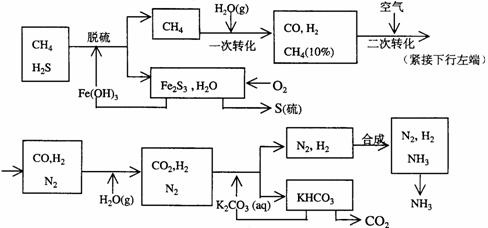
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2 mol(用含n的代数式表示)
(3)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 (多选扣分)
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于 (写出CO2的一种重要用途)。
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3(aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)。
14.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是
(3)控制城市空气污染源的方法可以有 (多选扣分)
a 开发氢能源 b 使用电动车 c 植树造林 d 戴上呼吸面具
13.抽烟对人体有害。烟草不完全燃烧产生的一氧化碳被吸进肺里跟血液中的血红蛋白(用Hb表示)化合,发生下述反应:CO+Hb•O2 ≒O2+Hb•CO实验表明,Hb•CO的浓度即使只有Hb•O2浓度的2%,也足以使人的智力受损。试回答:
(1)上述反应的平衡常数表达式为:K= 。
(2)抽烟后,吸入肺部的空气中测得的CO和O2的浓度分别为10-6摩/升和10-2摩/升。已知37℃时,平衡常数K=220,这时Hb•CO的浓度 (填大于、等于或小于)Hb•O2浓度的0.02倍。
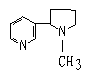 (3)进入肺部的众多有害物质中,除CO外还有一种称为尼古丁的
(3)进入肺部的众多有害物质中,除CO外还有一种称为尼古丁的
剧毒的物质,它的结构简式为:
式中以线示键,线的交点处代表有碳原子,并用原子数补足四价,
但C、H原子都未标记出来。试写出这它的分子式:
12.羟磷灰石[Ca3(PO4)2 ·Ca(OH)2]是牙齿表面的一层坚硬物质,它可保护牙齿,它在唾液中存在如下平衡:
 Ca3(PO4)2 ·Ca(OH)2 4Ca2+
+ 2PO43- + 2OH-
Ca3(PO4)2 ·Ca(OH)2 4Ca2+
+ 2PO43- + 2OH-
(1)进食后,细菌和酶作用于食物产生有机酸,这时牙齿会受到腐蚀,其原因是____________________________________________________________________________________________________。
(2)已知氟磷石灰石[Ca3(PO4)2 ·CaF2]的溶解度比上面的羟磷灰石更小,请用离子方程式表示,当牙膏中配有氟化物后,能防止龋齿的原因
。
(3)根据以上原理,请你提出一种其他促进牙齿矿化的方法
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com