
1. 圆C1: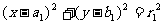 圆C2:
圆C2:
(1) 两圆相离
两圆相离
(2) 两圆相外切
两圆相外切
(3)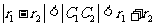 两圆相交
两圆相交
(4)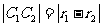 两圆相内切
两圆相内切
(5)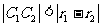 两圆内含
两圆内含
圆的方程二
3.红外光谱仪
用途 。
试题枚举
[例1] 下列实验中所选用的仪器合理的是( )
A. 用200mL量筒量取5.2mL稀硫酸
B. 用250mL容量瓶配制250mL0.2mol/L的氢氧化钠溶液
C. 用托盘天平称量11.7克氯化钠晶体
D. 用碱式滴定管量取25.1mL溴水
解析:这是一道考查称量仪器使用的题目。选用量筒时应注意选合适规格,量取5.2mL稀硫酸要用10mL量筒,所以A不正确;滴定管量取液体时应精确到0.01mL,所以D不正确。
托盘天平可称量精确到0.1克,一般配制多大体积的溶液就选用多大体积的容量瓶。
答案: BC
[变式]准确量取25.00 mL高锰酸钾溶液,可选用的仪器是 ( C )
A . 50 mL量筒 B. 10 mL量筒 C. 50 mL酸式滴定管 D. 50mL碱式滴定管
[例2] 一支40mL碱式滴定管注入苛性钠溶液后,液面正好在10mL刻度处,则苛性钠溶液体积为 ( )
A . 10mL B. 大于10mL C. 30 mL D. 大于30 mL
解析:滴定管的0刻度线在上方,40mL刻度线下至尖嘴处仍有溶液,所以大于30 mL
答案:D
[变式]下列量器和温度计的刻度表示正确的是(CD)
A.量筒的刻度值是由下向上增大,“0”刻度在下
B.250毫升容量瓶上一般刻有30℃250毫升的标记
C.滴定管的刻度值由上而下增大,“0”刻度在上
D.温度计的刻度是由下而上增大,“0”在有刻度标记区域
[例3] 现有下列仪器或用品:①铁架台(含铁圈,各种铁夹);②锥形瓶;③酸式滴定管与碱式滴定管;④烧杯(若干);⑤玻璃棒;⑥胶头滴管;⑦天平(含砝码);⑧滤纸;⑨量筒;⑩过滤漏斗。
(1)过滤时,应选用的上述仪器是 (填编号)。
(2)配制一定物质的量浓度的溶液时,还缺少的仪器是 。
(3)在中和滴定使用滴定管前,首先应 。
解析 这类试题的解题方法是首先看题目选项的具体操作。联想该操作的仪器、方法、注意事项等,对比题目中所给的仪器进行组合,看仪器是否完全具备进行某一项实验,这样才能得出正确结论,有时试题是给出一些仪器来完成某些实验操作,而所给的仪器不全,其解题方法与之类似,即通过联想完成。
答案 (1)过滤所用的仪器有:铁架台、烧杯、玻璃棒、滤纸、过滤漏斗。
(2)配制一定物质的量浓度的仪器有:天平(含砝码)、容量瓶、烧杯、玻璃棒、胶头滴管。
(3)检查活塞是否漏水,在确保不漏水后方可使用。
2.核磁共振仪
用途 。
1.质谱仪
用途 。
15、接触法制硫酸排放的尾气中含少量的SO2,为防止污染大气,在排放前设法进行综合利用。
(1)某硫酸厂每天排放的10000m3尾气0.2%(体积分数)的SO2,问用NaOH溶液、石灰及O2处理后,假设硫元素不损失,理论上可得到多少千克石膏(CaSO4•2H2O)?
(2)如果将一定体积的尾气通入100mL2mol•L-1的NaOH溶液中使其完全反应,经测定所得溶液含16.7g溶质。试分析该溶液的成分,并计算确定各成分的物质的量。
(3)工厂在尾气处理制石膏的过程中,中间产物是NaHSO3。调节尾气排放的流量,以取得SO2与NaOH间物质的量的最佳比值,从而提高亚硫酸氢钠的产量。现设nSO2、nNaOH、nNaHSO3分别表示SO2、NaOH和NaHSO3的物质的量,且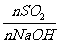 =x,试写出x在不同的取值范围时,n(NaHSO3)的值或NaHSO3与nSO2、nNaOH间的关系式。
=x,试写出x在不同的取值范围时,n(NaHSO3)的值或NaHSO3与nSO2、nNaOH间的关系式。
|
X |
N(NaHSO3) |
|
|
|
|
|
|
|
|
|
14、标准状况下1.68L无色可燃气体在足量氧气完全燃烧。若产物通入足量澄清石灰水,得到的白色沉淀质量为15.0g,若用足量碱石灰吸收燃烧产物,增重9.3g。
(1)计算燃烧产物中水的质量。
(2)若原气体是单一气体,通过计算推断它的分子式。
(3)若原气体是两种等物质的量的气体的混合物,其中一种是烃,请写出它们的分子式。(只要求写出一组)
13、现有等物质的量的NaHCO3、KHCO3的混合物a g与100mL盐酸反应。题中涉及的气体体积均以标准状况计,填空时可以用带字母的公式表示。
(1)该混合物中NaHCO3与KHCO3的质量比为 。
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为 mol·L-1。
(3)如果盐酸过量,生成CO2的体积为 L。
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道
。
(5)若NaHCO3和KHCO3不是以等物质的量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积范围是 。
12、工业上利用氨催化氧化法可制取硝酸,加入脱水剂后制得较高浓度的硝酸。现以17吨氨作为原料,假设NH3全部转化为HNO3。
(1)写出NH3完全转化为HNO3的总化学反应方程式
(2)生产过程中需加水吸收,如果加入脱水剂后脱去水的量相等,则所得硝酸溶液的质量分数为多少?
(3)如果生产中同时制得50%的硝酸m1吨和90%的硝酸m2吨(脱去的水可循环使用,制得教低浓度的稀硝酸),若共加入27吨水,则m1与m2的质量比为多少?
11、氢气和氧气的混合气体为120℃和一定压强下物质的量为amol,点燃后发生反应,待气体恢复到原来的温度和压强时,测得气体的物质的量为bmol,求原昆合气体中氢气和氧气的物质的量各是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com