
12.由氢气和氧气反应生成1mol水蒸气放出241.8kJ的热量,1g水蒸气转化为液态水放出2.45kJ的热量,则下列热化学方程式书写正确的是 ( )
A.H2(g)+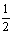 O2(g)=H2O(1);△H=-285.9kJ/mol
O2(g)=H2O(1);△H=-285.9kJ/mol
B.H2(g)+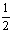 O2(g)=H2O(1);△H=-241.8kJ/mol
O2(g)=H2O(1);△H=-241.8kJ/mol
C.H2(g)+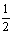 O2(g)=H2O(1);△H=+285.9kJ/mol
O2(g)=H2O(1);△H=+285.9kJ/mol
D.H2(g)+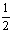 O2(g)=H2O(g);△H=+241.8kJ/mol
O2(g)=H2O(g);△H=+241.8kJ/mol
11.
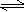 已知热化学方程式2SO3(g)
SO2(g)+O2(g);△H1=+197kJ/mol和热化学方程式2SO2(g)+O2(g) 2SO3(l);△H2=-a kJ/mol,则下列说法正确的是( )
已知热化学方程式2SO3(g)
SO2(g)+O2(g);△H1=+197kJ/mol和热化学方程式2SO2(g)+O2(g) 2SO3(l);△H2=-a kJ/mol,则下列说法正确的是( )
A.a>197 B.a<197
C.a=197 D.热化学方程式中化学计量数表示分子个数
10.含NaOH 20.0g的稀溶液与足量稀盐酸反应,放出28.7kJ的热量,表示该反应中和热的热化学方程式正确的是 ( )
A.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l);△H=+28.7kJ/mol
B.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l);△H=-28.7kJ/mol
C.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l);△H=+57.4kJ/mol
D.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l);△H=-57.4kJ/mol
9.含11.2g KOH的稀溶液与1L、0.1mol/L的H2SO4溶液反应放出11.46KJ的热量,该反应的热化学方程式正确的是 ( )
A.KOH(aq)+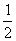 H2SO4(aq)=
H2SO4(aq)=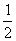 K2SO4(aq)+H2O(l) ΔH= -11.46 KJ/mo1
K2SO4(aq)+H2O(l) ΔH= -11.46 KJ/mo1
B. 2KOH(aq) +H2SO4(aq)= K2SO4(aq)+2H2O(aq) ΔH= -114.6 KJ/mo1
C.2KOH(aq)+ H2SO4(aq)= K2SO4(aq)+2H2Ol ΔH=-114.6 KJ/mo1
D.KOH(aq)+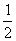 H2SO4(aq)=
H2SO4(aq)=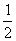 K2SO4(aq)+ H2O(1)
ΔH=-57.3
KJ/mo1
K2SO4(aq)+ H2O(1)
ΔH=-57.3
KJ/mo1
8.通常人们反拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
H-H |
Cl-Cl |
H-Cl |
|
生成1 mol化学键时放出的能量 |
436kJ·mol-1 |
243kJ·mol-1 |
431kJ·mol-1 |
则下列热化学方程式不正确 ( )
A.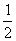 H2(g) +
H2(g) +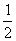 Cl2(g) = HCl(g);△H =-91.5kJ·mol-1
Cl2(g) = HCl(g);△H =-91.5kJ·mol-1
B. H2(g) +Cl2(g) = 2HCl(g);△H =-183kJ·mol-1
C.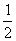 H2(g) +
H2(g) +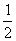 Cl2(g) = HCl(g);△H = + 91.5kJ·mol-1
Cl2(g) = HCl(g);△H = + 91.5kJ·mol-1
D. 2HCl(g) = H2(g) +Cl2(g);△H = + 183kJ·mol-1
7.已知1mol N2(气态)与适量H2(气态)反应,生成NH3(气态),放出92kJ的热量,且形成1mol N-H键时放出391kJ的热量,完全断裂1mol H-H键吸收436kJ的热量,则1mol N2断键时吸收热量的 ( )
A.946 kJ B.135 kJ C.1130 kJ D.780 Kj
6. 关于用水制取二级能源氢气,以下研究方向不正确的是 ( )
A. 设法将太阳光聚集,产生高温,使水分解产生氢气
B. 构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源
C. 寻找特殊化学物质,用于开发廉价能源以分解水制取氢气
D. 寻找高效催化剂,使水分解产生氢气,同时释放能量
5. 下列叙述正确的是 ( )
A. 电能是二级能源 B. 水力是二级能源
C. 天然气是一级能源 D. 水煤气是一级能源
4.充分燃烧一定量的丁烷(C4H10)放出热量为Q,经测定完全吸收它生成的CO2需消耗
5mol/LKOH溶液100mL,恰好生成正盐。则燃烧1mol丁烷放出的热量为 ( )
A.4Q B.5Q C.8Q D.16Q
能源可分为一级能源和二级能源,自然界中以现成形式提供的能源称为一级能源;需要依靠其他能源的能量间接制取的能源称为二级能源。氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:水吸收能量分解为H2和O2。根据以上叙述回答下面两题:
3.海湾战争中,科威特大批油井着火,在灭火工作中,下列措施不能考虑用于灭火的是( )
A.设法阻止石油喷射 B. 设法降低石油着火点
C.设法降低火焰温度 D.设法使火焰隔绝空气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com