
2008年9月27日北京时间16时44分,航天员翟志刚走出“神舟七号”舱门,实现了中国历史上首次太空行走。完成3--4题。
3、对该日的地理状况叙述正确的是
A. 地球在公转轨道上运动速度变慢 B. 太阳直射点北移
C. 内蒙古日出时间大约在5时左右 D. 海口的正午太阳高度比广州的大
4、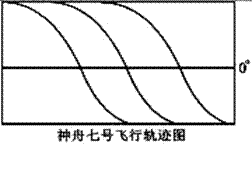 飞船绕地球运行周期是90分钟,
飞船绕地球运行周期是90分钟,
图为神舟七号轨道在地球表面上的投影。
则飞船连续两次在赤道上的投影间距
大约为
A.2200千米
B. 2500千米
C. 2800千米
D. 3000千米
2、下图“太阳直射点在地球表面移动示意图”中的①、②、③、④四处,与日历所示之日太阳直射点位置最接近的是( )
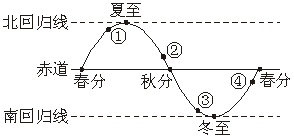
A.① B.② C.③ D.④
23.(共6分)铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l 、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色。现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 。
22、(4分)生活饮用水水质的标准主要有:色度、浑浊度、pH、细菌总数、嗅和味等。目前城市自来水处理过程中所使用的主要试剂仍是Cl2(消毒剂)和Al2(SO4)3(沉降剂),但由于种种原因,用这两种物质处理水质,总有缺陷。有资料报道:Na2FeO4(化合物中Fe呈+6价)是一种强氧化剂,可作为一种新型净水剂,在反应中被还原为Fe3+,因此使用该物质可代替Cl2和Al2(SO4)3。
⑴ 配平工业上制备铁酸钠的化学方程式:
Fe2O3+ NaNO3+ NaOH - Na2FeO4+ NaNO2+ H2O
⑵当反应物中含有1.4 mol Na+,且上述反应恰好完全进行时,电子转移总数为
NA。
21、(12分)根据下边反应框图填空。已知B、D、E、L常温下为密度比空气大的气体,D、E为单质,其他为化合物。A是一种淡黄色固体,C在水中的溶解度随温度的升高而减小,F、G均能与L的水溶液反应放出B。
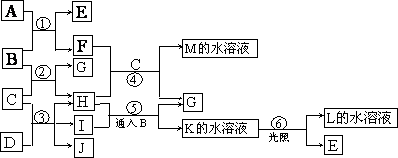
⑴ F的俗名是 。
⑵ 反应①~⑥中,属于氧化还原反应的是 。
⑶ 反应⑤的离子方程式为 。
⑷ 有一种单质能与H反应生成E,该反应的化学方程式为 。
⑸ 写出工业上制取M的化学方程式 ;
F中常混有少量M,如何检验M的存在? 。
20.(6分)某强碱性溶液中可能含有的离子是K+、NH4+、Al 3+ 、AlO2-、SO42- 、SiO32- 、CO32-、Cl-中的某几种离子,现进行如下实验:
①取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成。
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失。
则原溶液中肯定存在的离子是_____________,肯定不存在的离子是________________
已知一定量的原溶液中加入5 mL 0.2 mol/L盐酸时,沉淀会完全消失,再加入足量的硝酸银溶液可得到沉淀0.187 g,则原溶液中是否含有Cl-?_________________。
19.(7分)水是生命之源,也是化学反应中的主角。试回答下列问题:
(1)写出水的电子式 。
(2)A.B.C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A.B.C与水反应的化学方程式:
;
;
。
18.(9分)已知漂白粉的有效成分能与浓盐酸反应生成Cl2和一种能作干燥剂的固体物质等。请从下图中选用适当的实验装置,设计一个最简单的实验,测定漂白粉有效成分的质量分数。
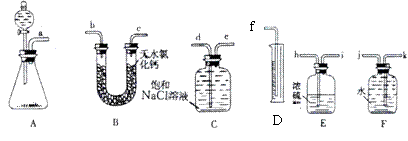

请填写下列空白:
(1)实验中漂白粉有效成分与浓盐酸反应的化学方程式为 。
(2)所选用装置的连接顺序应是(填各接口的字母代号) 。
(3)若各仪器内仍残留有少量Cl2,则测定结果将(填“偏高”、“偏低”或“不影响” ) ,其原因是 。
(4)某同学在实验中发现量筒里未收集到液体,其失败的原因可能是下列中的(填A、B、
C等代号) 。
①装置漏气 ②浓盐酸已变成稀盐酸 ③所选仪器容积太大
④漂白粉已全变质 ⑤e接f ⑥d接f
A.①②③ B.①②④⑤ C.①②④⑥ D.全部
17. (8分) 下面a-e是中学化学实验中常见的几种定量仪器:
a、量筒 b、容量瓶 c、滴定管 d、托盘天平 e、温度计
①能够用以精确量取液体体积的是 (填写编号)
②使用容量瓶的第一步操作是___________________________________ 。
③若用上述仪器配制500mL 2mol·L-1的NaCl溶液,还缺少的玻璃仪器是烧杯_________。
④若用上述仪器测定中和热,则缺少的玻璃仪器为烧杯、__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com