
29.(有机化学)(8分)300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构式为:
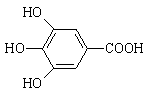
(1)用没食子酸制造墨水主要利用了___________________类化合物的性质(填代号)。
A、醇 B、酚 C、油脂 D、羧酸
(2)没食子酸丙酯且有抗氧化作用,是目前广泛应用的食品添加剂,其结构简式为________________________________________________。
(3)尼泊金酯是对羟基苯甲酸与醇形成的酯类化合物,是国家允许使用的食品防腐剂。尼泊金丁酯的分子式为_________________________,其苯环只与-OH和-COOR两类取代基直接相连的同分异构体有___________种。
(4)写出尼泊金乙酯与氢氧化钠溶液加热反应的化学方程式:
__________________________________________________ ___________
28.(8分)将标准状况下的HCl气体4.48 L溶于水形成100 mL溶液,然后与足量的铁屑充分反应。计算:(1)所得盐酸溶液的物质的量浓度。
(2)参加反应的铁的质量。
(3)生成的H2的体积(标况)。
(4)将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度是多少?
27.(8分)在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:

(1) (2) (3) (4) (5)
(1)连接上述仪器的正确顺序是(填各接口处的字母): 接 ,_____接 ,_____接 , 接 。
(2)在装置中:
①饱和食盐水起的作用是 ,
②浓硫酸起的作用是 ;
(3)该实验中收集氯气用的是 法,若图(2)装满饱和食盐水,也可以用来收集氯气,则收集时氯气应从 (填“C”或“D”)通入。
26.(4分)用98%的浓硫酸(其密度为1.84 g/cm3)配制100 mL 1.0 mol·L-1稀硫酸,若实验仪器有:
A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶 E.10 mL量筒 F.胶头滴管 G.50 mL烧杯 H.100 mL容量瓶
(1)需量取浓硫酸的体积为 mL。
(2)实验时选用的仪器有(填序号)
(3)在容量瓶使用方法中,下列操作不正确的是(填序号)
 A.使用容量瓶前检查它是否漏水
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将浓硫酸稀释后,立即注入容量瓶中
D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(4)配制过程中,下列情况会使配制结果偏高的是(填序号)
①定容时俯视刻度线观察液面
②容量瓶使用前未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
25.(4分)长期以来,人们一直认为氟的含氧酸不存在,自1971年美国科学家用F2通过细冰末获得HFO以来,对HFO的研究引起了充分重视。
⑴HFO的化学名称为
⑵HFO能与水发生反应:HFO+H2O=HF+H2O2,其中氧化剂是 ;
⑶写出F2与水发生发应的化学方程式,并用双线桥法标出该反应中电子转移的方向和数目:
24.(2分)在反应式X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6g X与Y完全反应后,生成4.4g R,则参加反应的Y的质量是____________
23.(2分)在50℃和1.01×105Pa时,相同质量的SO2和SO3的体积比是 ,密度比是___________
22.(2分)与16g氧气所含的原子总数相同的氨气是 g
21.(2分)碘升华实验后的烧杯沾有碘,应用 洗涤
20.用铝箔包装0.1 mol金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为(标准状况)( )
A.O2和H2的混合气体 B.1.12 L H2
C.大于1.12 L H2 D.小于1.12 L气体
第Ⅱ卷(40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com